Perbezaan antara air dan ais

The Perbezaan utama antara air dan ais ialah Air tidak mempunyai susunan molekul yang kerap manakala ais mempunyai struktur kristal tertentu.
Dari peringkat awal evolusi bumi, air telah menjadi sebahagian besar bumi. Bagi hari ini, air meliputi lebih daripada 70% permukaan bumi. Dari ini, sebahagian besar air berada di lautan dan laut; yang kira -kira 97%. Sungai, tasik dan kolam mempunyai 0.6% air, dan kira -kira 2% ada di topi ais kutub dan glasier. Beberapa jumlah air hadir di bawah tanah dan jumlah minit berada dalam bentuk gas sebagai wap dan awan. Di antara ini, terdapat kurang daripada 1% air yang tersisa untuk kegunaan manusia langsung. Air tulen ini juga tercemar dari hari ke hari, dan harus ada rancangan yang tepat untuk memulihara air.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu air
3. Apa itu ais
4. Perbandingan sampingan - Air vs ais dalam bentuk jadual
5. Ringkasan
Apa itu air?
Air adalah sebatian bukan organik yang mempunyai formula kimia h2O. Air adalah sesuatu yang tidak dapat kita jalani tanpa. Dua hidrogen ikatan kovalen dengan atom oksigen untuk membentuk molekul air. Selain itu, molekul mendapat bentuk yang bengkok untuk meminimumkan penolakan ikatan pasangan tunggal elektron, dan sudut H-O-H ialah 104o. Air adalah cecair yang jelas, tidak berwarna, tidak enak, tidak berbau. Tambahan pula, ia boleh berada dalam pelbagai bentuk seperti kabut, embun, salji, ais, wap, dll. Ia pergi ke fasa gas apabila panas melebihi 100 oC pada tekanan atmosfera biasa.
Air benar -benar molekul keajaiban. Ia adalah sebatian tak organik yang paling banyak dalam bahan hidup. Lebih daripada 75% badan kita menyusun air. Di sana, ia adalah komponen sel, bertindak sebagai pelarut dan reaktan. Walau bagaimanapun, ia adalah cecair pada suhu bilik, walaupun ia mempunyai berat molekul rendah 18 gmol-1.

Rajah 01: Air berada dalam fasa cecair
Keupayaan air untuk membentuk ikatan hidrogen adalah ciri unik yang dimilikinya. Di sana, molekul air tunggal dapat membentuk empat ikatan hidrogen. Oksigen lebih elektronegatif daripada hidrogen, menjadikan ikatan O-H dalam kutub molekul air. Kerana polaritas dan keupayaan untuk membentuk ikatan hidrogen, air adalah pelarut yang kuat. Lebih -lebih lagi, kami menyebutnya pelarut sejagat kerana keupayaannya membubarkan sebilangan besar bahan. Selanjutnya, air mempunyai ketegangan permukaan yang tinggi, pelekat tinggi, daya kohesif. Ia dapat menahan perubahan suhu tanpa pergi ke gas atau bentuk pepejal. Kami namakan ini sebagai kapasiti haba yang tinggi, yang seterusnya penting untuk kelangsungan hidup organisma hidup.
Apa itu ais?
Ais adalah bentuk air yang kukuh. Apabila kita memanggil air di bawah 0oC ia mula membekukan ais membentuk. Ais sama ada telus atau sedikit legap. Walau bagaimanapun, kadang -kadang ia mempunyai warna bergantung kepada kekotoran. Selanjutnya, sebatian ini mempunyai struktur kristal biasa yang diperintahkan.

Rajah 02: Ice mengapung di atas air
Ikatan hidrogen adalah penting untuk menjadikan struktur pepejal yang diperintahkan ini dalam ais. Ikatan hidrogen menyimpan h2O molekul dengan jarak tertentu antara satu sama lain, membentuk struktur kristal. Semasa proses ini, jumlah jisim yang sama H2O Memperluas (yang bermaksud jisim air mendapat jumlah yang tinggi apabila pembekuan untuk membentuk ais). Oleh kerana jumlah air berkembang apabila ia membeku, ketumpatan ais lebih rendah daripada air. Oleh itu, ia boleh terapung di atas air. Ini menghalang air di bahagian bawah badan air dari pembekuan pada musim sejuk, dengan itu melindungi kehidupan akuatik.
Apakah perbezaan antara air dan ais?
Ais adalah bentuk air yang kukuh, dan ia mempunyai struktur kristal tertentu, tetapi air tidak mempunyai susunan molekul yang kerap. Jadi, ini adalah perbezaan utama antara air dan ais. Di sini, perbezaan ini timbul kerana kehadiran ikatan hidrogen antara molekul air. Semasa proses pembekuan, ikatan hidrogen memegang h2O molekul pada jarak tertentu antara satu sama lain, memberikan struktur kristal ke ais. Juga, proses ini meningkatkan kelantangan. Oleh itu, sebagai satu lagi perbezaan penting antara air dan ais, kita boleh mengatakan bahawa ais mempunyai ketumpatan yang rendah berbanding dengan air. Oleh itu ia boleh terapung di atas air.
Juga, kita dapat mengenal pasti perbezaan antara air dan ais berdasarkan jumlah dan ketumpatan mereka juga. Itu dia; Untuk jisim yang sama, jumlah air agak lebih rendah daripada ais. Kerana, ketumpatan air lebih tinggi daripada ais. Infographic di bawah perbezaan antara air dan ais menunjukkan lebih banyak perbezaan antara kedua -duanya.
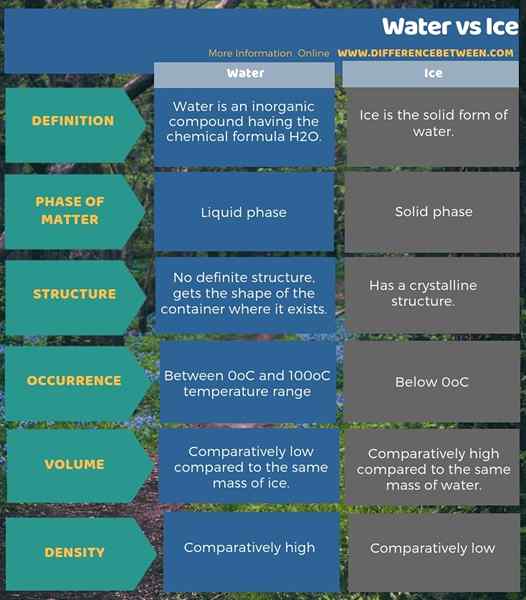
Ringkasan -Air vs ais
Ais adalah bentuk air yang kukuh. Walau bagaimanapun, disebabkan oleh kehadiran ikatan hidrogen antara molekul air, bentuk ais dengan susunan biasa H2O molekul apabila kita menyejukkan di bawah 0oC. Oleh itu, perbezaan utama antara air dan ais adalah bahawa air tidak mempunyai susunan molekul yang kerap manakala ais mempunyai struktur kristal tertentu.
Rujukan:
1. "Ais, air, dan kimia sederhana."Quatr.Panduan Kajian AS, Nama Penerbit Quatr.Logo Penerbit Panduan Panduan AS, 17 Apr. 2018. Terdapat di sini
2. Zumdahl, Steven S. "Air."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 4 Okt. 2018. Terdapat di sini
Ihsan gambar:
1."Kesan penurunan air di permukaan air - (2)" oleh Davide Restivo dari Aarau, Switzerland - Drops #3, (CC BY -SA 2.0) melalui Commons Wikimedia
2."Air dan Ais" oleh Victor Blacus - Kerja Sendiri, (CC BY -SA 4.0) melalui Commons Wikimedia


