Perbezaan antara klorida stannik dan stannous
The Perbezaan utama antara klorida stannic dan stannous adalah Stannic Chloride mempunyai keadaan pengoksidaan +4 timah, sedangkan klorida stannous mempunyai keadaan pengoksidaan +2 timah.
Nama -nama stannic dan stannous merujuk kepada timah elemen kimia yang mempunyai dua keadaan pengoksidaan yang berbeza. Stannic chloride adalah timah (iv) klorida manakala klorida stannous adalah timah (ii) klorida.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu klorida stannik
3. Apa itu klorida stannous
4. Perbandingan sampingan - Stannic vs stannous chloride dalam bentuk jadual
5. Ringkasan
Apa itu klorida stannik?
Stannic chloride adalah timah (iv) klorida. Ia juga dikenali sebagai tetrachloride timah, yang merupakan sebatian bukan organik yang mempunyai formula kimia SNCL4. Kompaun ini adalah cecair hygroscopic yang tidak berwarna yang mengalami fuming apabila bersentuhan dengan udara. Ia mempunyai bau yang acrid. Kompaun ini penting sebagai pendahulu untuk pengeluaran sebatian yang mengandungi timah yang lain. Ia ditemui oleh saintis Andreas Libavius.

Rajah 01: Kompaun klorida stannik
Kita boleh menyediakan klorida stannik melalui tindak balas antara gas klorin dan logam timah pada 115 darjah Celcius. Selain itu, sebatian ini menguatkan kira -kira tolak suhu darjah 33 Celsius. Pemejalan ini memberikan kristal monoklinik, dan struktur ini adalah isostruktur dengan SNBR4. Terdapat beberapa hidrat klorida stannik yang diketahui, seperti bentuk pentahydrate. Struktur terhidrat mempunyai molekul air tambahan yang menghubungkan molekul klorida stannik bersama -sama melalui ikatan hidrogen.
Apabila mempertimbangkan penggunaan stannic chloride, aplikasi utama sebatian ini adalah sebagai pendahulu kepada sebatian organotin yang berguna sebagai pemangkin dan penstabil polimer. Kita boleh menggunakan kompaun ini dalam proses sol-gel untuk menyediakan salutan Sno2, nanocrystals SnO2, dll.
Apa itu klorida stannous?
Stannous Chloride adalah timah (ii) klorida. Ia kelihatan sebagai pepejal kristal putih yang mempunyai formula kimia SNCL2. Bentuk utama sebatian ini adalah bentuk dihydrate, tetapi penyelesaian berair klorida stannous cenderung menjalani hidrolisis apabila penyelesaiannya panas. Selain itu, SNCL2 digunakan secara meluas sebagai ejen pengurangan, dan ia juga penting dalam mandi elektrolitik untuk penyaduran timah. Pepejal putih ini tidak berbau, yang merupakan perbezaan dari stannic chloride.
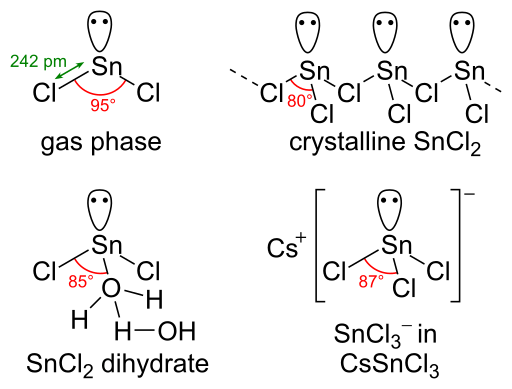
Molekul SNCL2 mempunyai pasangan elektron tunggal; Oleh itu, molekul ini mempunyai geometri bengkok dalam fasa gasnya. Apabila keadaan pepejal klorida stannous dipertimbangkan, ia membentuk struktur rantai yang dikaitkan melalui jambatan klorida.

Rajah 02: Struktur klorida stannous dalam fasa yang berbeza
Kita boleh menyediakan klorida stannous melalui tindakan gas klorida halogen kering pada logam timah. Kita boleh menghasilkan bentuk dihydrate dengan tindak balas yang sama menggunakan asid HCl. Selepas itu, air yang hadir dalam larutan harus dikeluarkan dengan teliti melalui penyejatan untuk mendapatkan kristal dikhidrat klorida stannous. Bentuk dihydrate ini dapat menjalani dehidrasi ke bentuk anhydrous menggunakan anhidrida asetik.
Terdapat banyak kegunaan yang berbeza dari klorida stannous termasuk penyaduran timah keluli, sebagai mordan dalam pencelupan tekstil kerana ia memberikan warna -warna cerah dengan beberapa pewarna, sebagai agen pelindung terhadap hakisan enamel dalam ubat gigi, sebagai pemangkin dalam pengeluaran bahan plastik PLA PLA , sebagai ejen pengurangan, dll.
Apakah perbezaan antara stannic dan stannous chloride?
Nama -nama stannic dan stannous merujuk kepada timah elemen kimia yang mempunyai dua keadaan pengoksidaan yang berbeza. Perbezaan utama antara stannic dan stannous chloride adalah bahawa klorida stannik mempunyai keadaan pengoksidaan +4 timah, sedangkan klorida stannous mempunyai keadaan pengoksidaan +2 timah. Apabila mempertimbangkan penyediaan kedua -dua sebatian ini, stannic chloride boleh dibuat melalui tindak balas antara gas klorin dan logam timah pada 115 darjah Celsius. Stannous Chloride boleh dibuat melalui tindakan gas klorida halogen kering pada logam timah.
Di bawah infographic menyenaraikan lebih banyak perbezaan antara stannic dan stannous chloride.
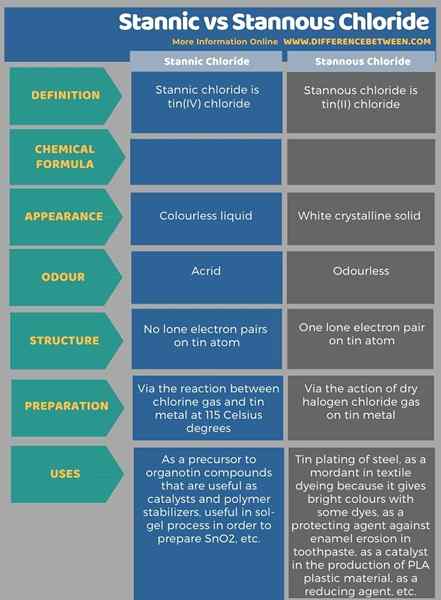
Ringkasan -Stannic vs Stannous Chloride
Nama -nama stannic dan stannous merujuk kepada timah elemen kimia yang mempunyai dua keadaan pengoksidaan yang berbeza. Perbezaan utama antara stannic dan stannous chloride adalah bahawa klorida stannik mempunyai keadaan pengoksidaan +4 timah, sedangkan klorida stannous mempunyai keadaan pengoksidaan +2 timah.
Rujukan:
1. "Stannous Chloride."Stannous Chloride - Gambaran Keseluruhan | Topik Sciencedirect, tersedia di sini.
Ihsan gambar:
1. "Tin (iv) Pentahydrate klorida" (domain awam) melalui Commons Wikimedia
2. "Struktur SNCL2" oleh HBF878 - Kerja Sendiri (CC0) melalui Commons Wikimedia