Perbezaan antara anod dan katod
The Perbezaan utama Antara anod dan katod ialah Anod adalah terminal positif manakala katod adalah terminal negatif.
Anod dan katod adalah elektrod dengan polariti yang bertentangan. Untuk mengetahui perbezaan antara anod dan katod, kita perlu memahami apa yang mereka ada. Anod dan katod adalah elektrod yang digunakan untuk menjalankan arus elektrik ke dalam atau keluar dari mana -mana peranti yang menggunakan elektrik. Elektrod adalah bahan yang mengendalikan yang membolehkan arus melaluinya. Elektrod biasanya diperbuat daripada logam seperti tembaga, nikel, zink, dll. Tetapi beberapa elektrod juga diperbuat daripada bukan logam seperti karbon. Selain itu, elektrod melengkapkan litar dengan melewati semasa melaluinya.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu anod
3. Apa itu katod
4. Perbandingan sampingan -anod vs katod dalam bentuk jadual
5. Ringkasan
Apa itu anod?
Anod adalah elektrod di mana arus meninggalkan sel dan di mana pengoksidaan berlaku. Kami juga menyebutnya elektrod positif. Bateri mudah terdiri daripada tiga bahagian utama: anod, katod dan elektrolit. Secara tradisinya, elektrod berada di hujung bateri. Apabila kita menyambungkan hujung ini dengan elektrik, tindak balas kimia bermula di dalam bateri. Di sini, elektron terganggu dan perlu menyusun semula. Mereka menangkis satu sama lain dan bergerak ke arah katod, yang mempunyai lebih sedikit elektron. Ini mengimbangi elektron sepanjang penyelesaian (elektrolit).
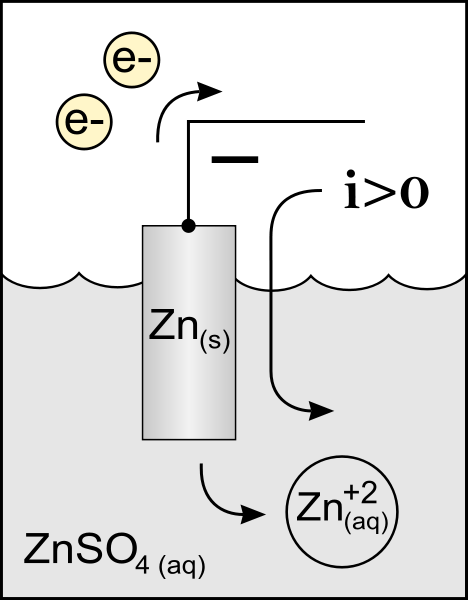
Rajah 01: Anod zink
Secara umum, arus mengalir keluar dari katod apabila peranti sedang dilepaskan. Walau bagaimanapun, arah semasa membalikkan apabila peranti sedang dikenakan dan katod mula berfungsi sebagai anod sementara anod menjadi katod.
Dalam sel utama atau bateri, terminal tidak dapat dibalikkan, yang bermaksud bahawa anod akan sentiasa positif. Ini kerana kami selalu menggunakan peranti ini untuk menunaikan arus elektrik. Tetapi sekiranya sel atau bateri sekunder, elektrod boleh diterbalikkan apabila peranti dilepaskan, tetapi juga menerima semasa untuk mengecas.
Apa itu katod?
Katod adalah elektrod di mana arus memasuki sel dan pengurangan berlaku. Kita juga boleh menyebutnya elektrod negatif. Walau bagaimanapun, katod boleh negatif dalam sel elektrolisis dan positif dalam sel galvanik.

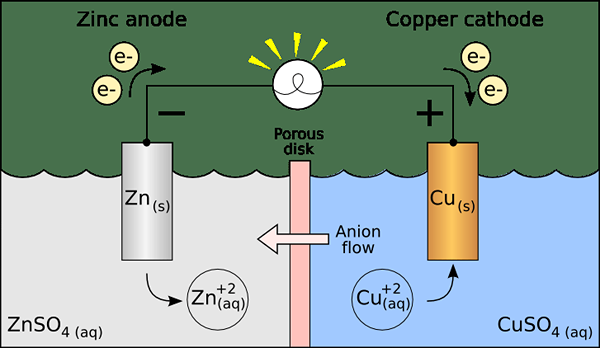
Rajah 02: Anod dan katod dalam sel elektrolisis
Katod menyediakan elektron untuk kation (ion yang dikenakan secara positif). Ion ini mengalir ke katod melalui elektrolit. Selain itu, arus katodik adalah aliran elektron dari katod ke kation dalam penyelesaian. Walau bagaimanapun, istilah katod dan anod mungkin merujuk kepada makna yang berbeza dalam aplikasi yang berbeza.
Apakah perbezaan antara anod dan katod?
Anod adalah elektrod di mana arus meninggalkan sel dan di mana pengoksidaan berlaku semasa katod adalah elektrod di mana arus memasuki sel dan pengurangan berlaku. Perbezaan utama antara anod dan katod ialah anod adalah terminal positif manakala katod adalah terminal negatif. Walau bagaimanapun, terdapat juga elektrod bipolar yang boleh berfungsi sebagai kedua -dua anod dan katod. Umumnya, anod menarik anion dan katod menarik kation, yang telah membawa nama elektrod ini.
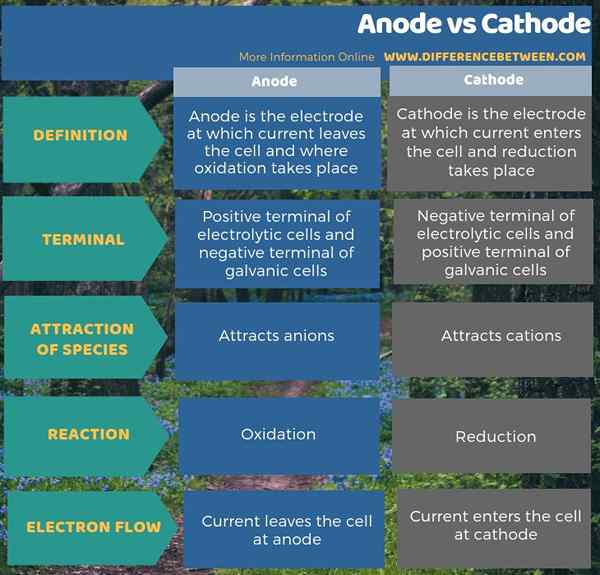
Ringkasan -Anode vs Cathode
Anod adalah elektrod di mana arus meninggalkan sel dan di mana pengoksidaan berlaku semasa katod adalah elektrod di mana arus memasuki sel dan pengurangan berlaku. Perbezaan utama antara anod dan katod ialah anod adalah terminal positif manakala katod adalah terminal negatif.
Rujukan:
1. "Cathode."Wikipedia, Yayasan Wikimedia, 27 Jun 2019, boleh didapati di sini.
Ihsan gambar:
1. "Anode Zink 2" - Kerja Asal: Fail: Anode Zink 2.PNG oleh Pengguna: Micheljullian (bercakap) Kerja Derivatif: Kes47 (Talk) - Fail: Zink Anode 2.PNG (CC BY-SA 3.0) melalui Commons Wikimedia
2. "Sel Galvanik Tanpa Aliran Kation"- Pemuat semula asal adalah Ohiostandard di Wikipedia Bahasa Inggeris. - Dipindahkan dari en.Wikipedia ke Commons oleh Burpelson AFB menggunakan Commonshelper (CC BY-SA 3.0) melalui Commons Wikimedia


