Apakah perbezaan antara ikatan berganda yang konjugasi dan terpencil
The Perbezaan utama antara ikatan berganda yang konjugasi dan terpencil adalah ikatan berganda yang konjugasi merujuk kepada struktur organik yang mempunyai ikatan berganda dan ikatan tunggal, sedangkan ikatan berganda terpencil merujuk kepada struktur organik di mana tidak ada ikatan berganda dan tunggal dan ikatan berganda berada dalam susunan rawak.
Istilah ikatan berganda dalam kimia merujuk kepada struktur di mana dua atom terikat antara satu sama lain melalui ikatan sigma dan ikatan pi. Dalam kimia organik, ikatan berganda merupakan ciri penting dalam sebatian organik di mana terdapat ikatan sigma dan ikatan Pi antara dua atom karbon.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa ikatan berganda konjugasi
3. Apa ikatan berganda terpencil
4. Konjugasi vs ikatan berganda terpencil dalam bentuk jadual
5. Ringkasan -Bon Double Conjugated vs Terasing
Apa ikatan berganda konjugasi?
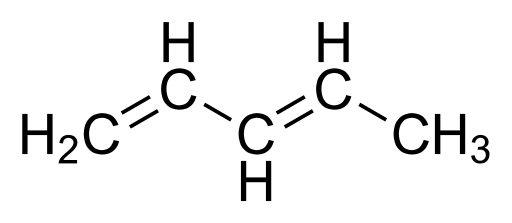
Bon berganda yang konjugasi adalah dua atau lebih bon ganda yang dipisahkan oleh bon tunggal. Dalam erti kata lain, jika terdapat lebih daripada dua ikatan berganda dalam struktur kimia, ikatan berganda ini disusun dalam corak seli dengan ikatan tunggal.
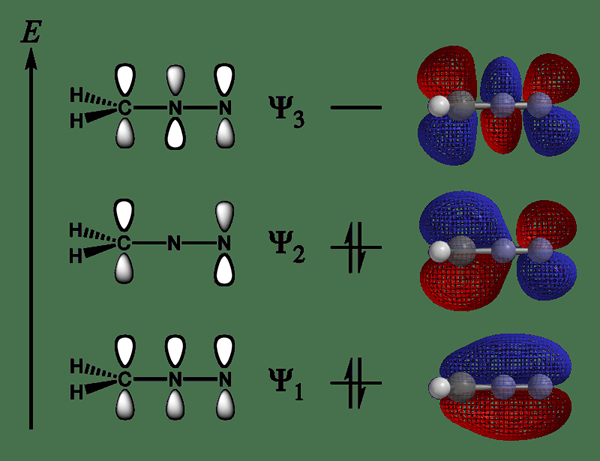
Sistem konjugasi ikatan berganda dan bon tunggal menyebabkan pembentukan sistem konjugasi yang mempunyai elektron yang disahpepijat. Ini bermakna sistem konjugasi mempunyai elektron yang tersebar di seluruh sistem konjugasi dan bukannya wujud dalam kedudukan tetap pada ikatan berganda. Ini dipanggil penyahkawalan. Penyingkiran ini biasanya mengurangkan tahap tenaga struktur, dengan itu meningkatkan kestabilan struktur. Bon berganda konjugasi boleh berlaku dalam struktur cincin, struktur aciklik, struktur linear, atau struktur campuran yang mempunyai struktur kitaran dan linear.

Istilah konjugasi merujuk kepada pencampuran atau pertindihan orbital P satu atom dengan orbital lain dalam ikatan sigma bersebelahan. Oleh itu, sistem konjugasi mempunyai kawasan di mana orbital p bertindih antara satu sama lain.
Apa ikatan berganda terpencil?
Ikatan berganda terpencil adalah ikatan kimia yang diperbuat daripada ikatan sigma dan ikatan pi. Biasanya, istilah ini digunakan apabila ikatan berganda dalam struktur organik tidak diatur dalam corak bergantian dengan ikatan tunggal. Dengan kata lain, ikatan berganda terpencil mempunyai dua atau lebih ikatan tunggal di antara mereka dan diatur secara rawak.
Oleh itu, ikatan berganda ini cenderung mengambil bahagian dalam tindak balas kimia seolah -olah terdapat satu ikatan berganda di sebatian. Di sini, tidak seperti dalam sistem konjugasi, tidak ada penyingkiran elektron yang berlaku. Ini kerana ikatan berganda dipisahkan antara satu sama lain, dan tidak ada kemungkinan untuk bertindih dari orbital p.
Apakah perbezaan antara ikatan berganda yang konjugasi dan terpencil?
Bon berganda yang konjugasi dan terpencil adalah dua jenis ikatan berganda. Perbezaan utama antara ikatan berganda yang konjugasi dan terpencil ialah ikatan berganda yang konjugasi bermaksud struktur organik yang mempunyai ikatan berganda bergilir dan ikatan tunggal, sedangkan ikatan berganda terpencil bermakna struktur organik di mana tidak ada ikatan berganda dan tunggal dan ikatan berganda berada dalam a susunan rawak.
Infographic di bawah menyenaraikan perbezaan antara ikatan berganda dan terpencil dalam bentuk tabular untuk perbandingan sampingan.
Ringkasan -Bon Double Conjugated vs Terasing
Bon berganda yang konjugasi dan terpencil adalah dua jenis ikatan berganda. Perbezaan utama antara ikatan berganda yang konjugasi dan terpencil ialah ikatan berganda yang konjugasi bermaksud struktur organik yang mempunyai ikatan berganda bergilir dan ikatan tunggal, sedangkan ikatan berganda terpencil bermakna struktur organik di mana tidak ada ikatan berganda dan tunggal dan ikatan berganda berada dalam a susunan rawak.
Rujukan:
1. "14.5: Dua ikatan berganda jiran: Dienes Konjugasi." Kimia Libreetexts, Libretexts, 14 Julai 2020.
Ihsan gambar:
1. "1,3-pentadien" oleh Cäsium137 (d.) - Kerja Sendiri (Teks Asal: Selbst Erstellt) (Domain Awam) melalui Commons Wikimedia
2. "Diazomethane-Pi-System" oleh Ben Mills-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia


