Perbezaan antara pH dan penyangga
The Perbezaan utama antara pH dan penimbal ialah pH adalah skala logaritma manakala penampan adalah penyelesaian berair.
Kita boleh menggunakan pH cecair untuk menentukan sama ada ia adalah asid atau asas. Ia juga membantu dalam menentukan kapasiti penampan penampan. Penyelesaian penampan mengandungi campuran asid lemah dan asas konjugasi, atau sebaliknya. Oleh itu, ia cenderung untuk menahan perubahan dalam pH penyelesaian.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu pH
3. Apa itu penampan
4. Perbandingan sampingan - pH vs buffer dalam bentuk jadual
5. Ringkasan
Apa itu pH?
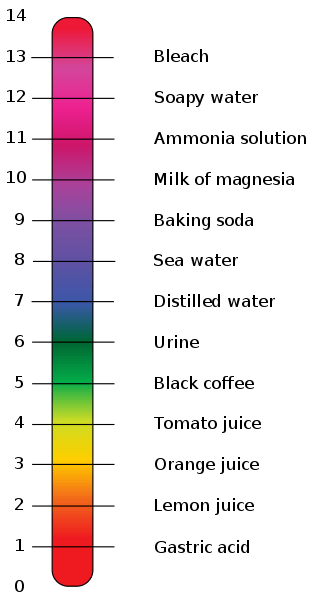
pH adalah skala logaritma yang kami gunakan untuk menentukan keasidan atau asas penyelesaian berair. Ia adalah asas negatif 10 logaritma kepekatan ion hidrogen yang diukur dalam unit mol/l. Sekiranya kita menyatakannya dengan lebih tepat, kita harus menggunakan aktiviti ion hidrogen dan bukannya kepekatan. Skala pH mempunyai nombor dari 0 hingga 14. Penyelesaian yang mempunyai pH kurang daripada 7 adalah berasid dan jika pH lebih tinggi daripada 7, ia adalah penyelesaian asas. PH 7 menunjukkan penyelesaian neutral, i.e. air tulen.

Rajah 01: pH komponen yang berbeza
Persamaan untuk penentuan pH adalah seperti berikut:
ph = log10(aH+)
Di sini "A" adalah aktiviti ion hidrogen (h+). Nilai pH bergantung pada suhu penyelesaian kerana suhu dapat mengubah aktiviti spesies kimia. Oleh itu, apabila memberikan pH penyelesaian berair, kita harus menunjukkan suhu di mana pH diukur dengan tepat. Kami menggunakan skala pH untuk menentukan kualiti air, tanah, dll.
Apa itu penampan?
Penampan adalah penyelesaian berair yang cenderung untuk menahan perubahan dalam pH. Penyelesaian ini mengandungi campuran asid lemah dan asas konjugasi atau sebaliknya. PH penyelesaian ini sedikit berubah apabila penambahan sama ada asid kuat atau asas yang kuat.
Asid lemah (atau asas) dan asas konjugasi (atau asid konjugasi) berada dalam keseimbangan antara satu sama lain. Kemudian jika kita menambah beberapa asid kuat ke sistem ini, keseimbangan beralih ke arah asid, dan ia membentuk lebih banyak asid menggunakan ion hidrogen yang dikeluarkan dari asid kuat tambahan. Oleh itu, walaupun kami menjangkakan peningkatan ion hidrogen apabila penambahan asid yang kuat, ia tidak banyak meningkatkannya. Begitu juga, jika kita menambah asas yang kuat, kepekatan ion hidrogen berkurangan dengan kurang daripada jumlah yang dijangkakan untuk kuantiti Alkali ditambah. Kita dapat mengukur rintangan ini terhadap perubahan pH sebagai kapasiti penampan. Kapasiti penampan mengukur rintangan penampan kepada perubahan pH pada penambahan OH- ion (asas). Kita boleh memberikannya dalam persamaan seperti berikut:
β = dn/d (ph)
Di mana β adalah kapasiti penampan, DN adalah jumlah asas tambahan yang ditambah, dan d (pH) adalah perubahan kecil yang terhasil dalam pH.
Apabila mempertimbangkan aplikasi penampan, penyelesaian ini diperlukan untuk memastikan pH yang betul untuk aktiviti enzimatik dalam organisma. Selain itu, ini digunakan dalam industri dalam proses penapaian, menetapkan keadaan yang betul untuk pewarna, dalam analisis kimia, menentukur pH meter, dll.
Apakah perbezaan antara pH dan penampan?
pH adalah skala logaritma yang kita gunakan untuk menentukan keasidan atau asas larutan berair sedangkan, penampan adalah larutan akueus yang cenderung untuk menahan perubahan dalam pH. Ini adalah perbezaan utama antara pH dan penampan. Selain itu, pH adalah skala yang sangat penting dalam kimia. Kita dapat mengukur pH penyelesaian menggunakan meter pH atau melalui kaedah eksperimen. Selain itu, kami menggunakan skala pH untuk menentukan kualiti air, tanah, dll. Sebaliknya, penggunaan penyelesaian penampan adalah untuk mengekalkan pH yang betul untuk aktiviti enzimatik, dalam proses penapaian dalam industri, dalam menetapkan keadaan yang betul untuk pewarna, dalam analisis kimia, menentukur pH meter, dll. Kami mengukur kapasiti penampan penampan menggunakan analisis kimia.

Ringkasan -PH vs Buffer
pH adalah skala asas yang kita gunakan dalam kimia untuk mengukur asas keasidan penyelesaian penyelesaian. Buffer adalah penyelesaian kimia yang dapat menahan perubahan dalam pH. Oleh itu, perbezaan antara pH dan penampan ialah pH adalah skala logaritma manakala penampan adalah penyelesaian berair.
Rujukan:
1. "Ph."Wikipedia, Yayasan Wikimedia, 3 Ogos. 2018. Terdapat di sini
2. "Penyelesaian Buffer."Wikipedia, Yayasan Wikimedia, 27 Julai 2018. Terdapat di sini
Ihsan gambar:
1."Skala Ph" oleh Edward Stevens - Kerja Sendiri, (CC oleh 3.0) melalui Commons Wikimedia


