Perbezaan antara oksida dan dioksida
The Perbezaan utama antara oksida dan dioksida ialah Oxide adalah sebatian yang mempunyai satu atau lebih atom oksigen yang digabungkan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandungi dua atom oksigen dalam molekulnya.
Istilah oksida adalah istilah umum yang menggambarkan kehadiran atom oksigen dalam sebatian. Di sini, atom oksigen wujud dalam kombinasi dengan elemen kimia lain; kebanyakan logam dan bukan logam. Menurut bilangan atom oksigen di dalam kompaun, kita boleh menamakannya sebagai monoksida, dioksida, trioksida, dan lain -lain. Oleh itu, dioksida adalah oksida yang mengandungi dua atom oksigen setiap molekul.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu oksida
3. Apa itu dioksida
4. Perbandingan sampingan -oksida vs dioksida dalam bentuk jadual
5. Ringkasan
Apa itu oksida?
Oksida adalah sebatian yang mempunyai satu atau lebih atom oksigen yang digabungkan dengan elemen kimia lain. "Oksida" di sini adalah anion divalen (o2-). Biasanya, oksida logam mengandungi dianion ini di mana atom oksigen berada dalam keadaan pengoksidaan -2. Kecuali gas inert ringan (termasuk helium, neon, argon dan krypton), oksigen boleh membentuk oksida dengan semua elemen lain.
Dalam pembentukan oksida, logam dan bukan logam dapat menunjukkan keadaan pengoksidaan terendah dan tertinggi mereka. Sesetengah oksida adalah sebatian ionik; logam alkali, logam bumi alkali dan logam peralihan membentuk oksida ionik ini. Sebatian lain mempunyai sifat kovalen; Logam dengan keadaan pengoksidaan yang tinggi boleh membentuk oksida kovalen. Selain itu, bukan logam membentuk sebatian oksida kovalen.
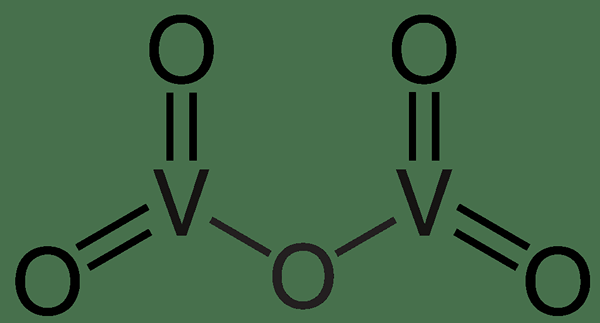
Rajah 01: Vanadium (v) oksida
Dalam imej di atas, atom logam vanadium mempunyai valensi 5 (jumlah valensi adalah 10 untuk dua atom vanadium) oleh itu, lima atom oksigen (dengan valensi 2 setiap atom oksigen) terikat kepada mereka.
Selain itu, beberapa sebatian organik juga bertindak balas dengan oksigen (atau ejen pengoksidaan) untuk menghasilkan oksida, e.g. amina oksida, oksida fosfin, sulfoksida, dll. Tambahan pula, bilangan atom oksigen dalam sebatian menentukan sama ada ia adalah monoksida, dioksida atau trioksida.
Menurut sifat mereka, ia juga mungkin untuk mengkategorikannya sebagai oksida berasid, asas, neutral dan amphoterik. Oksida berasid boleh bertindak balas dengan asas dan membentuk garam. Cth: sulfur trioksida (SO3). Oksida asas bertindak balas dengan asid dan membentuk garam. Cth: Natrium oksida (Na2O). Neutral tidak menunjukkan sifat berasid atau asas; Oleh itu, mereka tidak membentuk garam apabila bertindak balas dengan asid atau pangkalan. Cth: Carbon Monoxide (CO). Oksida amphoterik mempunyai sifat berasid dan asas; Oleh itu, mereka bertindak balas dengan kedua -dua asid dan asas untuk membentuk garam. Cth: Zink Oxide (ZnO).
Apa itu dioksida?
Dioksida adalah oksida yang mengandungi dua atom oksigen dalam molekulnya. Molekul harus mengandungi elemen kimia dengan valensi 4 untuk membentuk dioksida. Kerana satu atom oksigen menunjukkan valensi 2. Contohnya, dalam karbon dioksida, valensi karbon adalah 4.

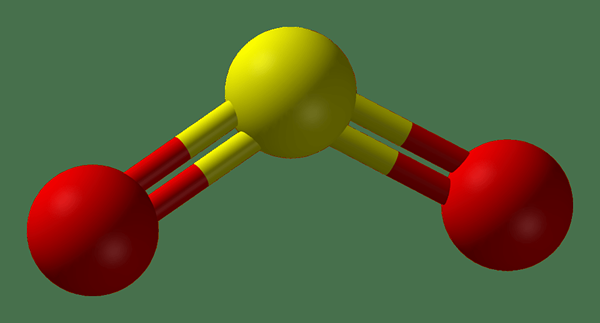
Rajah 02: Struktur bola dan tongkat sulfur dioksida
Beberapa contoh dioksida
- Karbon dioksida (CO2)
- Nitrogen dioksida (tidak2)
- Oksigen (o2)
- Kuarza atau silikon dioksida (SIO2)
Apakah perbezaan antara oksida dan dioksida?
Dioksida adalah sejenis oksida. Perbezaan utama antara oksida dan dioksida ialah oksida adalah sebatian yang mempunyai satu atau lebih atom oksigen yang digabungkan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandungi dua atom oksigen dalam molekulnya. Apabila mempertimbangkan valensi oksida, valensi oksigen adalah 2, dan valensi unsur -unsur lain boleh berbeza -beza; Walau bagaimanapun, untuk dioksida, valensi oksigen adalah 2 dan valensi elemen lain pada dasarnya adalah 4. Jadi, kita juga boleh menganggap ini sebagai perbezaan antara oksida dan dioksida.

Ringkasan -oksida vs dioksida
Oksida adalah istilah umum yang kami gunakan untuk menamakan mana -mana sebatian yang mengandungi atom oksigen dalam kombinasi dengan elemen lain. Selain itu, mengikut bilangan atom oksigen, kita boleh menamakannya sebagai monoksida, dioksida, trioksida, dan lain -lain. Perbezaan utama antara oksida dan dioksida ialah oksida adalah sebatian yang mempunyai satu atau lebih atom oksigen yang digabungkan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandungi dua atom oksigen dalam molekulnya.
Rujukan:
1."Oksida." Wikipedia, Yayasan Wikimedia, 2 Jun 2019, boleh didapati di sini.
Ihsan gambar:
1. "Vanadium (V) Oxide" oleh Kemikungen - Kerja Sendiri (Domain Awam) melalui Wikimedia Commons
2. "Sulfur-Dioxide-3D-Balls" oleh Ben Mills-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia