Perbezaan antara deaminasi oksidatif dan nonoksida
The Perbezaan utama antara deaminasi oksidatif dan nonoksidatif ialah Deaminasi oksidatif berlaku melalui pengoksidaan asid amino kumpulan amino manakala pengurangan nonoksidatif berlaku melalui tindak balas selain daripada pengoksidaan.
Deaminasi adalah, seperti namanya, penyingkiran kumpulan amina dari mana -mana molekul. Ini adalah tindak balas kimia yang dipangkin oleh enzim deaminase. Di dalam badan kita, tindak balas jenis ini berlaku di hati dan kadang -kadang di buah pinggang juga (contohnya: deaminasi glutamat dalam buah pinggang). Di sana, kumpulan amina yang dikeluarkan berubah menjadi ammonia dan dikeluarkan dari badan kita. Tambahan pula, terdapat empat reaksi utama yang berlaku sebagai tindak balas deaminasi; Mereka adalah pengoksidaan, pengurangan, hidrolisis, dan tindak balas intramolekul. Daripada ini, kecuali pengoksidaan, tindak balas lain adalah tindak balas nonoksida.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu deaminasi oksidatif
3. Apakah deaminasi nonoksidatif
4. Perbandingan sampingan - oksidatif vs deaminasi nonoksida dalam bentuk jadual
5. Ringkasan
Apa itu deaminasi oksidatif?
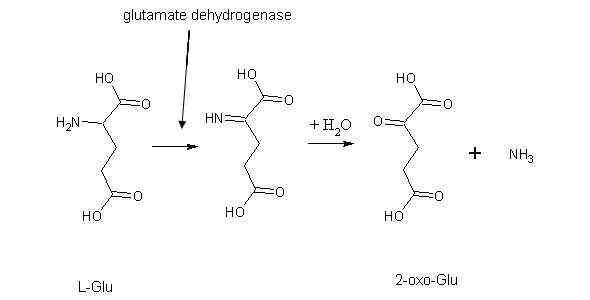
Deaminasi oksidatif adalah proses penyingkiran kumpulan amina dari molekul melalui pengoksidaan. Tindak balas jenis ini sebahagian besarnya berlaku di hati dan buah pinggang. Ia melibatkan penjanaan asid alfa-keto dan beberapa produk teroksida lain dari kumpulan amina. Reaksi ini sangat penting dalam katabolisme asid amino. Ia membentuk produk katabol dari asid amino. produk sampingan tindak balas ini adalah ammonia yang merupakan produk sampingan toksik. Di sini, kumpulan amina berubah menjadi ammonia. Dan kemudian, ammonia ini berubah menjadi urea dan dikeluarkan dari badan kita.

Rajah 01: Pengurangan oksidatif glutamat
Kebanyakan masa, asid glutamat atau glutamat adalah reaktan utama tindak balas jenis ini. Kerana, asid glutamat adalah produk akhir dari banyak reaksi transaminasi yang berlaku di sel kita. Tambahan pula, enzim yang terlibat dalam tindak balas ini adalah glutamat dehidrogenase. Enzim ini memangkinkan pemindahan kumpulan amino ke kumpulan asid alfa-keto. Juga, terdapat enzim lain yang melibatkan dalam tindak balas jenis ini. Ia adalah enzim oksidase monoamine yang memangkinkan deaminasi melalui penambahan oksigen.
Apakah deaminasi nonoksidatif?
Deaminasi nonoksidatif adalah proses penyingkiran kumpulan amina dari molekul melalui tindak balas yang berbeza selain daripada pengoksidaan. Kami menyebutnya "deaminasi langsung" tanpa pengoksidaan. Reaksi ini termasuk pengurangan, hidrolisis dan tindak balas intramolekul. Walau bagaimanapun, tindak balas ini juga melibatkan pengeluaran ammonia produk sampingan toksik dari asid amino. Selain itu, asid amino yang paling biasa yang menjalani tindak balas jenis ini adalah serine, threonine, sistein dan histidin. Begitu juga, enzim yang paling biasa yang terlibat dalam tindak balas ini adalah dehidratase, lirik dan hidrolase amida.
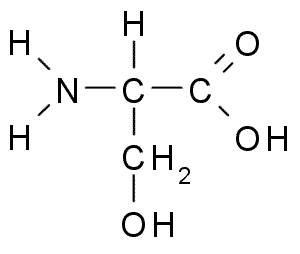
Rajah 02: Serine yang mengalami deaminasi nonoksida
Pengurangan pengurangan berlaku melalui pengurangan kumpulan amina ke dalam asid lemak. Deaminasi hidrolitik melibatkan penukaran kumpulan amina ke dalam kumpulan asid hidroksi. Dari tindak balas intramolekul, kumpulan amina berubah menjadi kumpulan asid lemak tak tepu. Sebagai contoh, enzim dehydratase boleh menukar serine menjadi piruvat dan ammonia dan juga dapat menukar threonine menjadi alpha-ketobutyrate dan ammonia.
Apakah perbezaan antara deaminasi oksidatif dan nonoksida?
Deaminasi adalah penyingkiran kumpulan amina dari molekul. Oleh itu, dalam deaminasi, kumpulan amina menukar kepada produk lain yang berbeza bergantung kepada jenis tindak balas yang berlaku. Perbezaan utama antara pengoksidaan oksidatif dan nonoksidatif adalah bahawa pengurangan oksidatif berlaku melalui pengoksidaan asid amino kumpulan amino manakala pengurangan nonoksidatif berlaku melalui tindak balas selain daripada pengoksidaan. Kerana perbezaan ini, tindak balas kimia yang terlibat dalam proses ini juga berbeza antara satu sama lain. Iaitu, deaminasi oksidatif melibatkan pengoksidaan manakala pengurangan nonoksidatif melibatkan pengurangan, hidrolisis atau reaksi intramolekul. Tambahan pula, perbezaan yang signifikan antara pengoksidaan oksidatif dan nonoksidatif adalah dalam enzim yang terlibat dalam reaksi ini. Iaitu, glutamat dehidrogenase dan monoamine oxidase melibatkan dalam proses oksidatif manakala dehidratase, lyase, dan amide hidrolase melibatkan dalam proses nonoksidatif sebagai enzim.
Infographic di bawah menggariskan perbezaan antara pengurangan oksidatif dan nonoksidatif dalam bentuk jadual.
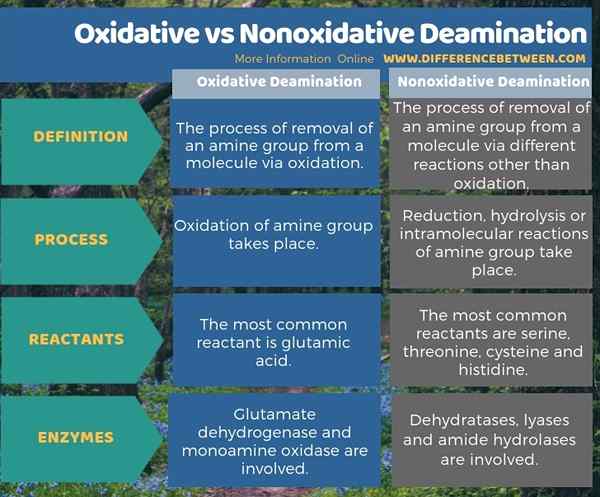
Ringkasan -Oxidative vs deaminasi nonoksida
Deamination adalah pembebasan ammonia melalui deaminasi kumpulan amina. Terdapat dua jenis utama pengoksidaan oksidatif dan nonoksida. Deaminasi nonoksidatif termasuk reaksi selain daripada pengoksidaan seperti pengurangan, hidrolisis, dan reaksi intramolekul. Oleh itu, perbezaan utama antara pengoksidaan oksidatif dan nonoksidatif adalah bahawa pengurangan oksidatif berlaku melalui pengoksidaan asid amino kumpulan amino manakala pengurangan nonoksidatif berlaku melalui tindak balas selain daripada pengoksidaan.
Rujukan:
1. "Deaminasi oksidatif."Wikipedia, Yayasan Wikimedia, 24 Apr. 2018. Terdapat di sini
2. Ahmed, Minhaz. "Transdeamin dan deaminasi."LinkedIn Slideshare, 24 Apr. 2014. Terdapat di sini
Ihsan gambar:
1."Deamination Oxidative" oleh Tomas Drab - Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2."Serine" (CC BY-SA 3.0) melalui Commons Wikimedia


