Perbezaan antara plumbum dan timah

The Perbezaan utama antara plumbum dan timah adalah Lead adalah logam kelabu logam dengan warna biru sedangkan timah adalah logam putih keperakan dengan warna kuning yang lemah.
Lead and Tin adalah kumpulan 14 elemen kimia dalam jadual berkala elemen. Kumpulan elemen ini dipanggil kumpulan karbon kerana ahli pertama kumpulan ini adalah elemen kimia biasa "Karbon".
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa yang memimpin
3. Apa itu timah
4. Perbandingan sampingan - Lead vs Tin dalam bentuk jadual
5. Ringkasan
Apa yang memimpin?
Lead adalah elemen kimia yang mempunyai nombor atom 82 dan simbol kimia PB. Ini adalah elemen kimia logam, dan dikategorikan sebagai logam berat yang lebih padat daripada bahan yang paling biasa yang kita tahu. Walau bagaimanapun, Lead adalah logam lembut dan lembut yang mempunyai titik lebur yang rendah. Kita boleh memotong logam ini dan dapat melihat petunjuk biru ciri bersama dengan penampilan logam kelabu keperakan. Logam ini boleh mencemarkan pendedahan ke udara, yang memberikan permukaan logam penampilan kelabu yang membosankan. Lebih penting lagi, Lead mempunyai bilangan atom tertinggi dari unsur yang stabil.

Rajah 01: Lead
Lead adalah logam selepas peralihan yang tidak aktif. Kita dapat menggambarkan watak metalik yang lemah memimpin menggunakan sifat amphoteriknya. E.g. Lead dan Lead Oxides bertindak balas dengan asid dan asas dan cenderung membentuk ikatan kovalen. Kita dapat mencari sebatian plumbum sering mempunyai +2 pengoksidaan keadaan plumbum dan bukannya keadaan pengoksidaan +4 (+4 adalah pengoksidaan yang paling biasa untuk kumpulan 14 elemen kimia).
Apabila mempertimbangkan sifat pukal plumbum, ia mempunyai ketumpatan tinggi, kelembapan, kemuluran, dan rintangan yang tinggi terhadap kakisan akibat passivasi. Lead mempunyai struktur padu berpusatkan wajah yang penuh dengan berat dan berat atom yang tinggi, yang menghasilkan ketumpatan yang lebih besar daripada ketumpatan logam yang paling biasa seperti besi, tembaga, dan zink. Apabila dibandingkan dengan kebanyakan logam, plumbum mempunyai titik lebur yang sangat rendah, dan titik mendidihnya juga paling rendah di kalangan kumpulan 14 elemen.
Lead cenderung membentuk lapisan pelindung apabila terdedah kepada udara yang mempunyai komposisi yang berbeza -beza. Penyusun yang paling biasa dari lapisan ini adalah plumbum (ii) karbonat. Juga, terdapat komponen sulfat dan klorida plumbum. Lapisan ini menjadikan permukaan logam plumbum secara berkesan secara kimia tidak aktif ke udara. Tambahan pula, gas fluorin boleh bertindak balas dengan plumbum dalam suhu bilik untuk membentuk plumbum (ii) fluorida. Terdapat tindak balas yang sama dengan gas klorin juga, tetapi memerlukan pemanasan. Selain itu, logam plumbum tahan terhadap asid sulfurik dan asid fosforik tetapi bertindak balas dengan asid HCl dan HNO3. Asid organik seperti asid asetik dapat membubarkan plumbum dengan kehadiran oksigen. Begitu juga, asid alkali pekat boleh membubarkan membawa kepada bentuk plumbites.
Apa itu timah?
Tin adalah elemen kimia yang mempunyai nombor atom 50 dan simbol kimia sn. Ia mempunyai penampilan keperakan putih, dan ada warna kuning yang lemah. Timah berada dalam kumpulan 14 dari jadual unsur berkala, dan oleh itu dalam kumpulan karbon. Ia adalah logam lembut yang dapat kita potong tanpa banyak daya. Walau bagaimanapun, timah menunjukkan persamaan kimia kepada kedua -dua jirannya, plumbum dan germanium.
Terdapat dua keadaan pengoksidaan utama timah; +2 dan +4 keadaan pengoksidaan. +4 keadaan sedikit lebih stabil daripada +2 keadaan pengoksidaan. Kita dapat menggambarkan timah sebagai logam yang lembut, mudah dibentuk, mulur dan logam putih yang sangat kristal. Terdapat sepuluh isotop stabil timah. Isotop yang paling banyak adalah isotop SN-120.

Rajah 02: Permukaan logam bersalut timah
Terdapat dua allotropes utama timah: alpha-tin dan beta-tin. Antaranya, beta-tin lebih stabil pada suhu bilik, dan ia juga mudah. Alfa-Tin stabil pada suhu rendah, dan ia rapuh pada suhu bilik.
Lebih penting lagi, timah tahan kakisan dari air. Walau bagaimanapun, logam ini boleh menjalani serangan oleh asid dan alkali. Oleh itu, ia boleh digilap, dan kita boleh menggunakannya sebagai kot pelindung untuk logam penting lain. Lapisan oksida pelindung yang berlaku pada logam timah dapat menghalang permukaan logam dari pengoksidaan, dan lapisan yang sama dapat membentuk pada aloi timah. Selain itu, timah boleh bertindak sebagai pemangkin dengan kehadiran oksigen dalam campuran tindak balas, dengan itu mempercepat tindak balas kimia tertentu.
Apakah perbezaan antara plumbum dan timah?
Memimpin dan timah adalah elemen logam. Simbol kimia untuk plumbum adalah pb, dan simbol kimia untuk timah adalah sn. Perbezaan utama antara plumbum dan timah ialah memimpin muncul dalam warna kelabu logam dengan warna biru manakala timah muncul sebagai logam putih keperakan dengan warna kuning yang lemah.
Di bawah infographic membandingkan sifat utama kedua -dua logam dan tabulat bersebelahan perbezaan antara plumbum dan timah.
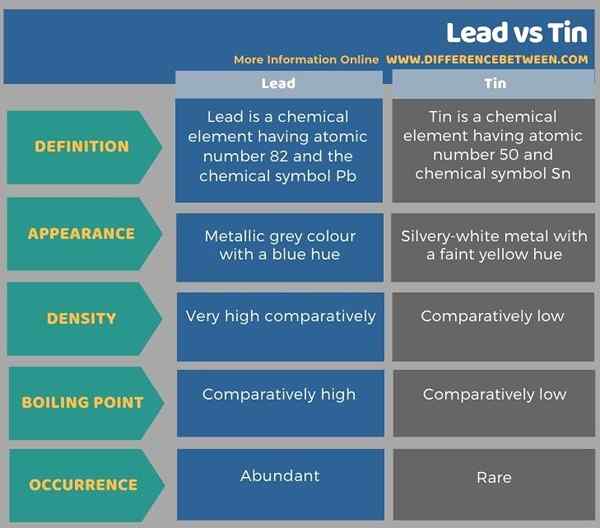
Ringkasan -Lead vs Tin
Memimpin dan timah adalah elemen logam. Perbezaan utama antara plumbum dan timah ialah memimpin muncul dalam warna kelabu logam dengan warna biru manakala timah muncul sebagai logam putih keperakan dengan warna kuning yang lemah.
Rujukan:
1. "Tin." Encyclopædia Britannica, Encyclopædia Britannica, Inc., Terdapat di sini.
Ihsan gambar:
1. "Lead Electrolytic dan 1cm3 Cube" oleh Alchemist-HP (Talk) (www.PSE-Mendelejew.DE) - Kerja Sendiri, Fal) melalui Commons Wikimedia
2. "Di dalam Timah Timah Boleh" oleh Schtone - Kerja Sendiri (Domain Awam) melalui Commons Wikimedia