Perbezaan antara interaksi ionik dan elektrostatik
The Perbezaan utama antara interaksi ionik dan elektrostatik ialah Interaksi ionik menggambarkan daya tarikan antara dua spesies ionik yang bertentangan. Sementara itu, interaksi elektrostatik menggambarkan daya tarikan antara dua spesies yang sepenuhnya atau sebahagiannya diionkan dengan caj yang bertentangan.
Interaksi ionik dan elektrostatik adalah konsep kimia yang sangat penting yang membantu dalam menentukan pembentukan molekul. Ini juga dinamakan sebagai ikatan bukan kovalen. Bentuk ikatan kimia kovalen disebabkan perkongsian elektron antara atom. Tetapi, bon bukan kovalen terbentuk kerana tarikan spesies yang dikenakan yang bertentangan dengan caj elektrik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah interaksi ionik
3. Apakah interaksi elektrostatik
4. Perbandingan sampingan - Ionic vs interaksi elektrostatik dalam bentuk jadual
5. Ringkasan
Apakah interaksi ionik?
Interaksi ionik adalah ikatan ionik di mana dua spesies ionik yang bertentangan secara elektrostatik saling menarik. Ia adalah jenis ikatan bukan kovalen. Lebih -lebih lagi, ia melibatkan spesies kimia yang sepenuhnya dikenakan (bukan sebahagian daripada spesies yang dikenakan). Ini adalah jenis utama ikatan kimia yang berlaku dalam sebatian ionik.
Ion adalah atom atau kumpulan atom yang sama ada diperoleh atau dikeluarkan elektron; ini menjadikan mereka spesies elektrik yang dikenakan. Anion dan kation adalah dua jenis ion. Anion yang terbentuk disebabkan oleh elektron yang diperoleh sementara kation dibentuk kerana mengeluarkan elektron. Oleh itu, anion dicas secara negatif kerana kehadiran elektron yang berlebihan sementara kation positif dikenakan kerana kekurangan elektron untuk meneutralkan pertuduhan proton.
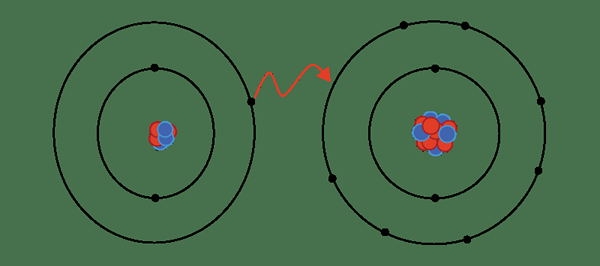
Ikatan ionik membentuk apabila elektron dikeluarkan dari atom (atau sekumpulan atom) untuk membentuk kation diperolehi oleh atom lain (atau kumpulan atom), yang membawa kepada pembentukan anion. Dalam erti kata yang paling mudah, ikatan ionik membentuk apabila elektron dikeluarkan dari logam, dan nonmetal menangkap elektron ini untuk membentuk anion.

Rajah 01: Pembentukan ikatan ionik
Walau bagaimanapun, semua ikatan ionik mempunyai beberapa tahap ciri kovalen kerana tiada atom dapat menghapuskan elektron sepenuhnya. Oleh itu, kita harus memahami bahawa istilah interaksi ionik merujuk pada masa di mana watak ionik lebih besar berbanding dengan watak kovalen.
Hampir semua sebatian ionik adalah sebatian pepejal kerana interaksi ionik cukup kuat untuk memegang anion dan kation yang terikat dengan erat. Walau bagaimanapun, sebatian ionik cair boleh menjalankan elektrik kerana ia mempunyai ion yang boleh membawa caj. Selain itu, kekuatan interaksi ionik yang tinggi membawa sebatian ionik mempunyai titik lebur yang sangat tinggi.
Apakah interaksi elektrostatik?
Interaksi elektrostatik adalah jenis daya tarikan di mana spesies lengkap atau sebahagiannya tertarik antara satu sama lain. Selanjutnya, istilah ini merangkumi kuasa menarik dan menjijikkan antara spesies ionik, i.e. ion yang dikenakan yang bertentangan antara satu sama lain sementara caj yang sama menangkis satu sama lain. Ini juga dinamakan sebagai ikatan bukan kovalen kerana daya tarikan tidak termasuk perkongsian elektron antara atom. Terdapat tiga jenis interaksi elektrostatik: interaksi ionik, ikatan hidrogen dan ikatan halogen.
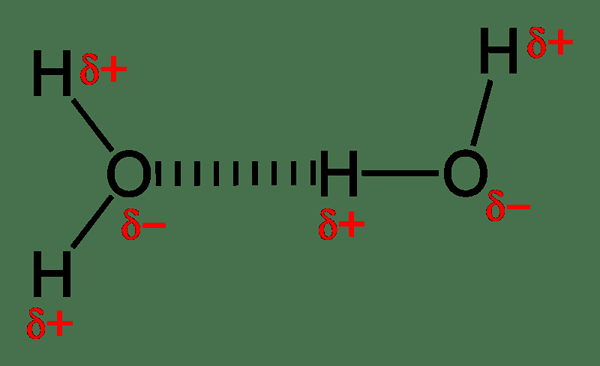
Rajah 02: Ikatan hidrogen adalah sejenis interaksi elektrostatik
Interaksi ionik termasuk daya tarikan antara spesies kimia yang terionisasi yang mempunyai caj bertentangan, e.g. Anion menarik kation. Interaksi ini menyebabkan pembentukan sebatian ionik. Daya interaksi ini sangat kuat; Oleh itu, sebatian ionik wujud dalam keadaan pepejal. Ikatan hidrogen adalah satu lagi jenis interaksi elektrostatik di mana kita dapat melihat interaksi dipole-dipole. Tarikan ini wujud antara atom hidrogen (yang sebahagiannya positif) dan atom elektronegatif yang sangat negatif (yang sebahagiannya negatif). Selain itu, ikatan halogen juga seperti ikatan hidrogen, tetapi perbezaannya adalah interaksi yang wujud antara halogen dan elektrofil.
Apakah perbezaan antara interaksi ionik dan elektrostatik?
Interaksi ionik dan interaksi elektrostatik adalah ikatan kimia bukan kovalen. Ini sangat penting dalam menerangkan pembentukan molekul yang berbeza. Perbezaan utama antara interaksi ionik dan elektrostatik adalah bahawa interaksi ionik menggambarkan daya tarikan antara dua spesies ionik yang bertentangan, sedangkan interaksi elektrostatik menggambarkan daya tarikan antara dua spesies yang sepenuhnya atau sebahagiannya dengan caj yang bertentangan.
Di bawah infographic meringkaskan perbezaan antara interaksi ionik dan elektrostatik.

Ringkasan -Interaksi Elektrostatik ionik vs
Interaksi ionik dan interaksi elektrostatik adalah ikatan kimia bukan kovalen. Ini sangat penting dalam menerangkan pembentukan molekul yang berbeza. Perbezaan utama antara interaksi ionik dan elektrostatik adalah bahawa interaksi ionik menggambarkan daya tarikan antara dua spesies ionik yang bertentangan, sedangkan interaksi elektrostatik menggambarkan daya tarikan antara dua spesies yang sepenuhnya atau sebahagiannya dengan caj yang bertentangan.
Rujukan:
1. Helmenstine, Anne Marie. "Definisi bon ionik."Thoughtco, Jan. 26, 2019, boleh didapati di sini.
2. Helmenstine, Anne Marie. "Definisi Kimia: Apakah kuasa elektrostatik?"Thoughtco, Oct. 5, 2019, boleh didapati di sini.
Ihsan gambar:
1. "Ikatan ionik" oleh Eliseetc / vektor dari ikatan ionik.PNG - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia
2. "Hydrogen-Bonding-In-Water-2D" (Domain Awam) melalui Commons Wikimedia


