Perbezaan antara tindak balas asas dan bukan asas
The Perbezaan utama antara tindak balas asas dan bukan asas ialah Reaksi asas mempunyai satu langkah, sementara reaksi bukan elementari mempunyai beberapa langkah.
Kita boleh mengklasifikasikan tindak balas kimia dengan cara yang berbeza bergantung kepada faktor yang berbeza, seperti reaktan tindak balas, produk tindak balas, pemangkin, urutan tindak balas, kadar tindak balas, dan lain -lain. Daripada jumlah ini, tindak balas asas dan bukan elementari dibahagikan berdasarkan bilangan sub-langkah reaksi kimia.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah reaksi asas
3. Apakah reaksi bukan asas
4. Perbandingan sampingan - Elementary vs reaksi bukan asas dalam bentuk jadual
5. Ringkasan
Apakah reaksi asas?
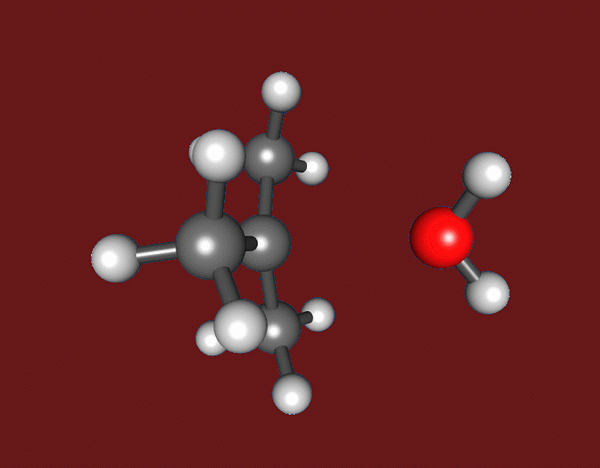
Reaksi asas adalah tindak balas kimia yang merangkumi sub-langkah tunggal. Dalam tindak balas ini, satu spesies kimia mengalami perubahan langsung untuk memberikan produk akhir dalam satu langkah. Di sini, satu keadaan peralihan diperhatikan. Secara eksperimen, jika kita tidak dapat mengesan sebarang produk perantaraan semasa tindak balas kimia, kita dapat mengkategorikan tindak balas itu sebagai reaksi asas.

Rajah 01: Reaksi asas dalam sintesis organik
Tambahan pula, terdapat beberapa jenis tindak balas asas. Mereka adalah seperti berikut:
Reaksi unimolecular
Dalam hal ini, reaktan tunggal mengalami tindak balas seperti penguraian untuk memberikan produk akhir. Contoh tindak balas yang tidak biasa termasuk isomerisasi cis-trans, pembukaan cincin, racemization, kerosakan radioaktif, dan lain-lain.
Reaksi bimolecular
Sementara itu, dalam tindak balas bimolecular, dua zarah menjalani perlanggaran untuk memberikan produk (s). Ini adalah tindak balas pesanan kedua kerana kadar tindak balas bergantung kepada kedua-dua reaktan. Contohnya termasuk tindak balas penggantian nukleofilik.
Reaksi trimolecular
Begitu juga, dalam tindak balas trimolecular, tiga zarah menjalani perlanggaran pada masa yang sama untuk memberikan produk (s). Walau bagaimanapun, jenis ini jarang berlaku kerana sukar bagi tiga reaktan untuk bertembung pada masa yang sama.
Apakah reaksi bukan asas?
Reaksi bukan elementari adalah tindak balas kimia yang merangkumi pelbagai sub-langkah. Maksudnya; Reaksi ini mempunyai beberapa langkah dan keadaan peralihan yang berbeza dengan perantaraan yang berbeza juga. Oleh itu, tindak balas ini sangat kompleks.
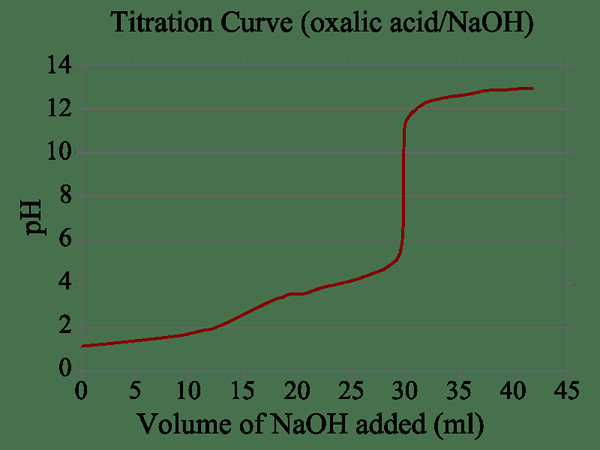
Rajah 02: Graf untuk reaksi dua langkah
Selain itu, tidak seperti dalam tindak balas asas, urutan tindak balas tidak bersetuju dengan koefisien stoikiometrik reaksi. Selain itu, susunan tindak balas ini boleh sama ada integer atau pecahan.
Apakah perbezaan antara tindak balas asas dan bukan asas?
Perbezaan antara tindak balas asas dan bukan asas bergantung kepada bilangan sub-langkah tindak balas kimia. Oleh itu, perbezaan utama antara tindak balas asas dan bukan asas ialah tindak balas asas mempunyai satu langkah sementara reaksi bukan elementari mempunyai beberapa langkah. Oleh itu, dalam tindak balas asas, terdapat satu keadaan peralihan, dan tidak ada perantara yang dapat dikesan yang dihasilkan semasa reaksi. Walau bagaimanapun, dalam tindak balas yang tidak berkepentingan, terdapat satu siri keadaan peralihan dengan pelbagai perantaraan yang dapat kami dapati dengan mudah.
Tambahan pula, tindak balas asas adalah mudah, sementara tindak balas bukan elementari adalah kompleks. Dalam tindak balas asas, urutan tindak balas sama dengan koefisien stoikiometrik tindak balas sementara, dalam tindak balas bukan elementari, urutan tindak balas mungkin atau mungkin tidak sama dengan pekali stoikiometrik reaksi.
Infographic di bawah menunjukkan lebih banyak maklumat mengenai perbezaan antara tindak balas asas dan bukan asas.
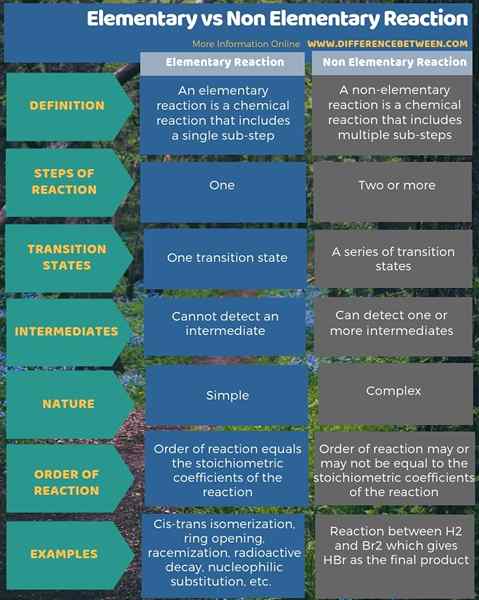
Ringkasan -REABULKAN REABLE REABLETARY ELMENTI
Ringkasnya, tindak balas asas dan bukan elementari dibahagikan berdasarkan bilangan sub-langkah reaksi kimia. Oleh itu, perbezaan utama antara tindak balas asas dan bukan elementari adalah bahawa reaksi asas mempunyai satu langkah, sementara reaksi bukan universiti mempunyai beberapa langkah.
Rujukan:
1. Helmenstine, Anne Marie. "Definisi tindak balas asas."Thoughtco, dec. 6, 2018, boleh didapati di sini.
2. DDY, Prawin. "Reaksi Asas dan Bukan Asas (NO -18) - Salinan."LinkedIn Slideshare, 29 Okt. 2015, boleh didapati di sini.
Ihsan gambar:
1. "Serangan Nukleofilik Oxonium Ion" oleh Fhenatizs - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia
2. "Grid titrasi asid oksalik" oleh mhz'as - dipindahkan dari en.Wikipedia (CC BY-SA 3.0) melalui Commons Wikimedia


