Perbezaan antara ikatan berganda dan ikatan tunggal
The Perbezaan utama antara ikatan berganda dan ikatan tunggal ialah, dalam satu pembentukan bon, Dua atom berkongsi Satu pasangan elektron hanya antara, dalam pembentukan ikatan berganda, dua atom berkongsi dua pasangan elektron.
Seperti yang dicadangkan oleh ahli kimia Amerika g.N.Lewis, atom stabil apabila mereka mengandungi lapan elektron dalam cangkang valensi mereka. Kebanyakan atom mempunyai kurang daripada lapan elektron dalam kerang valensi mereka (kecuali gas mulia dalam kumpulan 18 jadual berkala); Oleh itu, mereka tidak stabil. Atom -atom ini cenderung bertindak balas antara satu sama lain, menjadi stabil. Oleh itu, setiap atom dapat mencapai konfigurasi elektronik gas mulia. Dan, ini boleh berlaku dengan membentuk ikatan ionik, ikatan kovalen atau ikatan logam. Antaranya, ikatan kovalen adalah istimewa. Bon tunggal dan berganda berada di bawah kategori bon ini.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu ikatan berganda
3. Apa itu ikatan tunggal
4. Perbandingan sampingan - ikatan berganda vs ikatan tunggal dalam bentuk jadual
5. Ringkasan
Apa itu ikatan berganda?
Bentuk ikatan berganda apabila dua atom berkongsi dua pasang elektron di antara mereka untuk mengisi orbital valensi. Ikatan berganda lebih pendek daripada bon tunggal tetapi lebih kuat daripada mereka. Sp2 Hibridisasi membolehkan atom membentuk ikatan berganda.
Bon berganda boleh terdiri daripada dua jenis. Daripada kedua -dua bon, satu adalah ikatan sigma. Ia terbentuk melalui linear bertindih dari dua SP2 orbital hibrid. Kedua, ikatan lain (yang kita namakan sebagai ikatan Pi) membentuk melalui tumpang tindih sisi dua orbital p.
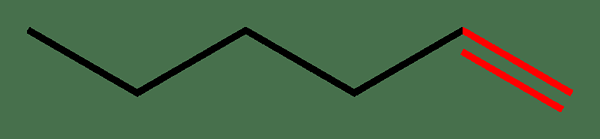
Rajah 01: ikatan berganda dalam warna merah
Contoh umum molekul dengan ikatan berganda adalah etilena. Dalam etilena, ikatan berganda antara dua atom karbon. Walau bagaimanapun, selain daripada atom yang sama, jenis ikatan ini boleh membentuk antara atom yang berbeza seperti dalam contoh karbon karbonil (c = o), imines (c = n), sebatian azo (n = n) dan lain -lain.
Apa itu ikatan tunggal?
Bentuk ikatan tunggal apabila dua atom dengan perbezaan elektronegativiti yang sama atau rendah berkongsi satu pasangan elektron. Kedua -dua atom ini boleh menjadi jenis yang sama atau pelbagai jenis. Contohnya, apabila jenis atom yang sama bergabung untuk membentuk molekul seperti CL2, H2, atau p4, Setiap atom mengikat dengan yang lain dengan satu ikatan kovalen.
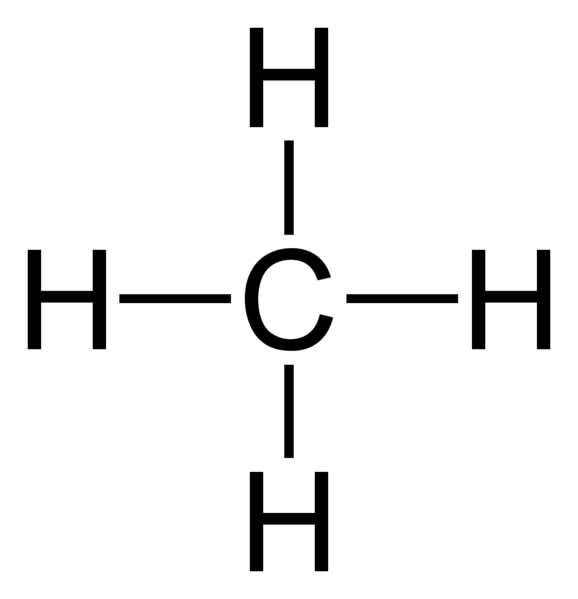
Molekul metana (CH4) mempunyai ikatan kovalen tunggal antara dua jenis elemen (atom karbon dan hidrogen). Selanjutnya, metana adalah contoh untuk molekul yang mempunyai ikatan kovalen antara atom dengan perbezaan elektronegativiti yang sangat rendah.

Rajah 02: Struktur molekul metana
Kami namakan bon kovalen tunggal juga sebagai ikatan sigma. Satu ikatan memberi molekul keupayaan untuk menjalani putaran di sekitar ikatan itu mengenai satu sama lain. Oleh itu, putaran ini membenarkan molekul mempunyai struktur konformasi yang berbeza. Juga, jenis bon ini terbentuk dengan SP3 atom hibrida molekul. Apabila dua SP sama3 molekul hibrida bertindih secara linear, satu bentuk ikatan tunggal.
Apakah perbezaan antara ikatan berganda dan ikatan tunggal?
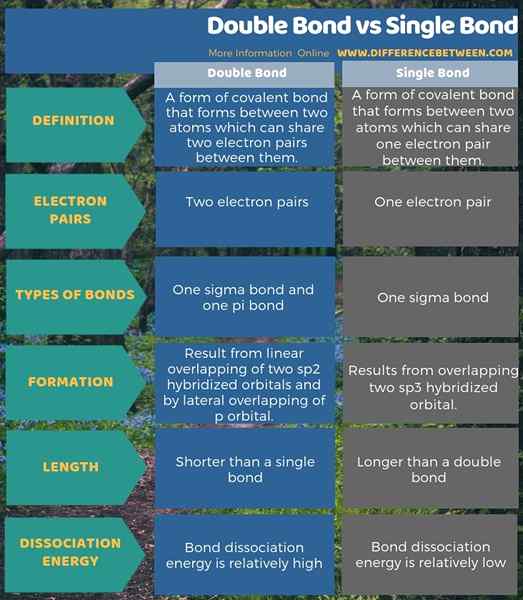
Bon kovalen adalah terutamanya daripada tiga jenis; bon tunggal, ikatan berganda, dan ikatan tiga. Perbezaan utama antara ikatan berganda dan ikatan tunggal ialah, dalam satu pembentukan ikatan tunggal, hanya satu pasangan elektron dikongsi antara dua atom manakala, dalam pembentukan ikatan berganda, dua pasangan elektron dikongsi.
Selain itu, perbezaan penting antara ikatan berganda dan ikatan tunggal ialah hasil ikatan tunggal dari tumpang tindih dua orbital hibrida SP3 manakala ikatan ganda hasil daripada tumpang tindih linear dua orbital hibrida SP2 dan oleh lateral p orbital.
Selain itu, satu ikatan mengandungi satu ikatan sigma, sedangkan ikatan berganda mengandungi satu ikatan sigma dan satu ikatan pi. Oleh itu, ini mempengaruhi panjang ikatan antara atom. Oleh itu, membawa kepada perbezaan lain antara ikatan berganda dan ikatan tunggal. Itu dia; Panjang ikatan tunggal lebih tinggi daripada ikatan berganda. Selanjutnya, tenaga pemisahan ikatan berganda agak lebih tinggi daripada tenaga pemisahan bon tunggal.
Ringkasan -ikatan berganda vs ikatan tunggal
Ikatan berganda dan bon tunggal adalah jenis ikatan kimia kovalen. Perbezaan utama antara ikatan berganda dan ikatan tunggal ialah, dalam satu pembentukan ikatan tunggal, hanya satu pasangan elektron dikongsi antara dua atom manakala, dalam pembentukan ikatan berganda, dua pasangan elektron dikongsi.
Rujukan:
1. Helmenstine, Anne Marie, PH.D. "Definisi dan contoh ikatan berganda dalam kimia."Thoughtco, dec. 5, 2018. Terdapat di sini
Ihsan gambar:
1."Skeletal-Formula-Terminal-Double-Bond" (Domain Awam) melalui Commons Wikimedia
2."Methane-2d-square" (Domain Awam) melalui Commons Wikimedia


