Perbezaan antara teori atom Dalton dan teori atom moden
Perbezaan utama - Teori Atom Dalton vs Teori Atom Moden
Teori Atom Dalton adalah teori tertua mengenai atom. Pada tahun 1808, John Dalton menerbitkan teorinya, yang terdiri daripada beberapa postulat yang dibina berdasarkan eksperimen dan undang -undang gabungan kimianya. Sejumlah saintis kemudian menyumbang kepada perkembangan teori atom moden, yang berbeza dengan teori atom Dalton dan mempunyai fakta yang lebih maju mengenai atom dan kelakuannya. Perbezaan utama antara teori atom Dalton dan teori atom moden ialah Struktur dan sifat atom menurut teori Dalton berbeza dari struktur dan sifat yang dicadangkan oleh teori atom moden.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah teori atom Dalton
3. Apakah teori atom moden
4. Perbandingan sampingan - teori atom Dalton vs teori atom moden dalam bentuk jadual
5. Ringkasan
Apakah teori atom Dalton?
Teori Atom Dalton adalah satu set postulates yang dicadangkan untuk menggambarkan struktur dan sifat atom. Perkembangan teori atom pertama ini dipengaruhi oleh fakta seperti pembubaran gas yang berlainan dalam air dalam perkadaran yang berbeza, komposisi oksida timah dengan 88% timah manakala selebihnya menjadi oksigen, dan lain -lain. Kemudian Dalton mencadangkan postulat berikut.
- Semua perkara diperbuat daripada atom yang tidak dapat dipisahkan.
- Atom satu elemen sama antara satu sama lain dalam jisim, saiz, dan bentuknya.
- Atom boleh menggabungkan antara satu sama lain dalam jumlah kecil.
- Atom tidak boleh dibuat atau dimusnahkan.
- Atom adalah unit perkara terkecil yang boleh mengambil bahagian dalam tindak balas kimia.
Postulat ini di atas tidak menjelaskan struktur atau sifat atom secara terperinci.
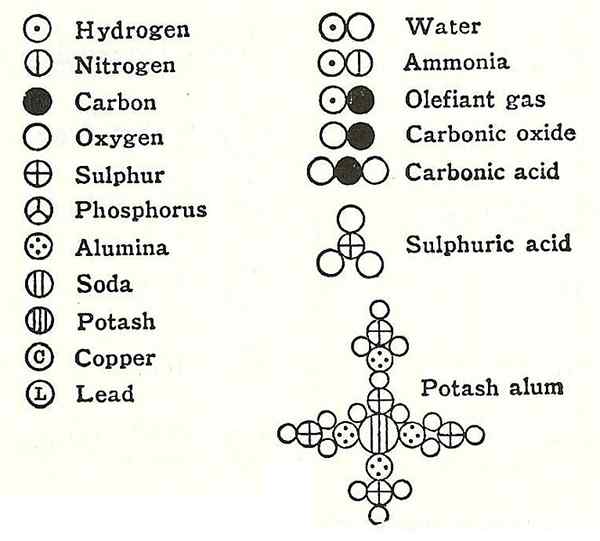
Rajah 01: Beberapa atom dan molekul dengan struktur mereka mengikut teori atom Dalton.
Apakah teori atom moden?
Oleh kerana terdapat banyak kecacatan dalam teori atom Dalton, saintis mula menjalankan lebih banyak eksperimen untuk menjelaskan struktur yang tepat dan sifat -sifat atom. Ini membawa kepada perkembangan teori atom moden. Teori atom moden menunjukkan kecacatan teori atom Dalton. Kecacatan ini boleh dinyatakan seperti di bawah.
- Atom tidak dapat dipisahkan; mereka terdiri daripada zarah subatomik.
- Boleh ada atom elemen yang sama yang tidak sama. Ini dipanggil isotop.
- Atom tidak selalu digabungkan dalam jumlah kecil. Dalam polimer, sebilangan besar atom digabungkan untuk menghasilkan molekul.
- Atom boleh dimusnahkan oleh pembelahan (contohnya: bom atom).
- Kadang -kadang, zarah subatomik berlaku dalam tindak balas tertentu. (Cth: Decay Radioaktif)
Selain itu, teori atom moden menerangkan lebih banyak maklumat mengenai atom dan kelakuannya. Beberapa butiran ini disenaraikan di bawah.
- Atom terdiri daripada zarah subatomik seperti elektron, proton dan neutron.
- Proton dan neutron bersama -sama membentuk teras atom di mana elektron ditemui di orbital di sekitar nukleus, yang kelihatan seperti awan.
- Orbital yang diduduki oleh elektron adalah tahap tenaga yang menunjukkan tenaga elektron tertentu.
- Tahap tenaga ini terdiri daripada tahap sub-tenaga.
- Ciri asas bahawa semua atom bahagian elemen yang sama adalah bilangan proton. Atom dari elemen yang sama boleh mempunyai bilangan elektron yang berbeza yang dipanggil ion dan bilangan neutron yang berbeza yang dipanggil isotop.
- Sebatian boleh dibuat daripada elemen yang sama atau unsur yang berbeza.
- Apabila semua elemen dianggap bersama, atom mereka mempunyai sifat yang berbeza secara berkala.

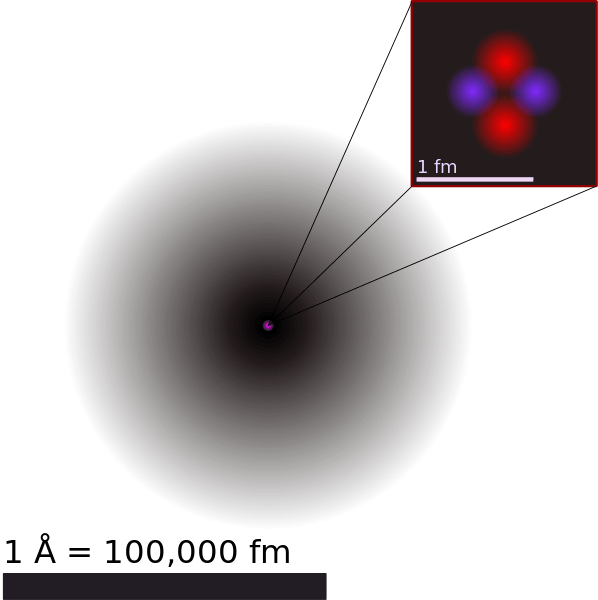
Rajah 02: Struktur atom helium mengikut teori atom moden.
Apakah perbezaan antara teori atom Dalton dan teori atom moden?
Teori Atom Dalton vs Teori Atom Moden | |
| Teori atom Dalton adalah teori tentang zarah -zarah yang tidak dapat dipisahkan yang dipanggil atom yang merupakan zarah terkecil dari semua perkara. | Teori atom moden adalah teori yang menerangkan struktur terperinci sepenuhnya atom. |
| Struktur atom | |
| Menurut teori atom Dalton, atom adalah zarah yang tidak dapat dipisahkan. | Teori atom moden mengatakan bahawa atom terdiri daripada zarah subatomik; proton, elektron, dan neutron. |
| Isotop | |
| Teori Dalton tidak menerangkan butiran mengenai isotop. Ia menyatakan bahawa semua atom elemen yang sama adalah sama. | Teori atom moden menerangkan butiran tentang isotop yang mempunyai bilangan neutron yang berbeza dan bilangan proton yang sama. |
| Elektron | |
| Dalton tidak dapat memberi butiran mengenai elektron. | Teori atom moden menerangkan lokasi, reaksi, dan tingkah laku elektron. |
| Tindak balas kimia | |
| Teori atom Dalton menjelaskan bahawa atom adalah zarah terkecil yang dapat terlibat dalam reaksi. | Teori atom moden menyatakan bahawa zarah subatomik boleh mengambil bahagian dalam reaksi. |
Ringkasan -Teori Atom Dalton vs Teori Atom Moden
Walaupun tidak ada makmal yang dilengkapi dengan baik, Dalton dapat membina teori mengenai atom, yang tidak dapat dilihat oleh mata. Ini membawa kepada perkembangan teori atom moden, yang dapat menjelaskan hampir segala -galanya mengenai struktur dan sifat atom. Terdapat perbezaan yang besar antara teori atom Dalton dan teori atom moden kerana struktur dan sifat atom menurut teori Dalton berbeza dari struktur dan sifat yang dicadangkan oleh teori atom moden.
Muat turun versi pdf teori atom Dalton vs teori atom moden
Anda boleh memuat turun versi PDF artikel ini dan menggunakannya untuk tujuan luar talian mengikut nota petikan. Sila muat turun versi pdf di sini perbezaan antara teori atom Dalton dan teori atom moden.
Rujukan:
1.Gillaspy, Rebecca. "Teori Atom Moden: Awan Elektron, Schrodinger & Heisenberg."Kajian.com. N.p., n.d. Web. Terdapat di sini.07 Jun 2017.
2.Shrestha, Binod. "Postulates of Daltons Teori Atom."Kimia Libreetexts. N.p., 21 Mac. 2017. Web. Terdapat di sini. 07 Jun 2017.
Ihsan gambar:
1."Zarah Daltons" oleh John Dalton; Diterbitkan dalam Sistem Falsafah Kimia Baru (Domain Awam) melalui Commons Wikimedia
2. "Helium Atom QM" oleh Pengguna: YZMO - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia


