Perbezaan antara unsur blok D dan elemen peralihan
Perbezaan Utama -Elemen Blok D vs Elemen Peralihan
Perbezaan antara unsur-unsur d-blok dan elemen peralihan agak mengelirukan. Kedua-dua perkataan digunakan secara bergantian, dan ramai orang menggunakan perkataan 'elemen peralihan' untuk elemen d-blok. The Perbezaan utama antara unsur-unsur d-blok dan elemen peralihan adalah ketika itu Semua elemen peralihan adalah elemen d-blok, Tidak semua elemen blok D adalah elemen peralihan. Jelas bahawa unsur-unsur d-blok mempunyai d-elektron dalam shell d-sub. Unsur -unsur peralihan adalah unsur -unsur yang membentuk ion stabil yang tidak lengkap diisi d-orbital. Sebagai contoh, zink dan scandium adalah unsur-unsur d-blok; Tetapi bukan elemen peralihan.
Apakah Unsur-unsur d-blok?

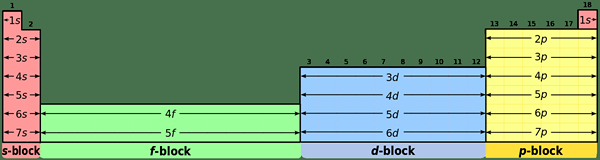
Unsur-unsur d-blok dapat dikenal pasti dengan jelas menggunakan konfigurasi elektron dan kedudukan jadual berkala. Ciri utama elemen blok D adalah sekurang-kurangnya satu elektron di d-sub shell. Perkara ganjil berlaku apabila pengisian elektron mengikut Aufbau prinsip dalam elemen d-blok adalah, 4s-elektron pertama kali diisi sebelum ini 3d-elektron; yang bermaksud 3D-elctrons mempunyai tenaga yang lebih tinggi daripada 4s-elektron. Tetapi, apabila mereka mengeluarkan elektron untuk membentuk ion; 4s-elektron mula -mula dikeluarkan dari atom.
| Elemen | Konfigurasi elektron | |
| Scandium | Sc | [AR] 3D14s2 |
| Titanium | Ti | [AR] 3D24s2 |
| Vanadium | V | [AR] 3D34s2 |
| Chromium | Cr | [AR] 3D54s1 |
| Mangan | Mn | [AR] 3D54s2 |
| Ferrous | Fe | [AR] 3D64s2 |
| Cobalt | Co | [AR] 3D74s2 |
| Nikel | Ni | [AR] 3D84s2 |
| Tembaga | Cu | [AR] 3D104s1 |
| Zink | Zn | [AR] 3D104s2 |
Catatan:[AR] = 1s22s22p63s23p6

Apakah elemen peralihan?
Unsur-unsur peralihan adalah unsur-unsur yang membentuk ion yang stabil dengan orbital D yang tidak lengkap.Apabila ion dibentuk oleh unsur-unsur d-blok; mereka mula -mula menghapuskan s-elektron (n-level) dan kemudian keluarkan d-elektron (tahap n-1). Zink dan Scandium adalah dua elemen khas dalam blok D; mereka tidak membentuk ion yang tidak lengkap diisi d-orbital; oleh itu mereka tidak dianggap sebagai elemen peralihan. Semua elemen lain dalam bentuk D-kumpulan yang stabil ion yang tidak lengkap diisi d-elektron.

Penyelesaian logam peralihan
Apakah perbezaan antara unsur-unsur d-blok dan elemen peralihan?
Definisi unsur-unsur d-blok dan elemen peralihan
D-blok elemen: Unsur -unsur yang mempunyai satu atau lebih d-elektron dalam d-Sub shell dikenali sebagai elemen d-blok. Sebilangan besar elemen blok adalah logam.
Unsur Peralihan: Unsur -unsur yang dapat membentuk ion yang stabil dengan penuh diisi d-Orbital dipanggil elemen peralihan.
Catatan:
Zn dan SC bukan elemen peralihan. Mereka tidak membentuk hanya zn2+dan sc3+ ion, yang tidak mengandungi d-orbital yang tidak terisi.
Zn2+ = 1s22s22p63s23p63d10
Sc3+= 1s22s22p63s23p63d10
Ion berikut mengandungi d-orbital yang tidak terisi.Oleh itu, unsur -unsur ini dianggap sebagai elemen peralihan.
Cu2+ = 1s22s22p63s23p63d9
Ni4+= 1s22s22p63s23p63d6
Mn2+= 1s22s22p63s23p63d5
Fe2+= 1s22s22p63s23p63d6
Keadaan pengoksidaan:
D-blok elemen: Beberapa elemen blok D menunjukkan pelbagai keadaan pengoksidaan dan beberapa daripadanya menunjukkan keadaan pengoksidaan tunggal.
Contoh:
Zink hanya menunjukkan +2 keadaan pengoksidaan dan scandium hanya menunjukkan +3 keadaan pengoksidaan.
Unsur-unsur lain dalam blok D menunjukkan pelbagai keadaan pengoksidaan.
Unsur Peralihan: Unsur Peralihan Menunjukkan Pelbagai Kepercayaan Pengoksidaan. Sekurang -kurangnya satu negeri mengandungi tidak terisi d-orbital.
Contoh:
Titanium +2, +4
Vanadium +2, +3, +4, +5
Kromium +2, +3, +6
Mangan +2, +3, +4, +6, +7
Ferrous +2, +3
Kobalt +2, +3
Nikel +2, +4
Tembaga +1, +2
Ihsan gambar:
1. "Blok jadual berkala SPDF (32 lajur)" oleh Pengguna: DEPIEP [CC BY-SA 3.0] melalui Commons
2. "Coloured-Transition-Metal-Solutions" [domain awam] melalui Commons


