Apakah perbezaan antara thymolphthalein dan phenolphthalein

The Perbezaan utama antara thymolphthalein dan phenolphthalein adalah bahawa perubahan warna thymolphthalein berlaku dari warna tanpa warna, sedangkan perubahan warna phenolphthalein berlaku dari warna tanpa warna ke warna merah jambu apabila mengubah keadaan tindak balas dari berasid ke asas.
Thymolphthalein dan phenolphthalein adalah dua petunjuk pH yang berbeza yang sangat berguna dalam proses analisis titrimetrik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu thymolphthalein
3. Apa itu phenolphthalein
4. Thymolphthalein vs phenolphthalein dalam bentuk jadual
5. Ringkasan -thymolphthalein vs phenolphthalein
Apa itu thymolphthalein?
Thymolphthalein adalah sejenis pewarna phthalein yang berguna sebagai penunjuk asid. Formula kimia thymolphthalein ialah C28H30O4. Ia adalah penunjuk pH yang memberikan perubahan warna pada perubahan pH campuran tindak balas. Julat pH peralihan penunjuk ini adalah sekitar 9.3 - 10.5. Thymolphthalein tidak berwarna di bawah pH 9.3, sedangkan ia muncul dalam warna biru pada nilai pH di atas 10.5. Selain itu, pekali kepupusan molar thymolphthalein adalah 38 000 m-1cm-1 pada 595 nm untuk anion penunjuk warna biru.
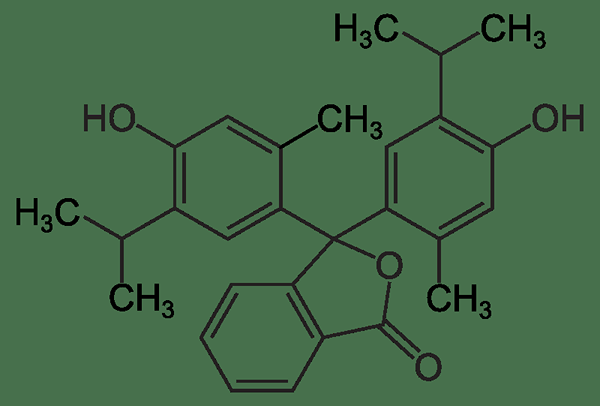
Rajah 01: Struktur kimia penunjuk thymolphthalein
Sintesis thymolphthalein boleh dilakukan menggunakan thymol dan anhydride phthalic. Produk tindak balas sintesis ini adalah serbuk putih yang juga merupakan bentuk thymolphthalein yang tersedia secara komersil. Pada suhu tinggi, bahan ini cenderung untuk mengurai. Selain itu, bahan ini digunakan sebagai julap dan untuk menghilangkan dakwat juga.
Apa itu phenolphthalein?
Phenolphthalein adalah penunjuk pH yang berguna sebagai penunjuk titrasi asid. Ini adalah petunjuk yang sangat biasa yang sering kita gunakan dalam proses titrasi makmal kami. Formula kimia bahan ini ialah C20H14O4. Kita boleh menulis istilah ini hanya sebagai "hin" atau sebagai "phph". Warna phenolphthalein berasid tidak berwarna, sementara warna asas phenolphthalein berwarna merah jambu. Julat pH untuk perubahan warna ini berlaku adalah sekitar 8.3 - 10.0 Ph.
Selain itu, penunjuk phenolphthalein sedikit larut air, dan selalunya, ia larut dalam alkohol. Dengan cara ini, kita dapat dengan mudah menggunakannya dalam titrasi. Phenolphthalein adalah asid lemah yang dapat melepaskan proton ke penyelesaian. Bentuk phenolphthalein berasid adalah nonionik, dan tidak berwarna. Bentuk fenolphthalein yang berwarna merah jambu berwarna merah jambu, dan ia adalah bentuk ionik. Jika kita menambah asas kepada campuran tindak balas yang terdiri daripada penunjuk phenolphthalein, keseimbangan antara bentuk ionik dan nonionik cenderung beralih ke arah keadaan deprotonasi kerana proton dikeluarkan dari larutan.

Rajah 02: Warna asas phenolphthalein
Mengenai sintesis penunjuk phenolphthalein, kita dapat menghasilkannya dari pemeluwapan anhydride phthalic dengan kehadiran dua setara fenol di bawah keadaan berasid. Selain itu, tindak balas ini boleh dikatalisis menggunakan campuran zink klorida dan thionyl chloride.
Apakah perbezaan antara thymolphthalein dan phenolphthalein?
Thymolphthalein dan phenolphthalein adalah dua petunjuk pH yang berbeza yang sangat berguna dalam proses analisis titrimetrik. Perbezaan utama antara thymolphthalein dan phenolphthalein adalah bahawa perubahan warna thymolphthalein berlaku dari warna tanpa warna, sedangkan perubahan warna phenolphthalein berlaku dari warna tanpa warna ke warna merah jambu apabila mengubah keadaan reaksi dari asid ke asas. Selain itu, julat pH aktif thymolphthalein adalah 9.3 hingga 10.5 manakala julat pH aktif phenolphthalein adalah 8.3 hingga 10.0.
Infographic di bawah membentangkan perbezaan antara thymolphthalein dan phenolphthalein dalam bentuk tabular untuk perbandingan sampingan.
Ringkasan -thymolphthalein vs phenolphthalein
Thymolphthalein dan phenolphthalein adalah dua petunjuk pH yang berbeza yang sangat berguna dalam proses analisis titrimetrik. Perbezaan utama antara thymolphthalein dan phenolphthalein adalah bahawa perubahan warna thymolphthalein berlaku dari warna tanpa warna, sedangkan perubahan warna phenolphthalein berlaku dari warna tanpa warna ke warna merah jambu apabila mengubah keadaan reaksi dari asid ke asas.
Rujukan:
1. "Phenolphthalein." Pusat Kebangsaan Maklumat Bioteknologi. Pangkalan Data Kompaun Pubchem, U.S. Perpustakaan Perubatan Negara.
Ihsan gambar:
1. "Phenolphthalein-at-ph-9" oleh Ben Mills-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia
2. "Thymolphthalein" oleh Neurotiker - Kerja Sendiri (Domain Awam) melalui Commons Wikimedia


