Apakah perbezaan antara orbital hibrid dan tidak terhidrid
The Perbezaan utama antara orbital hibrid dan tidak terhidrid Adakah orbital hibrida adalah hibrid atau campuran orbital atom, sedangkan orbital yang tidak dihidridkan adalah orbital atom biasa yang tidak dicampur dengan orbital atom lain.
Pemahaman orbital hibrid dan tidak terhidridasi sangat penting dalam mengkaji dan meramalkan struktur kimia sebatian kimia. Orbital hibrida adalah gabungan orbital yang tidak terhidrida.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah hibridisasi orbital
3. Apakah orbital hibrid
4. Apakah orbital yang tidak disengaja
5. Hibridasi vs orbital yang tidak dihidridkan dalam bentuk jadual
6. Ringkasan - hibridasi vs orbital yang tidak dihidangkan
Apakah hibridisasi orbital?
Hibridisasi orbital adalah konsep yang sangat penting dalam kimia. Ini adalah konsep mencampurkan orbital atom dan membentuk orbital hibrid baru yang sesuai untuk pasangan elektron dalam pembentukan ikatan kimia mengikut teori ikatan valensi. Sebagai contoh, atom karbon yang boleh membentuk empat ikatan tunggal mengandungi empat elektron shell valensi dalam empat orbital hibrid yang terbentuk dari hibridisasi satu orbital atom "s" dengan tiga orbital atom p.
Orbital atom adalah representasi model tingkah laku elektron dalam molekul. Hibridisasi mudah adalah penghampiran yang dibuat berdasarkan orbital atom yang serupa dengan yang diperolehi untuk atom hidrogen. Ia adalah satu -satunya atom yang dapat kita selesaikan persamaan Schrodinger. Apabila mempertimbangkan atom berat seperti karbon dan nitrogen, orbital atom menggunakan orbital atom 2s dan 2p yang serupa dengan orbital keadaan teruja untuk hidrogen.
Apakah orbital hibrid?
Orbital hibrida bercampur atau gabungan orbital atom yang terlibat dalam ikatan kimia. Mereka bercampur orbital atom hibrid yang berguna dalam penjelasan geometri molekul dan sifat ikatan atom. Ini dilupuskan secara simetri di ruang angkasa. Biasanya, orbital hibridisasi terbentuk dari pencampuran orbital atom dari tenaga setanding.
Orbital hibrid boleh dianggap sebagai campuran orbital atom. Ini disimpulkan antara satu sama lain dalam pelbagai perkadaran. Sebagai contoh, dalam metana, terdapat ikatan karbon hidrogen di mana orbital hibrid atom karbon mempunyai watak 25% dan 75% p watak. Oleh itu, ia digambarkan sebagai orbital hibrid SP3. Terdapat pelbagai jenis hibridisasi, termasuk SP, SP2, dan SP3.

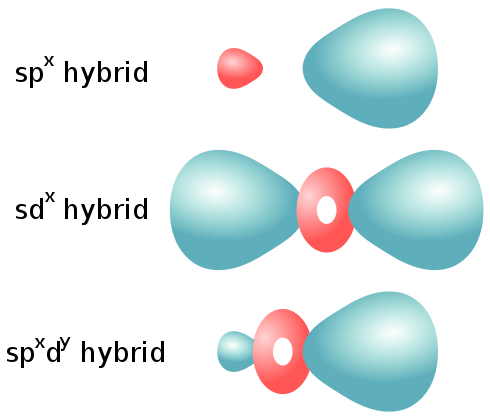
Orbitals SP terbentuk dari hibridisasi satu s dan satu or atom orbital. Jenis orbital hibrid ini boleh didapati dalam alkynes yang mempunyai ikatan tiga. Gabungan ini menghasilkan dua orbital hibrida SP dan dua orbital atom P yang tinggal.
Umumnya, hibridisasi membantu dalam menerangkan bentuk molekul. Ini kerana sudut antara bon hampir sama dengan sudut antara orbital hibrid.
Apakah orbital yang tidak disengaja?
Orbital yang tidak dihidangkan adalah orbital atom biasa yang tidak dicampur dengan orbital atom lain. Orbital atom P yang tidak diselimuti digunakan dalam pembentukan ikatan π. Biasanya, dua orbital atom P yang tidak dihidangkan dari atom yang berbeza boleh bertindih ke sisi, mengakibatkan pasangan elektron bersama yang menduduki ruang di atas dan di bawah garis yang bergabung dengan atom.
Semua orbital yang tidak terhidridasi berada dalam keadaan tanah atom. Penggunaan utama orbital jenis ini adalah pembentukan ikatan berganda dan tiga. Contohnya, dalam hibridisasi SP3, terdapat 4 orbital atom hibrida SP3 dan tidak ada orbital yang tidak dihidangkan. Oleh itu, jenis hibridisasi dalam atom ini boleh membentuk ikatan 4-sigma. Tetapi dalam hibridisasi SP2 dan SP, terdapat satu dan dua orbital P yang tidak diselaraskan yang tersisa dalam atom hibrida, masing -masing. Orbital atom P yang tidak diselimuti ini terlibat dalam pembentukan ikatan tiga dan berganda.
Apakah perbezaan antara orbital hibrid dan tidak terhidrid?
Perbezaan utama antara orbital hibrid dan tidak dihidridkan ialah orbital hibrida adalah hibrid atau campuran orbital atom, sedangkan orbital yang tidak diselaraskan adalah orbital atom biasa yang tidak bercampur dengan orbital atom lain. Walaupun orbital hibrida membentuk ikatan sigma, orbital yang tidak terhidrida membentuk ikatan PI.
Infographic di bawah membentangkan perbezaan antara orbital hibrid dan tidak terhidrid dalam bentuk tabular untuk perbandingan bersebelahan.
Ringkasan -hibridasi vs orbital yang tidak dihidangkan
Perbezaan utama antara orbital hibrid dan tidak dihidridkan ialah orbital hibrida adalah hibrid atau campuran orbital atom, sedangkan orbital yang tidak diselaraskan adalah orbital atom biasa yang tidak bercampur dengan orbital atom lain.
Rujukan:
1. "Orbital hibrid." Kimia Libreetexts, Libretexts, 26 Ogos. 2022.
Ihsan gambar:
1. "Bentuk Orbital Hibrid" oleh Pegawai781 - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia


