Perbezaan antara toluena dan xilena
The Perbezaan utama antara toluena dan xilena adalah bahawa Toluena mengandungi satu kumpulan metil yang dilekatkan pada cincin benzena manakala xilena mengandungi dua kumpulan metil yang dilampirkan pada cincin benzena.
Kedua -dua toluena dan xilena adalah sebatian organik yang penting yang mempunyai struktur kimia yang hampir sama. Kedua -duanya adalah sebatian aromatik yang mengandungi cincin benzena dan kumpulan metil yang dilampirkan.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu toluena
3. Apa itu xylene
4. Perbandingan sampingan - toluene vs xylene dalam bentuk jadual
5. Ringkasan
Apa itu toluena?
Toluena adalah sebatian organik yang mempunyai formula kimia c7H8. Nama IUPAC untuk toluena adalah metilbenzena. Ia mengandungi cincin benzena yang dilampirkan pada kumpulan metil. Jisim molar sebatian ini adalah kira -kira 92.14 g/mol. Pada suhu dan tekanan bilik, ia kelihatan sebagai cecair tanpa warna yang mempunyai bau seperti benzena yang pedas.
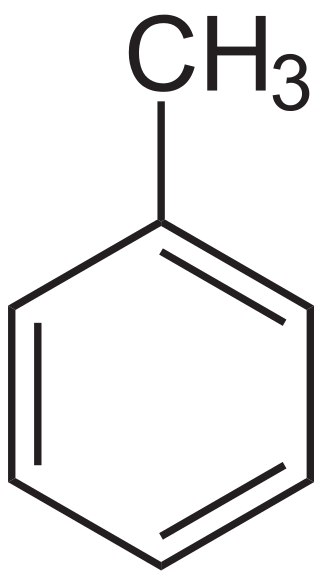
Rajah 01: Struktur kimia toluena
Titik toluena mendidih kira -kira 111 ° C. Ia adalah sebatian cecair yang sangat mudah terbakar. Ia dianggap sebagai terbitan benzena. Ia dapat menjalani tindak balas penggantian aromatik elektrofilik. Toluena sangat reaktif kerana kehadiran kumpulan metil. Kumpulan metil adalah kumpulan melepaskan elektron yang baik. Oleh itu, kumpulan metil yang terdapat dalam molekul toluena membantu menjadikan cincin benzena lebih kaya elektron. Oleh itu, ia dapat dengan mudah berkongsi elektron dengan elektrofil.
Toluena sangat berguna dalam tindak balas organik. Ia boleh digunakan sebagai bahan permulaan untuk menghasilkan benzena. Ia memberikan molekul benzena bersama dengan metana (CH4) molekul sebagai produk akhir. Toluena adalah pelarut yang baik yang biasa digunakan dalam pengeluaran cat. Kadang -kadang digunakan sebagai bahan bakar kerana mudah terbakarnya. Walau bagaimanapun, toluena dianggap sebagai sebatian toksik.
Apa itu xylene?
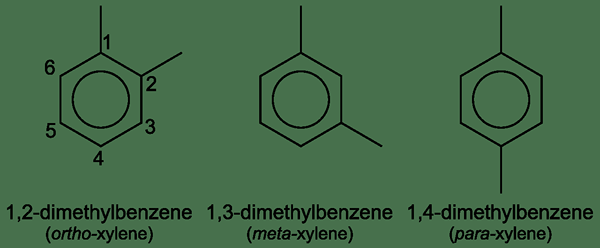
Xylene adalah sebatian organik yang mempunyai formula kimia (CH3)2C6H4. Ia berada di bawah kategori dimethylbenzene kerana ia mempunyai benzena dengan dua kumpulan metil yang dilampirkan. Selain itu, sebatian ini mempunyai tiga isomer yang kedudukannya kumpulan metil pada cincin benzena berbeza antara satu sama lain. Kesemua tiga isomer ini berlaku sebagai cecair yang tidak berwarna dan mudah terbakar; Lebih tepat lagi, campuran isomer ini dipanggil "xylenes".

Rajah 02: Struktur xilena
Pengeluaran xilena boleh dilakukan dengan pembaharuan pemangkin semasa penapisan petroleum atau oleh pengkanan arang batu semasa pembuatan bahan bakar kokas. Walau bagaimanapun, kaedah pengeluaran xilena yang kami gunakan adalah metilasi toluena dan benzena.
Xylene penting sebagai pelarut nonpolar. Walau bagaimanapun, ia mahal dan agak beracun. Sifat nonpolar adalah disebabkan oleh perbezaan rendah elektronegativiti antara c dan h. Oleh itu, xilena cenderung membubarkan bahan lipofilik dengan baik.
Menurut tempat di mana dua kumpulan metil dilampirkan pada cincin benzena, terdapat tiga jenis xilena sebagai o-xilena, p-xilena dan m-xilena. Ketiga istilah ini berdiri untuk kedudukan ortho, para dan meta dari dua kumpulan metil.
Apakah perbezaan antara toluena dan xilena?
Toluena dan xilena adalah sebatian organik aromatik. Perbezaan utama antara toluena dan xilena ialah toluena mengandungi satu kumpulan metil yang dilekatkan pada cincin benzena manakala xilena mengandungi dua kumpulan metil yang dilampirkan pada cincin benzena.
Jadual berikut menunjukkan lebih banyak komprison yang berkaitan dengan perbezaan antara toluena dan xilena.
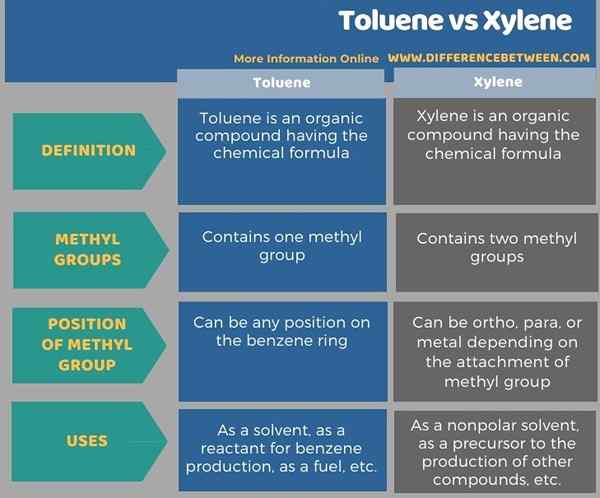
Ringkasan -toluene vs xylene
Toluena dan xilena adalah sebatian organik aromatik. Perbezaan utama antara toluena dan xilena ialah toluena mengandungi satu kumpulan metil yang dilekatkan pada cincin benzena manakala xilena mengandungi dua kumpulan metil yang dilampirkan pada cincin benzena.
Rujukan:
1. "Toluene." Wikipedia, Yayasan Wikimedia, 4 Mei 2020, boleh didapati di sini.
Ihsan gambar:
1. "Toluol" oleh Neurotiker - Kerja Sendiri (Domain Awam) melalui Commons Wikimedia
2. "IUPAC-CYCLIC" oleh Fvasconcellos 20:19, 8 Januari 2008 (UTC). Imej Asal oleh DrBob (Talk · Contribs). - Versi Vektor Imej: IUPAC-CYCLIC.PNG oleh DrBob (Talk · Contribs) (CC BY-SA 3.0) melalui Commons Wikimedia


