Perbezaan antara kestabilan termodinamik dan kinetik
The Perbezaan utama antara kestabilan termodinamik dan kinetik ialah Kestabilan termodinamik merujuk kepada status produk, sedangkan kestabilan kinetik merujuk kepada status reaktan.
Kestabilan termodinamik dan kinetik adalah dua istilah kimia penting yang menerangkan sistem dengan tindak balas kimia. Kestabilan termodinamik adalah kestabilan keadaan tenaga terendah sistem sementara kestabilan kinetik adalah kestabilan keadaan tenaga tertinggi sistem. Selain itu, keadaan termodinamik menerangkan keadaan keseimbangan sistem, sedangkan keadaan kinetik menggambarkan kereaktifan sistem.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah kestabilan termodinamik
3. Apakah kestabilan kinetik
4. Perbandingan sampingan -Thermodynamic vs kestabilan kinetik dalam bentuk jadual
5. Ringkasan
Apakah kestabilan termodinamik?
Kestabilan termodinamik adalah kestabilan keadaan tenaga terendah sistem. Ia juga dikenali sebagai kestabilan kimia secara umum digunakan. Keadaan tenaga terendah sistem adalah di mana hasil produk optimum diperolehi. Ini bermakna kestabilan termodinamik diperoleh apabila sistem datang ke keadaan keseimbangan. Kadang -kadang, kestabilan ini berlaku apabila terdapat keseimbangan dinamik di mana atom dan molekul individu cenderung mengubah bentuknya, menjaga perubahan keseluruhan pada titik sifar.

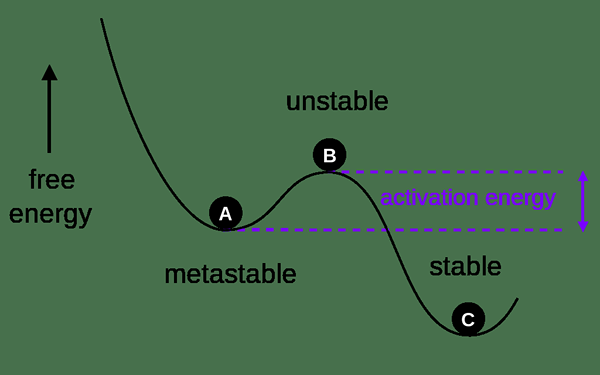
Rajah 01: Kestabilan produk di keadaan keseimbangan
Kebalikan dari kestabilan termodinamik adalah "kestabilan kinetik", yang menggambarkan kereaktifan sistem dan bukannya keadaan keseimbangan sistem itu.
Apakah kestabilan kinetik?
Kestabilan kinetik adalah kestabilan keadaan tenaga tertinggi sistem. Maksudnya; Kestabilan kinetik berlaku apabila terdapat peratusan reaktan optimum dalam sistem. Ini kerana reaktan biasanya mempunyai tahap tenaga yang tinggi yang menjadikan mereka bertindak balas antara satu sama lain untuk menukar produk yang mempunyai tahap tenaga yang rendah. Kestabilan kinetik sistem adalah berkaitan dengan kereaktifan reaktan. Selain itu, reaktan biasanya memerlukan input tenaga untuk menggerakkan reaksi dari kestabilan kinetik ke kestabilan termodinamik.
Apakah perbezaan antara kestabilan termodinamik dan kinetik?
Kestabilan termodinamik dan kinetik adalah istilah kimia penting dalam kimia fizikal. Perbezaan utama antara kestabilan termodinamik dan kinetik ialah kestabilan termodinamik merujuk kepada status produk, sedangkan kestabilan kinetik merujuk kepada status reaktan. Biasanya, reaktan reaksi mempunyai tenaga yang tinggi berbanding tahap tenaga produk. Dan, inilah sebab mengapa reaktan cenderung untuk menukar produk tenaga rendah agar dapat stabil.
Reaksi kimia biasanya memerlukan input tenaga untuk memindahkan sistem dari kestabilan kinetik ke kestabilan termodinamik di mana produk optimum dihasilkan. Oleh itu, istilah termodinamik merujuk kepada keadaan keseimbangan sistem, sementara istilah kinetik merujuk kepada kereaktifan sistem. Kadang-kadang, kestabilan termodinamik memberikan kestabilan sama ada reaksi keseimbangan atau tindak balas bukan keseimbangan.
Jadual berikut meringkaskan perbezaan antara kestabilan termodinamik dan kinetik.

Ringkasan -Thermodynamic vs Kestabilan Kinetik
Kestabilan termodinamik dan kinetik adalah istilah kimia penting dalam kimia fizikal. Kestabilan termodinamik adalah kestabilan keadaan tenaga terendah sistem sementara kestabilan kinetik adalah kestabilan keadaan tenaga tertinggi sistem. Perbezaan utama antara kestabilan termodinamik dan kinetik ialah kestabilan termodinamik merujuk kepada status produk, sedangkan kestabilan kinetik merujuk kepada status reaktan. Biasanya, sistem memerlukan beberapa tenaga input untuk memindahkan sistem dari kestabilan kinetik ke kestabilan termodinamik melalui kereaktifan reaktan.
Rujukan:
1. Anthony, hari. "Kestabilan kinetik." Sekolah Crystallography, Universiti Birbeck, 1996, boleh didapati di sini.
2. "Kestabilan termodinamik." Gambaran Keseluruhan | Topik Sciencedirect, Terdapat di sini.
Ihsan gambar:
1. "Kestabilan Thermodynamic en" oleh Woudloper - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia


