Perbezaan antara sulfur hexafluoride dan disulfur tetrafluoride
The Perbezaan utama antara sulfur hexafluoride dan disulfur tetrafluoride adalah Hexafluoride sulfur itu mempunyai ikatan kimia dengan panjang ikatan yang sama, tetapi disulfur tetrafluoride mempunyai ikatan kimia dengan panjang ikatan yang berbeza.
Sulfur hexafluoride dan disulfur tetrafluoride adalah sebatian bukan organik. Kedua -duanya mengandungi atom sulfur dan fluorin dalam sambungan dan susunan spatial yang berbeza. Walau bagaimanapun, bukan sahaja struktur kimia mereka tetapi keadaan fizikal dan sifat -sifat lain dari kedua -dua sebatian ini juga berbeza antara satu sama lain. Sebagai contoh, sulfur hexafluoride adalah sebatian gas pada suhu bilik, tetapi disulfur tetrafluoride adalah cecair.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu sulfur hexafluoride
3. Apa itu disulfur tetrafluoride
4. Perbandingan sampingan - sulfur hexafluoride vs disulfur tetrafluoride dalam bentuk jadual
5. Ringkasan
Apa itu sulfur hexafluoride?
Sulfur hexafluoride adalah sebatian bukan organik yang mempunyai formula kimia sf6. Ia adalah sebatian gas yang tidak berwarna dan tidak berbau yang tidak mudah terbakar dan tidak toksik. Ia dikategorikan sebagai gas rumah hijau. Ia juga merupakan penebat elektrik yang penting. Ia adalah gas yang lebih padat daripada udara.
Geometri sebatian ini adalah octahedral. Panjang ikatan semua ikatan S-F dalam molekul ini sama. Sulfur hexafluoride mempunyai atom sulfur pusat yang dilekatkan pada enam atom fluorin. Selain itu, molekul ini dianggap sebagai molekul hipervalen. Maksudnya; Molekul ini mempunyai elemen kumpulan utama yang mempunyai lebih daripada lapan elektron valensi. Dalam molekul ini, atom sulfur mempunyai dua belas elektron.
Oleh kerana sambungan atom dan susunan ruang mereka, molekul sulfur hexafluoride adalah nonpolar dan tidak larut dalam air. Tetapi, ia larut dalam pelarut organik nonpolar. Kita boleh menghasilkan sebatian ini menggunakan sulfur elemen tulen dan fluorin. Di sini kita perlu mendedahkan S8 pepejal ke f2 gas.
Terdapat banyak aplikasi sulfur hexafluoride:
- Digunakan sebagai industri elektrik penebat elektrik
- Dalam bidang perubatan untuk menyediakan tamponade dalam detasmen retina
- Sebagai ejen kontras dalam pengimejan ultrasound,
- Sebagai gas pengesan dalam menentukur model penyebaran udara jalan raya, dll.
Apa itu disulfur tetrafluoride?
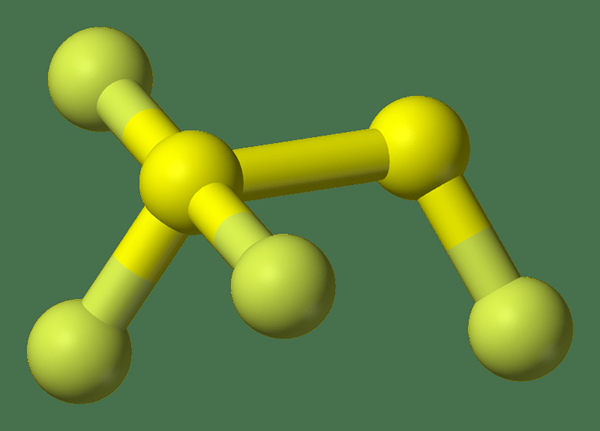
Disulfur tetrafluoride adalah sebatian bukan organik yang mempunyai formula kimia s2F4. Lebih tepat lagi, kita boleh menulis formula struktur untuk sebatian ini sebagai FSSF3 Kerana ia mempunyai tiga atom fluorin yang dilekatkan pada satu atom sulfur dan atom sulfur yang lain mengandungi atom fluorin yang tinggal. Panjang ikatan molekul ini berbeza, yang merupakan sifat molekul bukan organik yang tidak biasa.
Jisim molar sebatian ini adalah 140 g/mol. Ia wujud dalam keadaan cair pada suhu bilik. Selain itu, disulfur tetrafluoride dengan mudah menjalani hidrolisis dengan air. Ia juga secara spontan bertindak balas dengan oksigen untuk membentuk fluorida thionil. Kami boleh menyediakan tetrafluorida disulfur di makmal menggunakan sulfur klorida yang diluluskan fluorida kalium pada tekanan rendah dan suhu rendah. Walau bagaimanapun, tindak balas ini memberikan beberapa produk sampingan termasuk klorida dan fluorida sulfur yang berbeza. Kita boleh memisahkan sebatian yang dikehendaki melalui penyulingan suhu rendah.
Apakah perbezaan antara sulfur hexafluoride dan disulfur tetrafluoride?
Sulfur hexafluoride dan disulfur tetrafluoride adalah sebatian bukan organik yang mengandungi atom sulfur dan fluorin. Perbezaan utama antara sulfur hexafluoride dan disulfur tetrafluoride ialah sulfur hexafluoride mempunyai ikatan kimia dengan panjang ikatan yang sama, tetapi disulfur tetrafluoride mempunyai ikatan kimia dengan panjang ikatan yang berbeza. Tambahan pula, sulfur hexafluoride adalah sebatian gas pada suhu bilik, tetapi disulfur tetrafluoride adalah cecair. Jadi, ini adalah satu lagi perbezaan yang signifikan antara sulfur hexafluoride dan disulfur tetrafluoride.
Selain itu, jisim molar sulfur hexafluoride adalah 146 g/mol, manakala jisim molar disulfur tetrafluoride adalah 140 g/mol. Selain itu, kita boleh menghasilkan sulfur hexafluoride melalui menggunakan sulfur elemen tulen dan fluorin manakala penyediaan disulfur tetrafluorid.

Ringkasan -sulfur hexafluoride vs disulfur tetrafluoride
Sulfur hexafluoride dan disulfur tetrafluoride adalah sebatian bukan organik yang mengandungi atom sulfur dan fluorin. Perbezaan utama antara sulfur hexafluoride dan disulfur tetrafluoride ialah sulfur hexafluoride mempunyai ikatan kimia dengan panjang ikatan yang sama, sedangkan disulfur tetrafluoride mempunyai ikatan kimia dengan panjang bon yang berbeza.
Rujukan:
1. "Difluorodisulfanedifluoride." Wikipedia, Yayasan Wikimedia, 26 Okt. 2019, boleh didapati di sini.
Ihsan gambar:
1. "Sulfur-Hexafluoride-3D-VDW" (Domain Awam) melalui Commons Wikimedia
2. "Disulfur-Tetrafluoride-3D-Balls" oleh Benjah-Bmm27-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia