Perbezaan antara kompleks planar persegi dan tetrahedral
The Perbezaan utama antara kompleks planar persegi dan tetrahedral ialah Kompleks planar persegi mempunyai gambarajah medan kristal empat peringkat, tetapi kompleks tetrahedral mempunyai gambarajah medan kristal dua tingkat.
Teori medan kristal adalah teori dalam kimia yang menggambarkan pemecahan orbital elektron (terutamanya d dan f orbitals) kerana medan elektrik statik yang dihasilkan oleh caj anionik di sekeliling atom. Teori ini sangat penting dalam menggambarkan sifat -sifat kompleks logam peralihan. Kita dapat menerangkan struktur kompleks planar persegi dan tetrahedral juga.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu kompleks planar persegi
3. Apakah kompleks tetrahedral
4. Perbandingan sampingan - planar persegi vs. Kompleks tetrahedral dalam bentuk jadual
5. Ringkasan
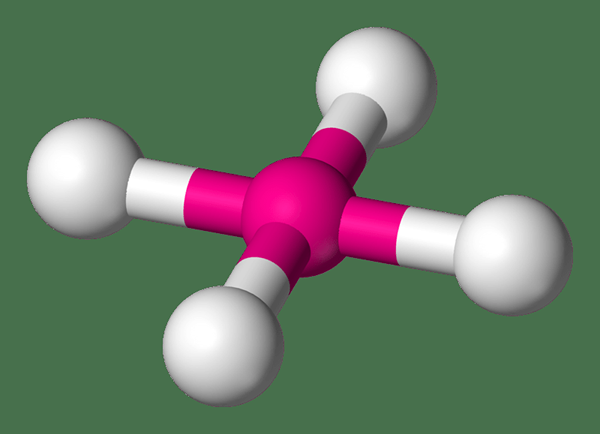
Apa itu kompleks planar persegi
Kompleks planar persegi adalah kompleks koordinasi yang mempunyai atom logam pusat yang dikelilingi oleh empat atom konstituen di sudut -sudut satah persegi yang sama. Sudut ikatan ikatan dalam struktur ini adalah 90 °. Logam peralihan yang mempunyai konfigurasi elektron yang berakhir d8 Kompleks koordinasi bentuk yang mempunyai geometri molekul ini. Sebagai contoh, RH (i), IR (I), PD (II), dll. Nombor koordinasi untuk kompleks planar persegi adalah empat.
Kita dapat menerangkan struktur kompleks ini menggunakan teori medan kristal (CFT). Menurut teori ini, kompleks planar persegi mempunyai gambarajah medan kristal empat peringkat. Dan, pemisahan empat peringkat ini dinamakan d4H. Empat tahap tenaga yang dihasilkan dinamakan dx2-y2, dxy, dz2, dan [dxz, dYz]. Selain itu, terdapat hubungan khusus antara geometri planar persegi dan geometri tetrahedral. Kita boleh menukar geometri tetrahedral menjadi geometri planar persegi dengan meratakan tetrahedron. Dan, penukaran ini menyediakan laluan untuk isomerisasi kompleks tetrahedral.
Apakah kompleks tetrahedral?
Kompleks Tetrahedral adalah kompleks koordinasi yang mempunyai atom logam pusat yang dikelilingi oleh empat atom konstituen di sudut tetrahedron. Sudut ikatan bon dalam struktur ini adalah kira -kira 109.5 °. Walau bagaimanapun, jika pengundi berbeza antara satu sama lain, sudut ikatan berbeza -beza. Terdapat dua jenis logam peralihan yang boleh membentuk jenis kompleks ini: logam yang mempunyai d0 konfigurasi dan d10 konfigurasi.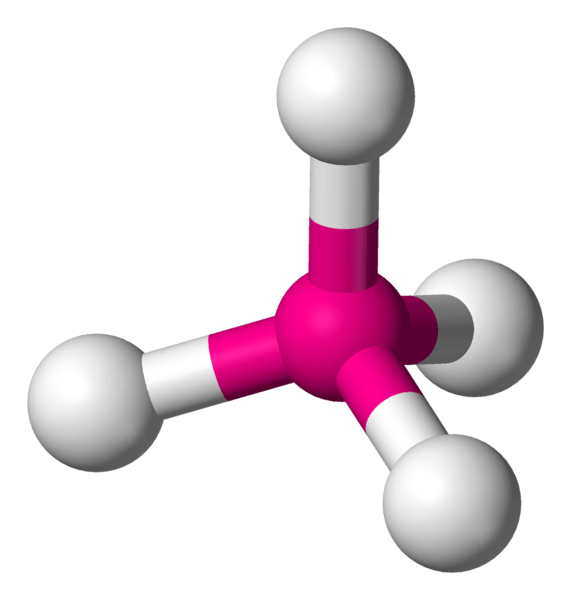
Selain itu, menurut teori medan kristal, kompleks tetrahedral mempunyai gambarajah medan kristal dua peringkat. Dua tahap tenaga rajah ini termasuk dua set orbital: Dxy, dxz, dYz Dalam satu tahap tenaga, dan Dx2-y2, dz2 di set lain.
Apakah perbezaan antara kompleks planar persegi dan tetrahedral?
Teori medan kristal sangat penting dalam menggambarkan sifat -sifat kompleks logam peralihan, serta struktur kompleks planar dan tetrahedral persegi. Perbezaan utama antara kompleks planar persegi dan tetrahedral ialah kompleks planar persegi mempunyai gambarajah medan kristal empat peringkat, tetapi kompleks tetrahedral mempunyai gambarajah medan kristal dua peringkat.
Selain itu, logam peralihan yang mempunyai konfigurasi elektron mereka berakhir dengan D8 Konfigurasi cenderung membentuk kompleks planar persegi, sementara logam yang mempunyai d0 konfigurasi dan d10 Konfigurasi cenderung membentuk kompleks tetrahedral.
Infographic di bawah menunjukkan lebih banyak perbandingan mengenai perbezaan antara kompleks planar dan tetrahedral persegi.
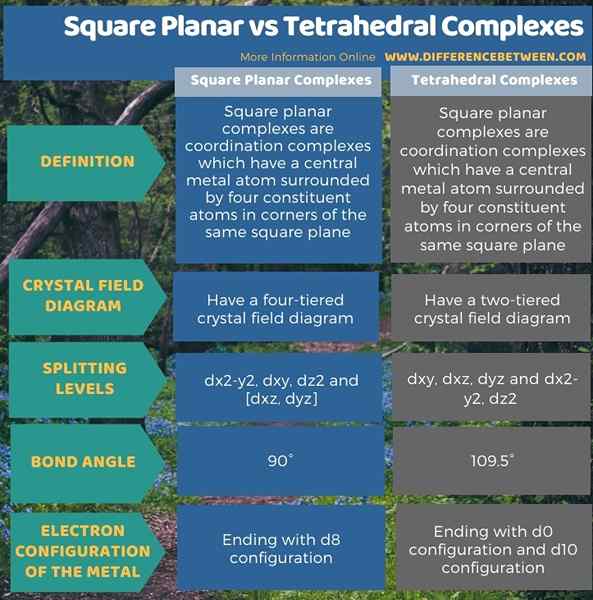
Ringkasan -planar persegi vs. Kompleks tetrahedral
Teori medan kristal sangat penting dalam menggambarkan sifat -sifat kompleks logam peralihan. Kita dapat menerangkan struktur kompleks planar persegi dan tetrahedral juga. Perbezaan utama antara kompleks planar persegi dan tetrahedral adalah bahawa kompleks planar persegi mempunyai gambarajah medan kristal empat peringkat, sedangkan kompleks tetrahedral mempunyai gambarajah medan kristal dua tingkat.
Rujukan:
1. Mott, Vallerie. "Pengenalan kepada Kimia."Lumen, boleh didapati di sini.
2. "Ikatan dalam sebatian koordinasi: teori medan kristal."Kimia Boundless, Lumen, boleh didapati di sini.
3. "Teori medan kristal."Libretexts, tersedia di sini.
Ihsan gambar:
1. "Square-Planar-3D-Balls" (Domain Awam) melalui Commons Wikimedia
2. "Tetrahedral-3D-Balls" (domain awam) melalui Wikimedia Commons


