Perbezaan antara natrium fosfat monobasic dan dibasic

Natrium fosfat monobasic vs dibasic | Natrium fosfat Dibasic vs Natrium fosfat monobasic | Monosodium fosfat vs disodium fosfat | Monosodium vs Disodium fosfat
Satu atom fosforus terikat dengan empat oxygens, untuk membentuk anion polyatomik a -3. Kerana ikatan tunggal dan ikatan berganda, antara P dan O, fosforus mempunyai keadaan pengoksidaan +5 di sini. Ia mempunyai geometri tetrahedral. Berikut adalah struktur anion fosfat.
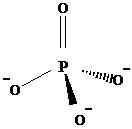
PO43-
Anion fosfat dapat bergabung dengan kation yang berbeza, untuk membentuk sebatian ionik. Natrium fosfat adalah garam seperti itu di mana tiga ion natrium secara elektrostatis terikat dengan satu anion fosfat. Trisodium fosfat adalah kristal berwarna putih, yang sangat larut di dalam air. Apabila larut dalam air, ia menghasilkan larutan alkali. Natrium fosfat monobasic dan natrium fosfat dibasic adalah dua sebatian natrium dan fosfat lain. Untuk asid, kita mentakrifkan istilah monobasic sebagai "asid, yang hanya memiliki satu proton yang boleh disumbangkan ke pangkalan semasa reaksi asid-asas."Begitu juga, dibasic untuk asid bermaksud mempunyai dua proton, yang boleh disumbangkan ke pangkalan. Tetapi apabila mempertimbangkan kedua -dua istilah ini mengenai garam, makna itu sama sekali berbeza. Garam monobasic merujuk kepada garam, yang hanya mempunyai satu atom logam yang tidak sama. Dan garam dibasic bermaksud mempunyai dua ion logam yang tidak seimbang. Dalam kes ini, ion logam univalen adalah kation natrium. Oleh kerana ini adalah garam, mereka mudah larut dalam air dan menghasilkan penyelesaian alkali. Sebatian ini boleh didapati secara komersial dalam bentuk hidrous dan anhidrat. Natrium fosfat monobasic dan dibasic bersama -sama sangat penting dalam sistem biologi sebagai penampan. Selanjutnya, secara perubatan kedua -dua ini digunakan sebagai julap garam, untuk merawat sembelit.
Natrium fosfat monobasic
Natrium fosfat monobasic atau monosodium fosfat mempunyai formula molekul nah2PO4. Jisim molar sebatian adalah 120 g mol-1. Anion dalam molekul ini bukan anion fosfat trivalen, tetapi H2PO4- Anion. Anion ini berasal dari ion fosfat di mana dua hidrogen terikat dengan dua oksigen negatif. Sebagai alternatif, di sisi lain ia telah diperoleh daripada penyingkiran satu proton dari asid fosforik (h3PO4). Anion fosfat dan h2PO4- Anion berada dalam keseimbangan, dalam media berair. Natrium fosfat monobasic disediakan sebagai kristal tidak berwarna atau serbuk putih. Ia mudah dibubarkan di dalam air, tetapi jangan larut dalam pelarut organik seperti alkohol. PKA ini antara 6.8-7.20. Kompaun ini boleh dibuat apabila asid fosforik bertindak balas dengan garam natrium seperti natrium halida.
Natrium fosfat dibasic
Kompaun ini juga dikenali sebagai disodium fosfat dan mempunyai formula molekul NA2HPO4. Jisim molar sebatian adalah 142 g mol-1. Apabila dua kation natrium menggantikan atom hidrogen dalam asid fosforik, natrium fosfat dibasic diperolehi. Oleh itu, di makmal kita dapat membuat sebatian ini dengan bertindak balas dua setara dengan natrium hidroksida dengan satu setara dengan asid fosforik. Kompaun adalah pepejal kristal putih, dan ia mudah larut di dalam air. PH penyelesaian berair ini adalah nilai asas, iaitu antara 8 dan 11. Garam ini digunakan untuk tujuan memasak, dan sebagai julap.
| Apakah perbezaan antara Natrium fosfat monobasic dan natrium fosfat dibasic? • Natrium fosfat monobasic mempunyai formula kimia nah2PO4, dan natrium fosfat dibasic mempunyai formula kimia na2HPO4. • Berat molekul natrium fosfat dibasic lebih tinggi daripada natrium fosfat monobasic. • Apabila natrium fosfat dibasic larut di dalam air, asasnya lebih tinggi dalam medium daripada ketika natrium fosfat monobasic larut dalam air. |


