Perbezaan antara SiO2 dan CO2

The Perbezaan utama antara SiO2 dan CO2 ialah SiO2 wujud dalam fasa pepejal sedangkan, CO2 wujud dalam fasa gas pada keadaan suhu dan tekanan standard.
SiO2 adalah silikon dioksida. CO2 adalah karbon dioksida. Kedua -dua silikon dan karbon adalah kumpulan 14 elemen dalam jadual berkala elemen. Kedua -dua oksida ini adalah oksida yang paling biasa dan stabil yang mereka buat. Walau bagaimanapun, terdapat banyak perbezaan antara SiO2 dan CO2. Perbezaan utama antara SiO2 dan CO2 adalah fasa di mana mereka wujud pada suhu dan tekanan standard.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu SiO2
3. Apa itu CO2
4. Perbandingan sampingan - SiO2 vs CO2 dalam bentuk jadual
5. Ringkasan
Apa itu SiO2?
SiO2 adalah silikon dioksida. Ia adalah oksida silikon yang paling biasa dan stabil. Kompaun ini wujud pada fasa pepejal pada keadaan suhu dan tekanan standard. Kita dapat menemuinya sebagai kuarza. Ia wujud sebagai penyusun utama pasir. Jisim molar sebatian ini ialah 60.08 g/mol. Ia kelihatan sebagai pepejal putih. Titik lebur dan mendidih masing -masing adalah 1,713 ° C dan 2,950 ° C.

Rajah 01: Contoh silikon dioksida
Walaupun atom silikon hanya mempunyai dua atom oksigen yang terikat kepadanya, geometri di sekitar atom silikon dikatakan tetrahedral. Itu kerana sebatian ini wujud sebagai bahan polimer yang mempunyai unit mengulangi SiO4. Terdapat banyak kegunaan kompaun ini. Ia mempunyai aplikasi untuk tujuan pembinaan, i.e. Pengeluaran Portland Cement. Juga, ia adalah bahan utama dalam pengeluaran kaca. Selanjutnya, SiO2 berguna dalam aplikasi makanan dan farmaseutikal juga, i.e. sebagai ejen aliran dalam makanan tepung.
Apa itu CO2?
CO2 adalah karbon dioksida, dan ia adalah oksida yang paling biasa dan stabil karbon. Ia wujud dalam fasa gas pada keadaan suhu dan tekanan standard. CO2 secara semulajadi berlaku sebagai gas karbon dioksida di atmosfera (kira -kira 0.03%). Ia adalah gas tanpa warna dengan ketumpatan yang lebih tinggi daripada udara kering. Jisim molar adalah 44.01 g/mol. Pada kepekatan yang rendah ia tidak berbau, tetapi pada kepekatan yang tinggi, ia mempunyai bau yang tajam dan asid. Titik lebur CO2 ialah -56.6 ° C.

Rajah 02: Gelembung karbon dioksida dalam minuman ringan
Molekul ini mempunyai struktur linear. Dua atom oksigen mengikat dengan atom karbon melalui ikatan berganda di sisi bertentangan. Molekul tidak mempunyai dipole elektrik kerana simetrik. Selain itu, sebatian ini larut dalam air; ia membentuk asid karbonik yang lemah. Hampir semua organisma aerobik menghasilkan gas ini dalam pernafasan mereka. Ia mempunyai banyak kegunaan dalam industri makanan, industri minyak, dan industri kimia. Sebagai contoh, ia adalah pendahulu kepada banyak bahan kimia lain seperti metanol. Selain itu, ia adalah bahan tambahan makanan, dan kami menggunakannya untuk pengeluaran minuman ringan berkarbonat. Selain itu, kita boleh menggunakan karbon dioksida untuk memadamkan api.
Apakah perbezaan antara SiO2 dan CO2?
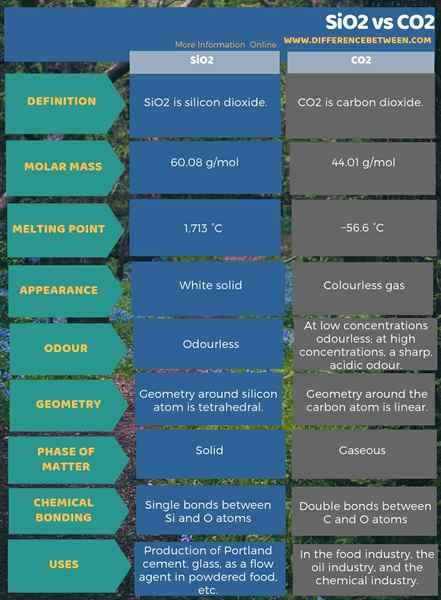
SiO2 adalah silikon dioksida, dan CO2 adalah karbon dioksida. Perbezaan utama antara SiO2 dan CO2 ialah SiO2 wujud dalam fasa pepejal sedangkan, CO2 wujud dalam fasa gas pada keadaan suhu dan tekanan standard. Selain itu, silikon dioksida telah mendapat warna putih manakala karbon dioksida adalah sebatian tanpa warna.
Perbezaan penting antara SiO2 dan CO2 ialah SiO2 mempunyai geometri tetrahedral di sekitar atom silikon manakala CO2 mempunyai geometri linear di sekitar atom karbon. Perbezaan selanjutnya antara SiO2 dan CO2 ialah SiO2 mempunyai ikatan tunggal antara atom Si dan O manakala CO2 mempunyai ikatan berganda antara atom C dan O.
Ringkasan -SiO2 vs CO2
Kedua -dua silikon (SI) dan karbon (c) adalah kumpulan 14 elemen dalam jadual berkala. Selain itu, oksida yang paling biasa dari unsur -unsur ini adalah SiO2 dan CO2. Perbezaan utama antara SiO2 dan CO2 ialah SiO2 wujud dalam fasa pepejal sedangkan, CO2 wujud dalam fasa gas pada keadaan suhu dan tekanan standard.
Rujukan:
1. Britannica, editor Encyclopaedia. "Karbon dioksida."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 3 Jan. 2018. Terdapat di sini
2. "Silicon dioksida."Wikipedia, Yayasan Wikimedia, 19 Nov. 2018. Terdapat di sini
Ihsan gambar:
1."Contoh silikon dioksida" oleh lhchem - kerja sendiri, (cc by -sa 3.0) melalui Commons Wikimedia
2."Soda Bubbles Macro" oleh Spiff (Domain Awam) melalui Commons Wikimedia


