Perbezaan antara resonans dan konjugasi π
The Perbezaan utama antara resonans dan konjugasi π ialah Resonans merujuk kepada kestabilan molekul dengan kehadiran elektron yang diselaraskan, sedangkan konjugasi π merujuk kepada konsep elektron PI yang diedarkan di seluruh kawasan molekul dan bukannya milik satu atom dalam molekul.
Resonans dan konjugasi π adalah istilah yang berkait rapat sejak konjugasi π menyebabkan resonans dalam sebatian kimia.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu resonans
3. Apakah konjugasi π
4. Perbandingan sampingan - Resonans vs π conjugation dalam bentuk jadual
5. Ringkasan
Apa itu resonans?
Resonans adalah konsep kimia yang menggambarkan interaksi antara pasangan elektron tunggal dan pasangan elektron ikatan sebatian. Umumnya, kesan resonans membantu dalam menentukan struktur kimia sebenar sebatian organik atau bukan organik. Kesan ini juga muncul dalam sebatian kimia yang mengandungi ikatan berganda dan pasangan elektron tunggal. Selain itu, kesan ini menyebabkan polariti molekul.
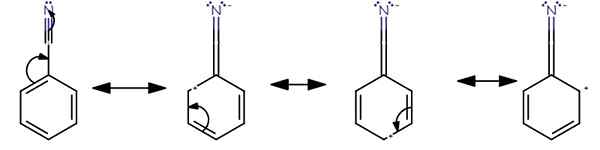
Resonans menunjukkan penstabilan sebatian kimia melalui elektron yang menghilangkan dalam ikatan PI. Di sini, elektron dalam molekul boleh bergerak di sekitar nukleus atom kerana elektron tidak mempunyai kedudukan tetap di dalam atom. Oleh itu, pasangan elektron tunggal dapat bergerak ke bon pi dan sebaliknya. Ini berlaku untuk mendapatkan keadaan yang stabil. Proses pergerakan elektron ini dikenali sebagai resonans. Selain itu, kita boleh menggunakan struktur resonans untuk mendapatkan struktur molekul yang paling stabil.

Rajah 01: Resonans dalam benzonitril
Molekul boleh mempunyai beberapa struktur resonans berdasarkan bilangan pasangan tunggal dan ikatan PI yang terdapat dalam molekul tersebut. Semua struktur resonans molekul mempunyai bilangan elektron yang sama dan susunan atom yang sama. Struktur sebenar molekul itu adalah struktur hibrid dalam semua struktur resonans. Terdapat dua jenis kesan resonans: kesan resonans positif dan kesan resonans negatif.
Kesan resonans positif menerangkan resonans yang boleh didapati dalam sebatian yang mempunyai caj positif. Kesan resonans positif membantu menstabilkan caj positif dalam molekul tersebut. Kesan resonans negatif menerangkan penstabilan caj negatif dalam molekul. Walau bagaimanapun, struktur hibrid yang diperolehi memandangkan resonans mempunyai tenaga yang lebih rendah daripada semua struktur resonans.
Apakah konjugasi π?
Istilah π conjugation merujuk kepada penghapusan dalam sebatian organik di mana kita dapat melihat pengagihan elektron PI tanpa bonding melalui molekul. Oleh itu, kita dapat menerangkan elektron dalam sistem konjugasi π sebagai elektron yang tidak bertenaga di sebatian kimia tersebut. Selain itu, istilah ini merujuk kepada elektron yang tidak dikaitkan dengan satu atom atau ikatan kovalen.
Sebagai contoh mudah, kita dapat memberikan benzena sebagai sistem aromatik yang mempunyai elektron yang diselaraskan. Umumnya, cincin benzena mempunyai enam elektron pi dalam molekul benzena; Kami sering menunjukkan ini secara grafik menggunakan bulatan. Lingkaran ini bermaksud bahawa elektron Pi dikaitkan dengan semua atom dalam molekul. Penyingkiran ini menjadikan cincin benzena mempunyai ikatan kimia dengan panjang ikatan yang sama.
Apakah perbezaan antara resonans dan konjugasi π?
Resonans dan konjugasi pi adalah istilah yang berkait rapat. Perbezaan utama antara resonans dan konjugasi π ialah resonans merujuk kepada kestabilan molekul dengan kehadiran elektron yang diselaraskan manakala konjugasi π merujuk kepada konsep elektron Pi yang diedarkan di seluruh kawasan molekul dan bukannya milik satu atom dalam molekul.
Infographic di bawah meringkaskan perbezaan antara resonans dan konjugasi π dalam bentuk jadual.
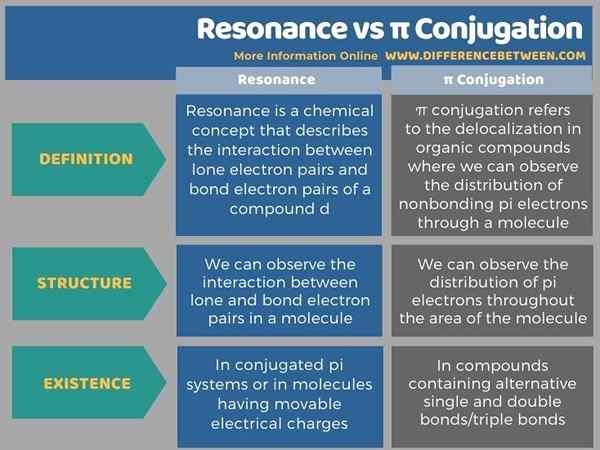
Ringkasan -Resonans vs π conjugation
Resonans dan konjugasi π adalah istilah yang berkait rapat di mana konjugasi π menyebabkan resonans dalam sebatian kimia. Perbezaan utama antara resonans dan konjugasi π ialah resonans merujuk kepada kestabilan molekul dengan kehadiran elektron yang diselaraskan manakala konjugasi π merujuk kepada konsep elektron Pi yang diedarkan di seluruh kawasan molekul dan bukannya milik satu atom dalam molekul.
Rujukan:
1. "Konjugasi dan Resonans dalam Kimia Organik." Kimia Organik Master, 26 Jan. 2020, boleh didapati di sini.
Ihsan gambar:
1. "Benzonitrile Resonance" oleh Fung06831 - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia


