Perbezaan antara ion dan sebatian polyatomik
The Perbezaan utama antara ion dan sebatian polyatomik ialah Ion polyatomik mempunyai caj elektrik positif atau negatif manakala sebatian tidak mempunyai caj elektrik bersih.
Ion polyatomik adalah istilah yang kita gunakan untuk menamakan spesies kimia yang mengandungi dua atau lebih atom yang mempunyai caj elektrik negatif atau positif bersih. Tuduhan elektrik ion ini adalah hasil daripada bilangan elektron yang terdapat dalam setiap atom; Sekiranya terdapat lebih banyak elektron daripada jumlah proton dalam atom, ia mendapat caj negatif bersih dan sebaliknya. Sebatian, sebaliknya, adalah spesies kimia tanpa caj elektrik. Mereka mempunyai bilangan elektron dan proton yang sama.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah ion polyatomik
3. Apa itu sebatian
4. Perbandingan sampingan - ion polyatomik vs sebatian dalam bentuk jadual
5. Ringkasan
Apakah ion polyatomik?
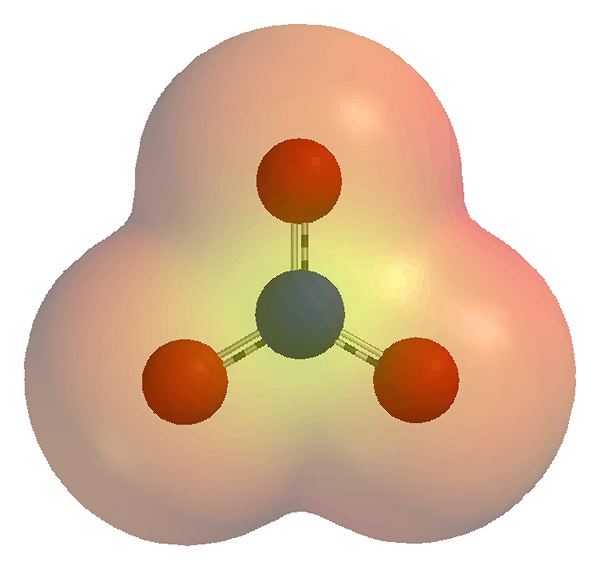
Ion polyatomik adalah spesies kimia yang mempunyai dua atau lebih atom dan cas elektrik bersih. Caj elektrik ini boleh sama ada caj positif atau caj negatif bergantung kepada bilangan elektron dan proton yang terdapat dalam spesies kimia. Sinonim untuk spesies ini adalah "ion molekul". Atom mengikat antara satu sama lain secara kovalen. Kita boleh mempertimbangkan beberapa kompleks logam sebagai ion polyatomik jika mereka bertindak sebagai satu unit. Sebaliknya, ion monoatomik adalah atom tunggal, yang membawa caj elektrik. Kita dapat mencari ion -ion ini dalam sebatian garam, sebatian koordinasi, dan banyak sebatian ionik lain; sebagai sebahagian daripada kompaun.

Rajah 01: ion nitrat
Beberapa contoh ion polyatomik:
- Ion asetat (CH3COO-)
- Benzoate ion (c6H5COO-)
- Ion karbonat (CO32-)
- Ion sianida (CN-)
- Ion hidroksida (oh-)
- Ion nitrit (tidak2-)
- Ion ammonium (NH4+)
Apa itu sebatian?
Sebatian adalah spesies kimia yang mengandungi molekul yang sama terdiri daripada atom dua atau lebih elemen kimia. Oleh itu, spesies kimia ini tidak membawa caj elektrik bersih. Oleh itu, mereka adalah spesies neutral. Atom mengikat antara satu sama lain melalui ikatan kovalen, ikatan koordinasi, atau ikatan ionik. Selain itu, jika terdapat molekul yang mengandungi dua atau lebih atom elemen yang sama terikat antara satu sama lain, ia bukan sebatian kerana tidak ada unsur yang berbeza.
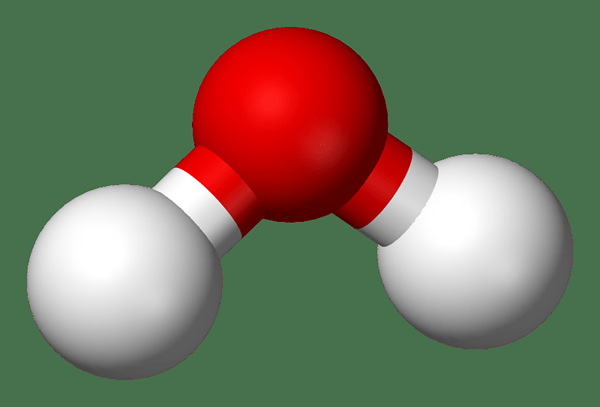
Rajah 02: Molekul air
Selain itu, menurut definisi, terdapat 4 jenis sebatian seperti berikut:
- Molekul mempunyai kombinasi unsur kimia yang berbeza
- Sebatian ionik terdiri daripada ikatan ionik
- Sebatian intermetallic yang mempunyai ikatan logam
- Kompleks koordinasi terdiri daripada bon koordinat
Kita boleh menggunakan formula kimia untuk menyatakan unsur -unsur kimia dan nisbah di antara mereka yang terdapat di dalam sebatian. Sebagai contoh, formula kimia molekul air ialah h2O. Ia mempunyai dua atom hidrogen dan satu atom oksigen, tetapi molekul tidak mempunyai caj elektrik bersih; Oleh itu, ia adalah sebatian kimia.
Apakah perbezaan antara ion dan sebatian polyatomik?
Ion polyatomik adalah spesies kimia yang mempunyai dua atau lebih atom dan cas elektrik bersih. Mereka mempunyai caj elektrik positif atau negatif. Sebatian adalah spesies kimia yang mengandungi molekul yang sama terdiri daripada atom dua atau lebih elemen kimia. Mereka tidak mempunyai caj elektrik bersih. Ini adalah perbezaan utama antara ion dan sebatian polyatomik. Selain itu, ion polyatomik mempunyai ikatan kovalen atau ikatan koordinasi antara atom. Sedangkan, sebatian mungkin mempunyai ikatan kovalen, ikatan ionik, ikatan logam atau ikatan koordinasi antara atom.
Infographic di bawah membentangkan perbezaan antara ion polyatomik dan sebatian dalam bentuk jadual.

Ringkasan -Ion Polatomik vs Sebatian
Perbezaan utama antara ion dan sebatian polyatomik adalah bahawa ion polyatomik mempunyai caj elektrik positif atau negatif manakala sebatian tidak mempunyai caj elektrik bersih. Ini terutamanya kerana ion polyatomik mempunyai bilangan elektron dan proton yang tidak seimbang manakala sebatian mempunyai bilangan elektron dan proton yang sama.
Rujukan:
1. Helmenstine, Anne Marie, PH.D. "Definisi dan contoh ion polyatomik."Pemikiran, Jun. 22, 2018. Terdapat di sini
2. Noller, Carl r., et al. "Kompaun Kimia."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 6 dec. 2016. Terdapat di sini
Ihsan gambar:
1."Nitrate-Ion-Elpot" oleh Benjah-Bmm27-Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2."Air-3D-Balls" oleh Benjah-Bmm27-Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia


