Perbezaan antara asid perchloric dan asid hidroklorik
The Perbezaan utama Antara asid perchloric dan asid hidroklorik ialah Asid perchloric mempunyai atom hidrogen, klorin dan oksigen manakala asid hidroklorik mempunyai atom hidrogen dan klorin sahaja.
Kedua -dua asid perchloric dan asid hidroklorik penting dalam tindak balas sintesis kimia kerana sifatnya yang sangat berasid. Kedua -duanya adalah bahan asid bukan organik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu asid perchloric
3. Apakah asid hidroklorik
4. Perbandingan sampingan - asid perchloric vs asid hidroklorik dalam bentuk jadual
5. Ringkasan
Apa itu asid perchloric?
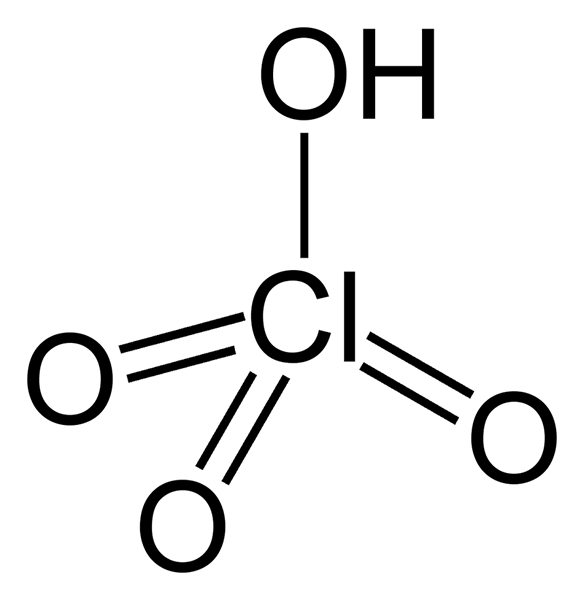
Asid perchloric adalah asid mineral yang mempunyai formula kimia HClo4. Ia adalah asid yang lebih kuat daripada asid sulfur dan nitrik. Ia berlaku sebagai cecair tidak berwarna yang tidak berbau juga. Asid perchloric panas adalah pengoksida yang kuat. Tetapi penyelesaian berair pada umumnya selamat. Selalunya, asid perchloric digunakan untuk penyediaan garam perchlorate, seperti ammonium perchlorate, dan campuran letupan.
Perchlorate adalah anion asid perchloric, yang mempunyai formula kimia CLO4-. Ini adalah derivatif penting asid perchloric yang mempunyai pelbagai aplikasi. Secara umum, istilah ini boleh merujuk kepada mana -mana sebatian yang mengandungi anion perchlorate. Keadaan pengoksidaan atom klorin dalam sebatian ini adalah +7. Ia adalah bentuk reaktif yang paling sedikit di kalangan klorat lain. Geometri ion ini adalah tetrahedral.
Kebanyakannya, sebatian yang mengandungi anion ini wujud sebagai pepejal tidak berwarna yang larut dalam air. Anion ini membentuk apabila sebatian perchlorate memisahkan air. Dalam skala perindustrian, kita boleh menghasilkan ion ini melalui kaedah elektrolisis; Ini melibatkan pengoksidaan natrium klorat berair.
Apakah asid hidroklorik?
Asid hidroklorik adalah hidrogen klorida berair, yang merupakan asid yang kuat. Hidrogen klorida mempunyai formula kimia hcl. Jisim molar sebatian ini adalah 36.5 g/mol. Asid hidroklorik mempunyai bau pedas. Selain itu, penting sebagai sebatian permulaan untuk banyak bahan kimia bukan organik seperti vinil klorida.
Asid hidroklorik dianggap sebagai bahan yang sangat berasid kerana ia dapat memisahkan sepenuhnya ionnya (ion hidrogen dan ion klorida) dan ia berlaku sebagai sistem asid yang mengandungi klorin dalam larutan akueus. Asid kuat ini boleh menyerang kulit kita ke atas pelbagai komposisi dan boleh menyebabkan luka kulit.

Secara semulajadi, asid hidroklorik terdapat dalam asid gastrik dalam sistem pencernaan kebanyakan haiwan, termasuk manusia. Ia boleh didapati secara komersil sebagai bahan kimia perindustrian untuk pengeluaran polyvinyl chloride untuk plastik. Selain itu, ia digunakan sebagai ejen penurunan dalam keperluan isi rumah, sebagai bahan tambahan makanan dalam industri makanan, dalam pemprosesan kulit, dan lain -lain.
Asid hidroklorik berlaku sebagai garam ion hidronium dan ion klorida. Kita boleh mempersiapkannya dengan merawat HCL dengan air. Asid HCl biasanya digunakan dalam analisis kimia untuk penyediaan atau pencernaan sampel untuk analisis. Ini kerana asid HCl pekat boleh membubarkan banyak logam, dan ia boleh membentuk klorida logam teroksida dengan gas hidrogen.
Apakah perbezaan antara asid perchloric dan asid hidroklorik?
Asid perchloric adalah asid mineral yang mempunyai formula kimia HClo4 manakala asid hidroklorik adalah hidrogen klorida akueus dengan formula kimia HCl. Perbezaan utama antara asid perchloric dan asid hidroklorik ialah asid perchloric mempunyai atom hidrogen, klorin dan oksigen manakala asid hidroklorik mempunyai atom hidrogen dan klorin sahaja.
Selain itu, perbezaan lain antara asid perchloric dan asid hidroklorik adalah keasidan mereka. Asid perchloric sangat berasid manakala asid hidroklorik kurang berasid berbanding dengan asid perchloric.
Di bawah infographic menunjukkan lebih banyak maklumat mengenai perbezaan antara asid perchloric dan asid hidroklorik.

Ringkasan -asid perchloric vs asid hidroklorik
Asid perchloric dan hidrogen klorida adalah asid tak organik yang kuat. Perbezaan utama antara asid perchloric dan asid hidroklorik ialah asid perchloric mempunyai atom hidrogen, klorin dan oksigen manakala asid hidroklorik mempunyai atom hidrogen dan klorin sahaja.
Rujukan:
1. "Asid Perchloric." Wikipedia, Yayasan Wikimedia, 24 Jun 2020, boleh didapati di sini.
Ihsan gambar:
1. "Perchloric-asid-2d" oleh Benjah-Bmm27-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia
2. "Asid hidroklorik 30 peratus" oleh W. OELEN -(CC BY -SA 3.0) melalui Commons Wikimedia


