Perbezaan antara ozonolisis oksidatif dan reduktif
The Perbezaan utama antara ozonolisis oksidatif dan reduktif ialah Ozonolisis oksidatif memberikan asid atau keton karboksilik sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau sebatian karbonil.
Ozonolisis adalah tindak balas kimia organik di mana ikatan kimia tak tepu dipotong menggunakan ozon. Di sini, molekul reaktan adalah alkena, alkynes, atau sebatian azo. Bergantung pada bahan permulaan, produk akhir berbeza; e.g. Sekiranya belahan berlaku di alkena atau alkynes, produk akhir adalah sebatian karbonyl. Ozonolisis boleh dilakukan dalam dua cara kerana ozonolisis oksidatif dan ozonolisis reduktif. Walau bagaimanapun, cara yang paling biasa adalah ozonolisis reduktif.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah ozonolisis oksidatif
3. Apakah ozonolisis reduktif
4. Perbandingan sampingan - oksidatif vs ozonolisis reduktif dalam bentuk tabular
5. Ringkasan
Apakah ozonolisis oksidatif?
Ozonolisis oksidatif adalah proses pengoksidaan yang melepasi ikatan tak tepu dengan kehadiran ozon. Ozon adalah allotrope reaktif oksigen. Dan, tindak balas kimia ini melibatkan ikatan berganda atau ikatan tiga antara atom karbon terikat kovalen dalam sebatian organik. Ikatan berganda atau tiga digantikan oleh oksigen, membentuk sebatian karbonyl. Tambahan pula, ozonolisis oksidatif adalah penting dalam mengenal pasti alkenes yang tidak diketahui.

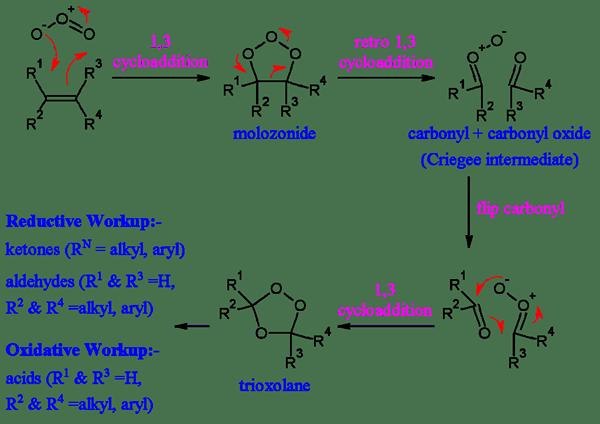
Rajah 01: Dua laluan ozonolisis
Selain itu, ozonolisis boleh didapati sebagai proses semula jadi. Produk akhir ozonolisis oksidatif adalah asid karboksilik. Apabila mempertimbangkan mekanisme ozonolisis oksidatif, langkah pertama ialah penambahan sinaran ozon kepada ikatan tak tepu. Di sana, elektron PI dalam ikatan tidak tepu aksi kerana nukleofil dan ozon adalah elektrofil. Apabila elektrofil menyerang sebatian, ikatan karbon-oksigen kedua terbentuk di hujung ikatan berganda. Selepas itu, penyusunan semula berlaku untuk membentuk produk yang stabil. Produk ini adalah ozonida yang kemudiannya terurai ke dalam keton dan asid karboksilik di hadapan hidrogen peroksida.
Apakah ozonolisis reduktif?
Ozonolisis reduktif adalah tindak balas kimia organik di mana ikatan tak tepu berkedukkan secara reduktif. Ozonolisis jenis ini memberikan alkohol dan sebatian karbonyl sebagai produk akhir. Walaupun ozon adalah oksidan yang baik, proses reduktif juga mungkin dengan ozonolisis. Dalam proses ini, ejen pengurangan ditambah kepada campuran tindak balas; e.g. logam zink atau dimetil sulfida.
Biasanya, ozonolisis reduktif adalah kaedah yang paling biasa untuk memecahkan ikatan tak tepu. Sebagai perbandingan dengan ozonolisis reduktif, ozonida yang dibentuk pada langkah pertama diuraikan oleh ejen pengurangan (dalam ozonolisis oksidatif, produk ozonida ini dipotong oleh hidrogen peroksida). Apabila bahan permulaan ozonolisis reduktif adalah alkena, produk akan menjadi bentuk alkohol atau aldehida bersama dengan ketone.
Apakah perbezaan antara ozonolisis oksidatif dan reduktif?
Ozonolisis adalah tindak balas kimia organik. Ia boleh berlaku dalam dua laluan sebagai laluan oksidatif dan laluan reduktif. Ozonolisis oksidatif adalah proses pengoksidaan yang melepasi ikatan tak tepu dengan kehadiran ozon. Ozonolisis reduktif adalah tindak balas kimia organik di mana ikatan tak tepu berkedukkan secara reduktif. Perbezaan utama antara ozonolisis oksidatif dan reduktif ialah ozonolisis oksidatif memberikan asid atau keton karboksilat sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau sebatian karbonil.
Infographic di bawah meringkaskan perbezaan antara ozonolisis oksidatif dan reduktif.

Ringkasan -Ozonolisis reduktif oksidatif vs
Ozonolisis adalah tindak balas kimia organik. Ia boleh berlaku dalam dua laluan sebagai laluan oksidatif dan laluan reduktif. Perbezaan utama antara ozonolisis oksidatif dan reduktif ialah ozonolisis oksidatif memberikan asid karboksilat atau keton sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau sebatian karbonil.
Rujukan:
1. "12.12: Pembelahan oksidatif: Ozonolisis."Kimia Libreetexts, Libretexts, 3 Jun 2019, boleh didapati di sini.
2. "Ozonolisis (kerja oksidatif)."KimiaScore, 12 Feb. 2020, boleh didapati di sini.
3. "Ozonolisis."Wikipedia, Yayasan Wikimedia, 7 Mar. 2020, boleh didapati di sini.
Ihsan gambar:
1. "Ozonolysis-2" oleh Ozonolisis.PNG: Kerja Kimia: Kimia (bercakap) - Ozonolisis.PNG (CC oleh 2.5) Melalui Wikimedia Commons


