Perbezaan antara molariti dan molaliti

The Perbezaan utama antara molariti dan molalitas adalah bahawa molaritas adalah Bilangan tahi lalat larut dalam 1 liter penyelesaian manakala molality adalah bilangan tahi lalat yang hadir dalam 1kg pelarut.
Molariti dan molaliti adalah ukuran kepekatan penyelesaian. Kepekatan penyelesaian memberikan jumlah larutan yang dibubarkan dalam jumlah penyelesaian. Kedua -dua langkah ini berbeza antara satu sama lain mengikut parameter yang kami gunakan untuk mengukur jumlah unit penyelesaian; Molariti menganggap kelantangan penyelesaian sementara molality menganggap jisim pelarut. Walau bagaimanapun, dalam kedua -dua kes, kita mengukur bilangan larutan dalam tahi lalat.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu molariti
3. Apa itu Molality
4. Perbandingan sampingan - molariti vs molality dalam bentuk jadual
5. Ringkasan
Apa itu molariti?
Molariti adalah kepekatan penyelesaian yang diberikan oleh bilangan larutan yang ada dalam satu liter penyelesaian. Oleh itu, kita mengukur kepekatan penyelesaian melalui jumlah apabila menentukan molariti. Unit pengukuran adalah mol/l.

Rajah 01: Penyelesaian yang berbeza mempunyai kepekatan yang berbeza bergantung pada jumlah penyelesaian
Tambahan pula, parameter ini bergantung kepada suhu penyelesaian kerana jumlah penyelesaian boleh berubah dengan suhu, i.e. Hampir semua kali jumlah cecair berkembang dengan peningkatan suhu. Contohnya, penyelesaian yang mengandungi dua tahi lalat larut dibubarkan dalam satu liter penyelesaian mempunyai 2.Kepekatan 0 mol/l. Kita boleh menunjukkan molariti dengan "m".
Apa itu Molality?
Molaliti adalah kepekatan penyelesaian yang diberikan oleh jumlah larutan yang ada dalam satu kilogram pelarut. Oleh itu, kita mengukur kepekatan penyelesaian melalui jisim pelarut ketika menentukan molalitas penyelesaiannya. Oleh itu, unit pengukuran adalah mol/kg.
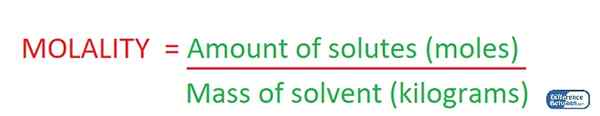
Rajah 02: Penentuan molaliti penyelesaian
Selain itu, parameter ini tidak bergantung pada suhu penyelesaian kerana jisim tidak berubah dengan suhu. Contohnya, jika penyelesaian mengandungi 2 mol larutan yang dibubarkan dalam satu kilogram pelarut, maka kepekatannya ialah 2.0 mol/kg. Kami biasanya menunjukkan istilah ini sebagai "m".
Apakah perbezaan antara molariti dan molaliti?
Molariti adalah kepekatan penyelesaian yang diberikan oleh jumlah larutan yang ada dalam satu liter penyelesaian manakala molaliti adalah kepekatan penyelesaian yang diberikan oleh jumlah larutan yang ada dalam satu kilogram pelarut. Oleh itu, ini adalah perbezaan utama antara molariti dan molaliti. Tambahan pula, perbezaan penting antara molariti dan molaliti adalah bahawa molariti bergantung kepada suhu penyelesaian sementara molalitas bebas dari suhu. Ini terutamanya kerana jumlahnya dapat berkembang dengan peningkatan suhu manakala jisim tetap berterusan apabila suhu berubah.
Infographic di bawah menunjukkan perbezaan antara molariti dan molaliti dalam bentuk jadual.
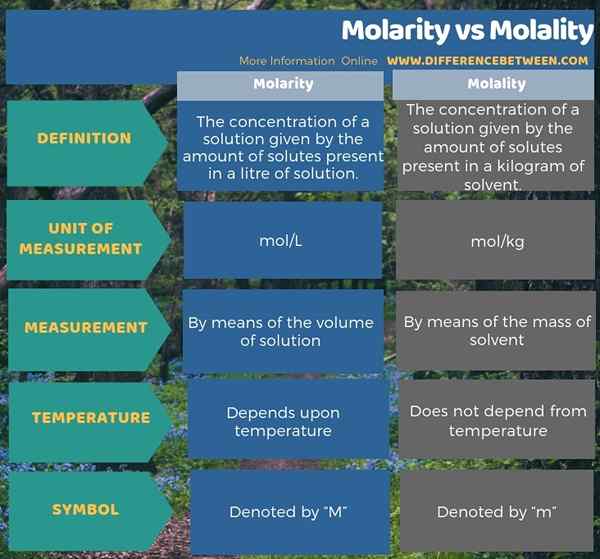
Ringkasan -Molariti vs Molality
Molariti dan molaliti adalah ukuran kepekatan penyelesaian. Perbezaan utama antara molariti dan molalitas adalah bahawa molaritas adalah bilangan tahi lalat larut dalam 1 liter larutan sedangkan molalitas adalah bilangan tahi lalat larut yang ada dalam 1kg pelarut.
Rujukan:
1. Mott, Vallerie. "Pengenalan kepada Kimia."Lumen. Terdapat di sini
2. "Kepekatan molar."Wikipedia, Yayasan Wikimedia, 17 Okt. 2018. Terdapat di sini
Ihsan gambar:
1."217043" oleh PublicDomainPictures (CC0) melalui Pixabay


