Perbezaan antara metana dan etana

Perbezaan utama - metana vs etana
Metana dan etana adalah ahli terkecil dari keluarga alkana. Formula molekul kedua -dua sebatian organik ini adalah CH4 dan c2H6 masing -masing. The Perbezaan utama antara metana dan etana adalah struktur kimia mereka; Molekul etana boleh dianggap sebagai dua kumpulan metil disatukan sebagai dimer kumpulan metil. Perbezaan kimia dan fizikal yang lain terutamanya timbul kerana perbezaan struktur ini.
Apa itu metana?
Metana adalah ahli terkecil keluarga alkana dengan formula kimia CH4 (Empat atom hidrogen terikat dengan satu atom karbon). Ia dianggap sebagai komponen utama gas asli. Metana adalah gas yang tidak berwarna, tidak berbau dan tidak enak; juga dikenali sebagai Carbane, Gas Marsh, Gas Asli, Karbon Tetrahydride, dan Karbida hidrogen. Ia dapat dengan mudah dinyalakan, dan wapnya lebih ringan daripada udara.
Metana secara semula jadi dijumpai di bawah tanah dan di bawah dasar laut. Metana atmosfera dianggap sebagai gas rumah hijau. Metana rosak ke ch3- dengan air di atmosfera. 
Apa itu Ethane?
Ethane adalah sebatian gas yang tidak berwarna dan tidak berbau pada suhu dan tekanan standard. Formula molekul dan berat molekulnya adalah c2H6 dan 30.07 g · mol-1 masing -masing. Ia diasingkan dari gas asli, sebagai hasil sampingan dari proses penapisan petroleum. Ethane sangat penting dalam pengeluaran etilena. 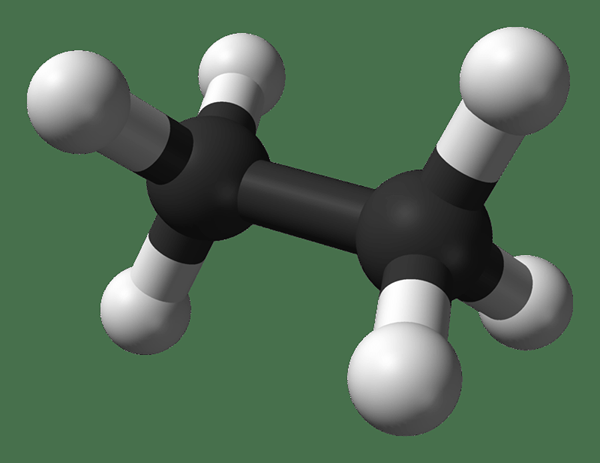
Apakah perbezaan antara metana dan etana?
Ciri -ciri metana dan etana
Struktur:
Metana: The formula molekul metana adalah Ch4, Dan ia adalah contoh molekul tetrahedral dengan empat ikatan C-H bersamaan (Sigma Bonds). Sudut ikatan antara atom H-C-H ialah 109.50 dan semua bon C-H bersamaan, dan sama dengan108.70 malam.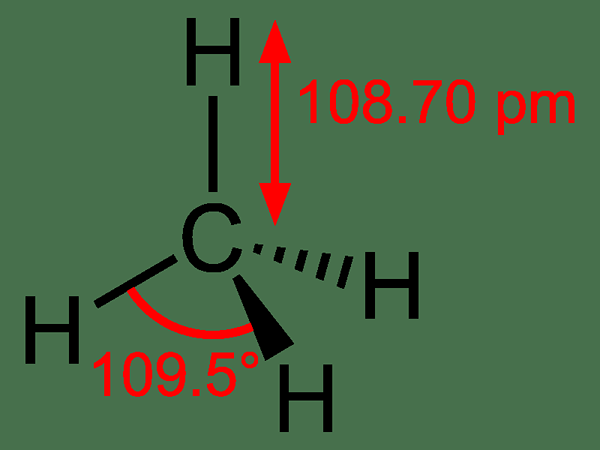
Ethane: The Formula etana molekul adalah C2H6, Dan ia adalah hidrokarbon tepu kerana ia tidak mengandungi pelbagai bon.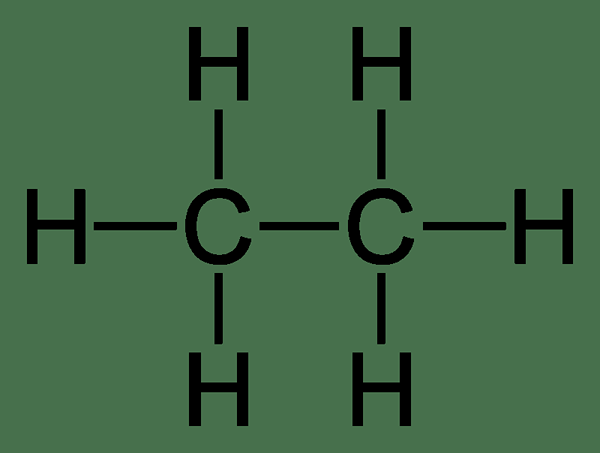
Sifat Kimia:
Metana:
Kestabilan: Metana adalah molekul kimia yang sangat stabil yang tidak bertindak balas dengan kmno4, K2Cr2O7, H2Jadi4 atau hno3 di bawah keadaan biasa.
Pembakaran: Di hadapan udara atau oksigen yang berlebihan, metana terbakar dengan api yang tidak berwarna biru pucat yang menghasilkan karbon dioksida dan air. Ia adalah tindak balas yang sangat eksotermik; Oleh itu, ia digunakan sebagai bahan bakar yang sangat baik. Di hadapan udara atau oksigen yang tidak mencukupi, sebahagiannya terbakar ke dalam gas karbon monoksida (CO).
Reaksi penggantian: Metana menunjukkan tindak balas penggantian dengan halogen. Dalam tindak balas ini, satu atau lebih atom hidrogen digantikan dengan bilangan atom halogen yang sama dan ia dipanggil "halogenasi."Ia bertindak balas dengan klorin (CL) dan bromin (BR) dengan kehadiran cahaya matahari.
Tindak balas dengan stim: Apabila campuran metana dan stim diluluskan melalui nikel yang dipanaskan (1000 K) yang disokong pada permukaan alumina, ia dapat menghasilkan hidrogen.
Pyrolysis: Apabila metana dipanaskan hingga kira -kira 1300 K, ia akan dibusukkan kepada karbon hitam dan hidrogen.
Ethane:
Reaksi: Gas Ethane (CH3Ch3) bertindak balas dengan wap bromin dengan kehadiran cahaya untuk membentuk bromoetana, (ch3Ch2Br) dan bromida hidrogen (Hbr). Ia adalah tindak balas penggantian; Atom hidrogen dalam etana digantikan oleh atom bromin.
Ch3Ch3 + Br2 à ch3Ch2Br +Hbr
Pembakaran: Pembakaran Ethane Lengkap menghasilkan 1559.7 kJ/mol (51.9 kJ/g) haba, karbon dioksida, dan air.
2 c2H6 + 7 O2 → 4 Co2 + 6 H2O + 3120 kJ
Ia juga boleh berlaku tanpa lebihan oksigen, menghasilkan campuran karbon amorf dan karbon monoksida.
2 c2H6 + 3 O2 → 4 C + 6 H2O + tenaga
2 c2H6 + 5 O2 → 4 CO + 6 H2O + tenaga
2 c2H6 + 4 O2 → 2 c + 2 co + 6 H2O + tenaga dan lain -lain.
Definisi:
Reaksi penggantian: tindak balas penggantian adalah tindak balas kimia yang melibatkan anjakan satu kumpulan berfungsi dalam sebatian kimia dan menggantikannya oleh Kumpulan lain yang berfungsi.
Kegunaan:
Metana: Metana digunakan dalam banyak proses kimia perindustrian (sebagai bahan bakar, gas asli, gas asli cecair) dan diangkut sebagai cecair yang disejukkan.
Ethane: Ethane digunakan sebagai bahan bakar untuk motor dan sebagai penyejuk untuk sistem suhu yang sangat rendah. Ia dihantar dalam silinder keluli sebagai gas cecair di bawah tekanan wap sendiri.
Rujukan: "Ethane". Wikipedia. N.p., 2016. Web. 7 Jun 2016. Khanna, Bhishm. "Apakah sifat kimia metana ?". Pengawet.com. N.p., 2016. Web. 7 Jun 2016. "Methane | CH4 - Pubchem ”. Pubchem.NCBI.NLM.NIH.gov. N.p., 2016. Web. 7 Jun 2016. "Metana". Wikipedia. N.p., 2016. Web. 7 Jun 2016. Imej ihsan: "Model bola-dan-melekat molekul metana" oleh (domain awam) melalui Commons Wikimedia "Model Ball-and-Stick Ethane Molecule" Y Ben Mills-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia "Methane" oleh Jynto-Kerja sendiri, berdasarkan fail: Methane-CRC-MW-Dimensions-2D.PNG, (Domain Awam) melalui Commons Wikimedia "Ethane" (Domain Awam) melalui Commons Wikimedia

