Perbezaan antara sebatian hipervalen dan hipovalen
The Perbezaan utama antara sebatian hipervalen dan hipovalen ialah Sebatian Hypervalent mengandungi atom pusat dengan lebih daripada lapan elektron dalam shell elektron valensi manakala sebatian hipovalen mengandungi atom pusat dengan kurang daripada lapan elektron dalam shell elektron valensi.
Istilah hipervalen dan hipovalen merujuk kepada sebatian kovalen bukan organik yang mengandungi atom pusat. Kedua -dua jenis sebatian ini berbeza antara satu sama lain bergantung kepada bilangan elektron di atom pusat - sebatian hipervalen mempunyai oktet lengkap manakala sebatian hipovalen tidak.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu sebatian hipervalen
3. Apa itu sebatian hipovalen
4. Perbandingan sampingan - sebatian hypervalent vs hipovalen dalam bentuk tabular
5. Ringkasan
Apa itu sebatian hipervalen?
Sebat. Kami juga menyebutnya sebagai oktet yang diperluaskan. Saintis pertama yang menentukan jenis molekul ini ialah Jeremy I. Musher, pada tahun 1969. Terdapat beberapa kelas sebatian hipervalen seperti sebatian iodin hipervalen, sebatian gas mulia seperti sebatian xenon, polyfluorides halogen, dan lain -lain.
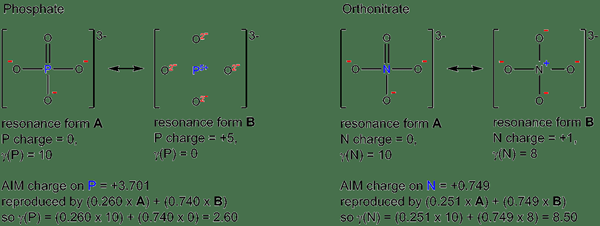
Rajah 01: Sebatian hipervalen
Ikatan kimia dalam sebatian hipervalen dapat diterangkan berdasarkan teori orbital molekul. Sebagai contoh, jika kita mengambil sebatian sulfur hexafluoride, ia mempunyai enam atom fluorin yang terikat kepada satu atom sulfur melalui ikatan tunggal. Oleh itu, terdapat 12 elektron di sekitar atom sulfur. Menurut teori orbital molekul, orbital 3s, tiga orbital 3p dan enam orbital 2p dari setiap atom fluorin menyumbang kepada pembentukan kompaun ini. Oleh itu, terdapat sejumlah sepuluh orbital atom yang terlibat dalam pembentukan kompaun. Menurut konfigurasi elektron sulfur dan fluorin, ada ruang untuk 12 elektron valensi. Oleh kerana terdapat 12 elektron, sebatian sulfur hexafluoride adalah sebatian hipervalen.
Apa itu sebatian hipovalen?
Sebatian hipovalen adalah spesies kimia yang mengandungi atom pusat dengan kurang daripada lapan elektron dalam shell elektron valensi. Oleh itu, ini dinamakan sebagai spesies kekurangan elektron. Tidak seperti sebatian hipervalen, hampir semua sebatian hipovalen adalah spesies bukan ionik. Oleh itu, mereka kebanyakannya berkuasa atau berbutir.

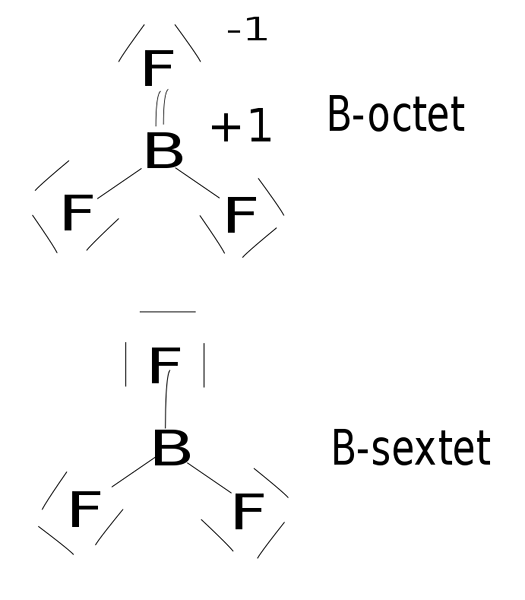
Rajah 02: Boron trifluoride adalah sebatian hipovalen
Sebatian kovalen ini tidak menanggung lebih daripada empat ikatan kovalen tunggal di sekelilingnya sejak empat sebatian kovalen merujuk kepada lapan elektron. Di samping itu, bentuk sebatian kovalen kebanyakannya linear atau trigonal planar.
Apakah perbezaan antara sebatian hipervalen dan hipovalen?
Perbezaan utama antara sebatian hipervalen dan hipovalen ialah sebatian hipervalen adalah spesies kimia yang mengandungi atom pusat dengan lebih daripada lapan elektron dalam shell elektron valensi, sedangkan sebatian hipovalen adalah spesies kimia yang mengandungi atom pusat dengan kurang daripada lapan elektron dalam kulit elektron valensi. Selain itu, sebatian hipervalen yang paling banyak adalah spesies ionik, sementara hampir semua sebatian hipovalen adalah sebatian kovalen.
Tambahan pula, bentuk sebatian hipervalen kovalen sama ada struktur tetragonal atau lebih kompleks, sementara sebatian hipovalen tidak dapat membentuk struktur rumit; mereka sama ada linear atau trigonal planar. Oleh itu, ini juga merupakan perbezaan yang signifikan antara sebatian hipervalen dan hipovalen. Selain itu, terdapat lebih daripada empat ikatan kovalen di sekitar atom pusat sebatian hipervalen tetapi terdapat dua atau tiga ikatan kovalen di sekitar atom pusat sebatian hipovalen.

Ringkasan -Sebatian Hypervalent vs Hypovalent
Istilah hipervalen dan hipovalen menggambarkan sebatian kovalen bukan organik yang mengandungi atom pusat. Perbezaan utama antara sebatian hipervalen dan hipovalen adalah bahawa sebatian hipervalen adalah spesies kimia yang mengandungi atom pusat dengan lebih daripada lapan elektron dalam shell elektron valensi, tetapi sebatian hipovalen adalah spesies kimia yang mengandungi atom pusat dengan kurang daripada lapan elektron dalam shell elektron valensi.
Rujukan:
1. "Molekul Hypervalent." Wikipedia, Yayasan Wikimedia, 18 Jan. 2020, boleh didapati di sini.
Ihsan gambar:
1. "Pengiraan Gamma Hypervalency" oleh Marcus Durrant - Kerja Sendiri (CC BY -SA 4.0) melalui Commons Wikimedia
2. "BF3-Lewis" oleh JCWF di Dutch Wikibooks (CC BY-SA 2.5) Melalui Wikimedia Commons


