Perbezaan antara hidrolisis dan pemeluwapan

Hidrolisis vs pemeluwapan
Pemeluwapan dan hidrolisis adalah dua jenis tindak balas kimia, yang terlibat dalam pembentukan bon dan kerosakan bon. Pemeluwapan adalah sebaliknya hidrolisis. Kedua -dua jenis tindak balas ini biasanya dijumpai dalam sistem biologi, dan kami juga menggunakan tindak balas ini untuk mendapatkan banyak produk penting secara komersil.
Pemeluwapan
Reaksi pemeluwapan adalah sejenis tindak balas kimia di mana molekul kecil berkumpul untuk membentuk molekul tunggal yang besar. Tindak balas berlaku dalam dua kumpulan berfungsi dalam molekul. Ciri ciri lain dari tindak balas pemeluwapan adalah bahawa molekul kecil hilang semasa reaksi. Molekul ini boleh menjadi air, hidrogen klorida, asid asetik, dan lain -lain. Sekiranya molekul yang hilang adalah air, jenis reaksi pemeluwapan dikenali sebagai tindak balas dehidrasi. Oleh kerana molekul reaktan lebih kecil dan molekul produk sangat besar, ketumpatan produk akan selalu lebih tinggi daripada reaksi dalam reaksi pemeluwapan. Reaksi pemeluwapan berlaku dalam beberapa cara. Sebagai contoh, kita boleh membahagikannya secara meluas kepada dua jenis sebagai tindak balas pemeluwapan intermolecular dan reaksi pemeluwapan intra. Sekiranya kedua-dua kumpulan berfungsi tinggal dalam molekul yang sama, mereka dikenali sebagai pemeluwapan intra-molekul. Sebagai contoh, glukosa mempunyai struktur linear seperti berikut.
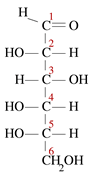
Dalam penyelesaian, majoriti molekul berada dalam struktur kitaran. Apabila struktur kitaran terbentuk, -OH pada karbon 5 ditukar menjadi hubungan eter, untuk menutup cincin dengan karbon 1. Ini membentuk enam struktur cincin hemiacetal ahli. Semasa tindak balas pemeluwapan intra-molekul ini, molekul air ditolak, dan hubungan eter terbentuk. Reaksi intermolecular menghasilkan banyak produk yang berguna dan biasa. Selama ini, tindak balas berlaku antara kumpulan berfungsi dua molekul berasingan. Contohnya, semasa membentuk makromolekul seperti protein, asid amino dipendekkan. Molekul air dilepaskan, dan hubungan amide terbentuk yang dikenali sebagai ikatan peptida. Apabila dua asid amino terikat bersama, dipeptida terbentuk, dan apabila banyak asid amino disatukan, ia dipanggil polipeptida. DNA dan RNA juga dua makromolekul terbentuk sebagai hasil daripada tindak balas pemeluwapan antara nukleotida. Reaksi pemeluwapan menghasilkan molekul yang sangat besar dan kadang -kadang molekul tidak begitu besar. Contohnya: Dalam tindak balas esterifikasi antara alkohol dan asid karboksilik, molekul ester kecil jika terbentuk. Pemeluwapan penting dalam pembentukan polimer. Polimer adalah molekul besar, yang mempunyai unit struktur yang sama berulang kali. Unit berulang dipanggil monomer. Monomer ini terikat antara satu sama lain dengan ikatan kovalen untuk membentuk polimer.
Hydrolysis
Ini adalah tindak balas di mana ikatan kimia dipecahkan menggunakan molekul air. Semasa tindak balas ini, molekul air berpecah menjadi proton dan ion hidroksida. Dan kemudian kedua -dua ion ini ditambah ke dua bahagian molekul di mana ikatan dipecahkan. Contohnya, berikut adalah ester. Ikatan ester antara -co dan -o.
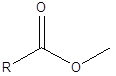
Dalam hidrolisis, proton dari air menambah ke sisi -O, dan ion hidroksida menambah ke sisi -co. Oleh itu, sebagai hasil daripada hidrolisis, alkohol dan asid karboksilik akan membentuk reaktan ketika membentuk ester.
| Apakah perbezaan antara hidrolisis dan pemeluwapan? • Hydrolysis adalah sebaliknya pemeluwapan. • Reaksi pemeluwapan membuat ikatan kimia manakala hidrolisis memecahkan ikatan kimia. • Polimer dibuat oleh tindak balas pemeluwapan, dan mereka dipecahkan oleh tindak balas hidrolisis. • Semasa tindak balas pemeluwapan, molekul air dapat dikeluarkan. Dalam tindak balas hidrolisis, molekul air dimasukkan ke dalam molekul. |


