Perbezaan antara sel galvanik dan sel tumpuan
The Perbezaan utama antara sel galvanik dan sel tumpuan ialah a sel galvanik mungkin atau mungkin tidak mempunyai dua sel separuh dengan komposisi yang sama manakala sel tumpuan mempunyai dua sel separuh dengan komposisi yang sama.
Kedua -dua sel galvanik dan sel tumpuan adalah sel elektrokimia. Sel elektrokimia adalah peranti yang dapat menjana elektrik menggunakan tindak balas kimia atau membuat tindak balas kimia berlaku menggunakan elektrik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu sel galvanik
3. Apa itu sel tumpuan
4. Perbandingan sampingan - sel galvanik vs sel kepekatan dalam bentuk jadual
5. Ringkasan
Apa itu sel galvanik?
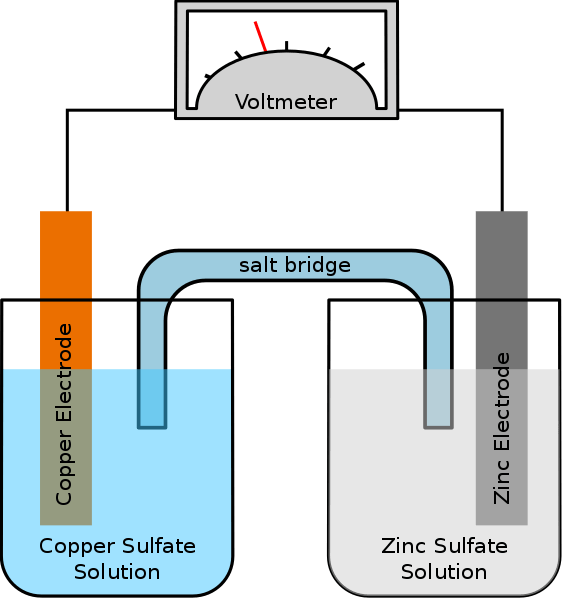
Sel galvanik adalah jenis sel elektrokimia yang menggunakan tindak balas redoks spontan untuk menjana tenaga elektrik. Sinonim untuk sel ini adalah sel voltan. Sel mengandungi dua sel separuh yang boleh menjadi komposisi yang sama atau komposisi yang berbeza. Setiap separuh sel mengandungi elektrod dan elektrolit. Elektrod harus direndam dalam larutan elektrolisis. Kadang -kadang elektrolit ini benar -benar terpisah, tetapi masa lain mereka dipisahkan hanya dengan halangan berliang. Apabila elektrolit dipisahkan sepenuhnya, kita perlu menggunakan jambatan garam untuk mengekalkan pergerakan ion antara kedua -dua elektrolit.

Rajah 01: Sel galvanik sederhana
Dalam menyediakan sel ini, kita perlu mempertimbangkan sama ada elektrod dan elektrolit adalah spontan atau tidak. Kita dapat menemuinya secara teoritis dengan mengira potensi elektrod setiap sel separuh. Walau bagaimanapun, sel setengah harus menunjukkan pengoksidaan, sedangkan sel separuh yang lain harus menunjukkan tindak balas pengurangan. Pengoksidaan berlaku pada anod, sedangkan pengurangan berlaku di katod. Oleh kerana sel galvanik (voltan) menggunakan tenaga yang dikeluarkan semasa tindak balas redoks spontan untuk menjana elektrik, sel galvanik penting sebagai sumber tenaga elektrik. Mereka menghasilkan arus langsung.
Apakah sel tumpuan?
Sel Konsentrasi adalah sejenis sel galvanik di mana kedua -dua sel sel adalah serupa dalam komposisi. Oleh itu, kita mengatakan bahawa kedua -dua sel itu bersamaan. Mereka hanya berbeza dalam kepekatan. Voltan yang dihasilkan oleh sel ini sangat kecil kerana sel ini cenderung untuk mendapatkan keadaan keseimbangan. Keseimbangan datang apabila kepekatan dua sel separuh menjadi sama.
Sel kepekatan menghasilkan elektrik melalui pengurangan tenaga bebas termodinamik sistem. Oleh kerana komposisi sel separuh adalah serupa, tindak balas yang sama berlaku, tetapi dalam arah yang bertentangan. Proses ini meningkatkan kepekatan sel kepekatan yang lebih rendah dan mengurangkan kepekatan sel kepekatan yang lebih tinggi. Apabila aliran elektrik, tenaga haba dijana. Sel menyerap tenaga ini sebagai haba. Terdapat dua jenis sel tumpuan seperti berikut:
- Sel Konsentrasi Elektrolit - Elektrod terdiri daripada bahan yang sama, dan separuh sel mengandungi elektrolit yang sama dengan kepekatan yang berbeza
- Sel Konsentrasi Elektrod - Dua elektrod (bahan yang sama) dari kepekatan yang berbeza dicelupkan dalam elektrolit yang sama
Apakah perbezaan antara sel galvanik dan sel tumpuan?
Sel galvanik adalah jenis sel elektrokimia yang menggunakan tindak balas redoks spontan untuk menjana tenaga elektrik. Sel konsentrasi, sebaliknya, adalah sejenis sel galvanik di mana kedua -dua sel sel adalah sama dalam komposisi. Oleh itu, perbezaan utama antara sel galvanik dan sel kepekatan adalah bahawa sel galvanik mungkin atau mungkin tidak mempunyai dua sel separuh dengan komposisi yang sama manakala sel kepekatan mempunyai dua setengah sel dengan komposisi yang sama.
Selain itu, elektrod sel galvanik boleh dibuat sama ada bahan yang sama atau bahan yang berbeza manakala elektrod sel kepekatan diperbuat daripada bahan yang sama dengan kepekatan yang sama atau kepekatan yang berbeza. Di samping itu, sel -sel galvanik mempunyai elektrolit yang sama atau elektrolit yang berbeza dalam dua sel separuh manakala sel kepekatan mempunyai elektrolit yang sama dengan kepekatan yang sama atau kepekatan yang berbeza.
Infographic di bawah meringkaskan perbezaan antara sel galvanik dan sel tumpuan.

Ringkasan -Sel Konsentrasi Sel Galvanik Vs
Sel galvanik adalah jenis sel elektrokimia yang menggunakan tindak balas redoks spontan untuk menjana tenaga elektrik. Sel Konsentrasi adalah sejenis sel galvanik di mana kedua -dua sel sel adalah serupa dalam komposisi. Oleh itu, perbezaan utama antara sel galvanik dan sel kepekatan adalah bahawa sel galvanik mungkin atau mungkin tidak mempunyai dua sel separuh dengan komposisi yang sama manakala sel kepekatan mempunyai dua setengah sel dengan komposisi yang sama.
Rujukan:
1. Helmenstine, Anne Marie. "Sel Elektrokimia."Thoughtco, Jan. 26, 2019, boleh didapati di sini.
Ihsan gambar:
1. "Galvanic Cell" oleh Gringer - Fail: Galvanische Zelle.PNG, oleh Tinux (CC BY-SA 3.0) melalui Commons Wikimedia