Perbezaan antara kemurungan titik beku dan ketinggian titik mendidih
Perbezaan utama - pembekuan Kemurungan titik vs ketinggian titik mendidih
Kemurungan titik beku menyebabkan penyelesaian membekukan pada suhu yang lebih rendah daripada titik pembekuan pelarut tulen kerana penambahan larut. Ketinggian titik mendidih menyebabkan penyelesaian mendidih pada suhu yang lebih tinggi daripada titik mendidih pelarut tulen kerana penambahan larut. Oleh itu, Perbezaan utama Antara kemurungan titik pembekuan dan ketinggian titik mendidih ialah The Kemurungan titik pembekuan mengurangkan titik pembekuan penyelesaian manakala ketinggian titik mendidih meningkatkan titik mendidih penyelesaian.
Kemurungan titik beku dan ketinggian titik mendidih adalah sifat colligative bahan. Ini bermakna bahawa mereka hanya bergantung pada jumlah larutan, bukan pada sifat larut.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah kemurungan titik beku
3. Apakah ketinggian titik mendidih
4. Perbandingan sampingan - Kemurungan titik beku vs ketinggian titik mendidih dalam bentuk jadual
5. Ringkasan
Apakah kemurungan titik beku?
Kemurungan titik pembekuan adalah penurunan titik pembekuan pelarut kerana penambahan larut ke dalam pelarut. Ia adalah harta colligative. Ini bermaksud kemurungan titik pembekuan hanya bergantung pada jumlah larutan, bukan pada sifat larut. Apabila kemurungan titik pembekuan telah berlaku, titik pembekuan pelarut berkurangan kepada nilai yang lebih rendah daripada pelarut tulen. Kemurungan titik pembekuan adalah sebab mengapa air laut kekal dalam keadaan cair walaupun pada 0 ° C (titik beku air tulen). Kemurungan titik pembekuan boleh diberikan seperti di bawah.
Δtf = TF (pelarut) - Tf (penyelesaian)
Atau
Δtf = Kfm
Di dalam ini,
- Δtf Adakah kemurungan titik pembekuan,
- TF (pelarut) Adakah titik pembekuan pelarut tulen
- Tf (penyelesaian) adalah titik pembekuan penyelesaian (pelarut + larutan)
- Kf Adakah kemurungan titik pembekuan tetap
- m adalah molaliti penyelesaiannya.
Walau bagaimanapun, larutan tambahan mestilah larut tidak berubah-ubah, jika tidak larut tidak mempengaruhi titik pembekuan pelarut kerana ia mendapat volatilasi dengan mudah. Bukan sahaja untuk penyelesaian, tetapi konsep ini juga boleh digunakan untuk menjelaskan perubahan dalam titik pembekuan campuran pepejal. Kompaun pepejal serbuk halus mempunyai titik pembekuan yang lebih rendah daripada sebatian pepejal tulen apabila kekotoran hadir (campuran padat pepejal).
Titik pembekuan adalah suhu di mana tekanan wap pelarut dan tekanan wap bentuk pepejal pelarut itu sama. Sekiranya larutan tidak berubah-ubah ditambah kepada pelarut ini, tekanan wap pelarut tulen berkurangan. Kemudian bentuk pepejal pelarut boleh kekal dalam keseimbangan dengan pelarut walaupun pada suhu yang lebih rendah daripada titik pembekuan biasa.
Apakah ketinggian titik mendidih?
Ketinggian titik mendidih adalah peningkatan titik mendidih pelarut kerana penambahan larut ke dalam pelarut. Di sini, titik mendidih penyelesaian (selepas penambahan larut) lebih tinggi daripada pelarut tulen. Oleh itu, suhu di mana larutan mula mendidih lebih tinggi daripada suhu biasa.

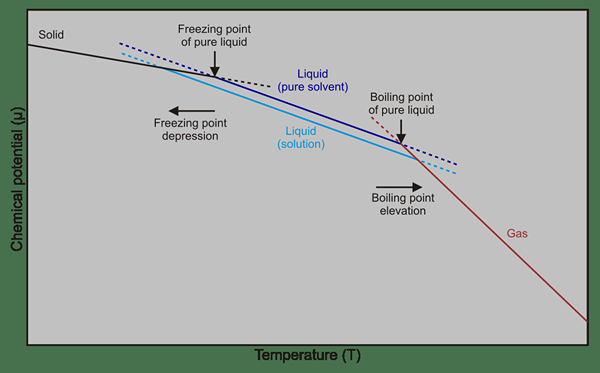
Rajah 01: Titik beku dan perbezaan titik mendidih antara pelarut dan penyelesaian tulen (pelarut + larut)
Walau bagaimanapun, larutan tambahan harus larut tidak berubah-ubah, atau lain-lain, larut akan volatilisasi dan bukannya melarutkan pelarut. Ketinggian titik mendidih juga merupakan harta koligatif sehingga hanya bergantung pada jumlah larutan (bukan pada sifat larut).
Δtb = TB (pelarut) - Tb (penyelesaian)
Atau
Δtb = Kbm
Di dalam ini,
- Δtb Adakah ketinggian titik mendidih
- TB (pelarut) Adakah titik mendidih pelarut tulen
- Tb (penyelesaian) Adakah titik mendidih penyelesaian (pelarut + larutan)
- Kb Adakah ketinggian ketinggian titik mendidih
- m adalah molaliti penyelesaiannya
Contoh umum fenomena ini adalah titik mendidih larutan garam berair. Larutan garam mendidih pada suhu yang lebih tinggi daripada 100 ° C (titik mendidih air tulen).
Apakah perbezaan antara kemurungan titik beku dan ketinggian titik mendidih?
Titik titik beku vs ketinggian titik mendidih | |
| Kemurungan titik pembekuan adalah penurunan titik pembekuan pelarut kerana penambahan larut ke dalam pelarut. | Ketinggian titik mendidih adalah peningkatan titik mendidih pelarut kerana penambahan larut ke dalam pelarut. |
| Suhu | |
| Kemurungan titik beku mengurangkan titik pembekuan penyelesaian. | Ketinggian titik mendidih meningkatkan titik mendidih penyelesaian. |
| Prinsip | |
| Kemurungan titik beku menyebabkan penyelesaian membekukan pada suhu yang lebih rendah daripada pelarut tulen. | Ketinggian titik mendidih menyebabkan penyelesaian mendidih pada suhu yang lebih tinggi daripada pelarut tulen. |
| Persamaan | |
| Kemurungan titik beku diberikan oleh ΔTf = TF (pelarut) - Tf (penyelesaian) atau Δtf = Kfm. | Ketinggian titik mendidih Δtb = TB (pelarut) - Tb (penyelesaian) atau Δtb = Kbm. |
Ringkasan -Pembekuan Kemurungan titik vs ketinggian titik mendidih
Kemurungan titik beku dan ketinggian titik mendidih adalah dua sifat colligative utama perkara. Perbezaan antara kemurungan titik pembekuan dan ketinggian titik mendidih ialah kemurungan titik pembekuan menurunkan titik pembekuan penyelesaian manakala ketinggian titik mendidih meningkatkan titik mendidih penyelesaian.
Rujukan:
1.Helmenstine, Anne Marie. "Apa ketinggian titik mendidih dan bagaimana ia berfungsi."Pemikiran. Terdapat di sini
2."Ketinggian titik mendidih."Wikipedia, Yayasan Wikimedia, 13 Mac. 2018. Terdapat di sini
3."Kemurungan titik beku."Kimia Libretexts, Libretexts, 19 Feb. 2018. Terdapat di sini
Ihsan gambar:
1.'Kemurungan titik pembekuan dan ketinggian titik mendidih'by tomas erderivative work (cc by-sa 3.0) melalui Commons Wikimedia


