Perbezaan antara pengujaan dan potensi pengionan
Perbezaan Utama - Potensi Pengionan Vs Pengionan
Potensi pengujaan dua istilah dan potensi pengionan berkaitan dengan tenaga yang diperlukan untuk memindahkan elektron, tetapi terdapat perbezaan di antara mereka berdasarkan destinasi pergerakan elektron. Dalam erti kata lain, dalam kedua -dua situasi ini, destinasi elektron selepas pergerakan itu berbeza. Dua pergerakan elektron dapat dikenal pasti dengan cara ini. Elektron boleh bergerak ke tahap tenaga yang lebih tinggi dalam atom atau molekul atau melepaskan diri dari nukleus dan bergerak dari atom. Kedua -dua proses ini memerlukan jumlah tenaga yang pasti. Elektron tidak dapat bergerak kecuali tenaga yang diperlukan tidak diserap. The Perbezaan utama antara pengujaan dan potensi pengionan ialah Potensi pengujaan adalah tenaga yang diperlukan untuk melompat dari satu tahap tenaga ke yang lain manakala Potensi pengionan adalah tenaga yang diperlukan untuk mengeluarkan elektron dari atom.
Apa itu Potensi pengujaan?
Atom mempunyai tahap tenaga yang dipanggil orbit. Elektron bergerak di sekitar nukleus di orbit ini. Elektron tidak boleh memilih orbit sewenang -wenangnya; Mereka diletakkan di orbit tertentu mengikut tahap tenaga mereka dan mereka terhad untuk bergerak atau melompat ke tahap tenaga lain kecuali mereka menyerap jumlah tenaga yang diperlukan. Bergerak dari satu orbit ke yang lain setelah menyerap jumlah tenaga yang diperlukan dipanggil pengujaan dan tenaga yang diserap untuk bergerak dari satu orbit ke yang lain dipanggil potensi pengujaan atau tenaga pengujaan. 
Apa itu Potensi pengionan?
Pengionan adalah proses mengeluarkan elektron dari shell valence. Secara umum, elektron terikat kepada nukleus melalui daya elektrostatik yang kuat. Oleh itu, tenaga diperlukan untuk mengeluarkan sepenuhnya elektron dari atom. Ini ditakrifkan sebagai mengeluarkan elektron dari atom atau molekul ke jarak tak terhingga. Tenaga yang diperlukan untuk proses ini dipanggil, "tenaga pengionan"Atau" potensi pengionan ".
Dalam erti kata lain, ia adalah perbezaan yang berpotensi antara keadaan awal, di mana elektron dibatasi ke nukleus dan keadaan akhir di mana elektron tidak lagi dilampirkan pada nukleus di mana ia berehat di tak terhingga.

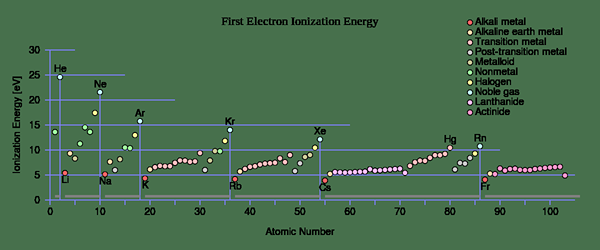
Trend berkala untuk tenaga pengionan (iaitu) vs. nombor proton
Apakah perbezaan antara potensi pengujaan dan pengionan?
Definisi Potensi Pengujaan dan Pengionan
Potensi Pengujaan:
Tenaga yang diserap oleh elektron untuk bergerak dari satu tahap tenaga ke tahap tenaga yang lebih tinggi dipanggil, "potensi pengujaan" atau tenaga pengujaan. Ini biasanya perbezaan tenaga antara keadaan awal dan akhir.
Nota: Elektron bergerak di dalam atom, tetapi dalam tahap tenaga yang berbeza.
Potensi pengionan:
Tenaga yang diperlukan untuk mengeluarkan elektron dari atom dipanggil, "potensi pengionan" atau "tenaga pengionan". Ini adalah perbezaan potensi antara dua negeri di mana elektron dibatasi ke nukleus dan elektron dikeluarkan dari atom. Tenaga apabila elektron berada pada jarak tak terhingga dianggap sebagai sifar.
Nota: Elektron dikeluarkan dari atom dan tidak ada tarikan dengan nukleus apabila dikeluarkan.
Pengiraan:
Potensi Pengujaan:
Apabila elektron melompat dari keadaan tanah (n = 1) ke tahap tenaga yang lain (n = 2) tenaga yang sepadan dipanggil 1st potensi pengujaan.
| 1st Potensi Pengujaan = Tenaga (n = 2 tahap) - Tenaga (n = 1 tahap) = -3.4 eV - (-13.6 eV) = 10.2 eV |
Apabila elektron melompat dari keadaan tanah (n = 1) ke tahap tenaga yang lain (n = 3) tenaga yang sepadan dipanggil potensi pengujaan ke -2.
| 2nd Potensi Pengujaan = Tenaga (n = 3 tahap) - Tenaga (n = 1 tahap) = -1.5 eV - (-13.6 eV) = 12.1 eV |
Potensi pengionan:
Pertimbangkan untuk mengeluarkan elektron dari tahap tenaga n = 1. Potensi pengionan adalah tenaga yang diperlukan untuk mengeluarkan elektron dari tahap n = 1 ke tak terhingga.
| Potensi pengionan = e Infinity - E (n = 1 tahap)= 0 - (-13.6 eV) = 13.6 eV |
Di atom, elektron yang paling longgar terikat dikeluarkan terlebih dahulu dan potensi pengionan secara beransur -ansur meningkat apabila ia mengionkan.
Ihsan gambar:
"Potensi pengujaan yang bermakna "oleh HPAUL - Kerja Sendiri. (Domain Awam) melalui Wikimedia Commons
"Tenaga Pengionan Pertama" oleh Pengguna: Sponk (CC BY-SA 3.0) Melalui Commons


