Perbezaan antara entalpi dan entropi
The Perbezaan utama antara entalpi dan entropi adalah bahawa Entalpi adalah pemindahan haba yang berlaku dalam tekanan yang berterusan manakala entropi memberikan idea tentang kekangan sistem.
Untuk tujuan kajian dalam bidang kimia, kita membahagikan alam semesta menjadi dua sebagai sistem dan sekitarnya. Pada bila -bila masa, bahagian yang akan kita pelajari adalah sistem, dan selebihnya adalah sekitar. Entalpi dan entropi adalah dua istilah yang menerangkan reaksi yang berlaku dalam sistem dan sekitarnya. Kedua -dua entalpi dan entropi adalah fungsi keadaan termodinamik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu entalpi
3. Apa itu entropi
4. Perbandingan sampingan - entalpi vs entropi dalam bentuk jadual
5. Ringkasan
Apa itu entalpi?
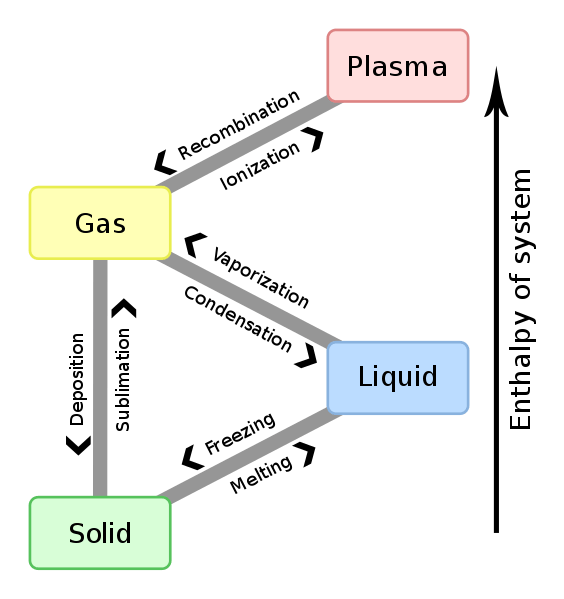
Apabila tindak balas berlaku, ia boleh menyerap atau mengembangkan haba, dan jika kita menjalankan tindak balas pada tekanan tetap, kita menyebutnya entalpi reaksi. Walau bagaimanapun, kita tidak dapat mengukur entalpi molekul. Oleh itu, kita perlu mengukur perubahan entalpi semasa reaksi. Kita boleh mendapatkan perubahan entalpi (ΔH) untuk tindak balas dalam suhu dan tekanan yang diberikan dengan menolak entalpi reaktan dari entalpi produk. Sekiranya nilai ini negatif, maka tindak balasnya adalah eksotermik. Sekiranya nilai positif, maka tindak balasnya adalah endotermik.

Rajah 01: Hubungan antara perubahan entalpi dan perubahan fasa
Perubahan entalpi antara mana -mana pasangan reaktan dan produk adalah bebas dari jalan di antara mereka. Selain itu, perubahan entalpi bergantung pada fasa reaktan. Sebagai contoh, apabila gas oksigen dan hidrogen bertindak balas untuk menghasilkan wap air, perubahan entalpi ialah -483.7 kJ. Walau bagaimanapun, apabila reaktan yang sama bertindak balas untuk menghasilkan air cair, perubahan entalpi ialah -571.5 kJ.
2h2 (g) +o2 (g) → 2h2O (g); ΔH = -483.7 kJ
2h2 (g) +o2 (g) → 2h2O (l); ΔH = -571.7 kJ
Apa itu entropi?
Beberapa perkara berlaku secara spontan, yang lain tidak. Sebagai contoh, haba akan mengalir dari badan panas ke yang lebih sejuk, tetapi kita tidak dapat melihat sebaliknya walaupun ia tidak melanggar pemuliharaan peraturan tenaga. Apabila perubahan berlaku, jumlah tenaga kekal malar tetapi dibuang secara berbeza. Kita dapat menentukan arah perubahan dengan pengagihan tenaga. Perubahan adalah spontan jika ia membawa kepada rawak dan kekacauan yang lebih besar di alam semesta secara keseluruhan. Kita boleh mengukur tahap kekacauan, rawak, atau penyebaran tenaga oleh fungsi negara; Kami namakannya sebagai entropi.
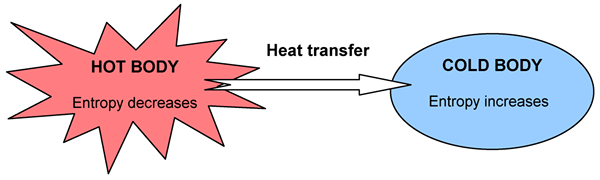
Rajah 02: Rajah yang menunjukkan perubahan entropi dengan pemindahan haba
Undang -undang termodinamik kedua berkaitan dengan entropi, dan ia berkata, "Entropi alam semesta meningkat dalam proses spontan."Entropi dan jumlah haba yang dihasilkan saling berkaitan dengan sejauh mana sistem menggunakan tenaga. Malah, jumlah perubahan entropi atau gangguan tambahan yang disebabkan oleh jumlah haba Q bergantung pada suhu. Sekiranya sudah sangat panas, sedikit haba tambahan tidak menimbulkan lebih banyak gangguan, tetapi jika suhu sangat rendah, jumlah haba yang sama akan menyebabkan peningkatan dramatik dalam gangguan. Oleh itu, kita boleh menulisnya seperti berikut: (di mana ds diubah dalam entropi, dq diubah dalam haba dan T adalah suhu.
ds = dq/t
Apakah perbezaan antara entalpi dan entropi?
Entalpi dan entropi adalah dua istilah yang berkaitan dalam termodinamik. Perbezaan utama antara entalpi dan entropi ialah entalpi adalah pemindahan haba berlaku dalam tekanan malar manakala entropi memberikan idea tentang rawak sistem. Selain itu, entalpi berkaitan dengan undang -undang termodinamik pertama manakala entropi berkaitan dengan undang -undang termodinamik kedua. Satu lagi perbezaan penting antara entalpi dan entropi ialah kita boleh menggunakan entalpi untuk mengukur perubahan tenaga sistem selepas tindak balas sedangkan kita boleh menggunakan entropi untuk mengukur tahap gangguan sistem selepas reaksi.
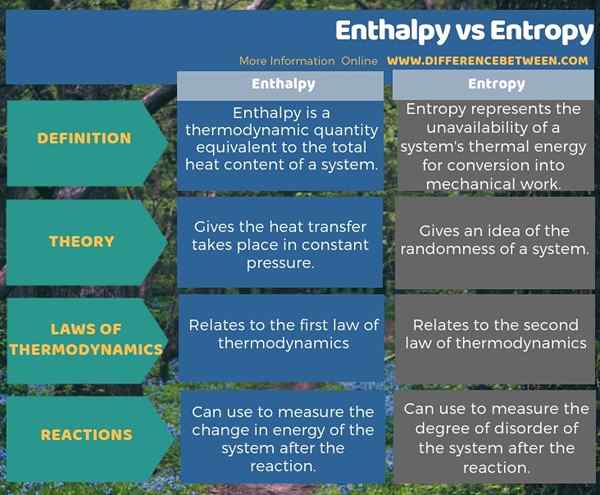
Ringkasan -Entropi entalpi vs
Entalpi dan entropi adalah istilah termodinamik yang sering kita gunakan dengan tindak balas kimia. Perbezaan utama antara entalpi dan entropi ialah entalpi adalah pemindahan haba berlaku dalam tekanan malar manakala entropi memberikan idea tentang rawak sistem.
Rujukan:
1. Libretexts. "Enthalpy."Kimia Libretexts, Yayasan Sains Kebangsaan, 26 Nov. 2018. Terdapat di sini
2. Drake, Gordon W.F. "Entropi."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 7 Jun 2018. Terdapat di sini
Ihsan gambar:
1."Perubahan Fasa - en" oleh F L A N K E R, Penubag - Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2."Entropy Hot to Cold" oleh Ibrahim Dincer dan Yunus A. Cengel - Entropi 2001, 3 (3), 116-149; doi: 10.3390/e3030116 http: // www.MDPI.com/1099-4300/3/3/116, (CC oleh 3.0) melalui Commons Wikimedia


