Perbezaan antara potensi elektrod dan potensi sel
The Perbezaan utama antara potensi elektrod dan potensi sel ialah Potensi elektrod merujuk kepada keupayaan elektrod dalam sel untuk dikurangkan atau teroksida manakala potensi sel adalah perbezaan antara potensi elektrod elektrod yang terdapat dalam sel elektrokimia.
Potensi elektrod dan potensi sel adalah istilah yang menjelaskan daya elektromotif sel elektrokimia. Potensi elektrod memberikan potensi voltan elektrod tunggal manakala potensi sel menganggap potensi elektrod kedua -dua elektrod.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah potensi elektrod
3. Apa itu Potensi Sel
4. Perbandingan sampingan - potensi elektrod vs potensi sel dalam bentuk jadual
5. Ringkasan
Apakah potensi elektrod?
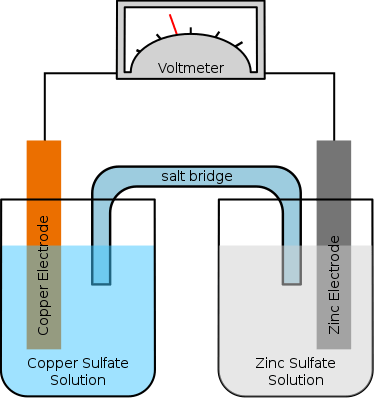
Potensi elektrod adalah kecenderungan elektrod dalam sel elektrokimia untuk dikurangkan atau teroksida. Ia adalah daya elektromotif sel. Terdapat tiga faktor yang mempengaruhi nilai potensi elektrod: sifat elektrod, kepekatan ion dalam larutan dan suhu elektrolitik. Bagi mana -mana sel elektrokimia, jumlah potensi adalah jumlah potensi elektrod kedua -dua elektrod. Kita boleh menunjukkan potensi elektrod sebagai e. Walau bagaimanapun, kita tidak dapat mengukur potensi elektrod secara berasingan. Ia mesti diukur dalam tindak balas dengan beberapa elektrod lain.

Rajah 01: Sel elektrokimia mudah
Selain itu, potensi elektrod bergantung kepada kepekatan elektrod, suhu sel elektrokimia, dan juga tekanan (jika sel mengandungi elektrod gas). Umumnya, potensi elektrod diukur dengan elektrod standard.
Elektrod standard biasa ialah elektrod hidrogen dan potensi elektrodnya diambil sebagai sifar. Di samping itu, kita mesti menggunakan syarat termodinamik standard agar apabila mengukur potensi; Jika tidak, kita tidak boleh mendapatkan nilai potensi yang tepat kerana potensi elektrod bergantung pada suhu, tekanan, dan lain -lain. Di sini, keadaan termodinamik standard termasuk mengukur terhadap elektrod hidrogen, larutan elektrolitik yang mempunyai kepekatan 1 mol/L, tekanan 1 atm, dan suhu 25 ° C.
Apa itu Potensi Sel?
Potensi sel merujuk kepada jumlah potensi voltan sel elektrokimia yang mempunyai dua elektrod. Di sini, sel-sel elektrokimia harus mempunyai dua reaksi separuh berasingan yang berlaku selari antara satu sama lain dan kemudian, potensi sel adalah seperti berikut:
Esel = Potensi pengoksidaan+ potensi pengurangan
Oleh itu, potensi sel adalah jumlah potensi elektrod katod dan potensi elektrod anod. Sel voltan sebenar berbeza dari keadaan standard. Oleh itu, kita perlu menyesuaikan nilai eksperimen untuk mendapatkan nilai standard. Ia adalah seperti berikut:
Esel = E0sel - (RT/NF) LNQ
Di mana esel adalah potensi sel eksperimen, e0sel adalah potensi sel standard, r adalah pemalar sejagat, T adalah suhu, n adalah tahi lalat elektron yang ditukar dalam separuh tindak balas, f adalah pemalar faraday dan q adalah reaksi termodinamik.
Apakah perbezaan antara potensi elektrod dan potensi sel?
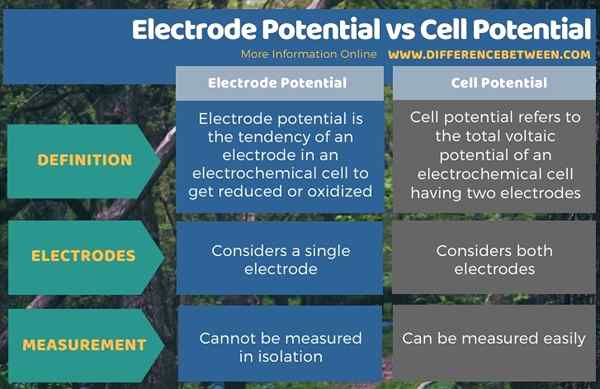
Perbezaan utama antara potensi elektrod dan potensi sel ialah potensi elektrod merujuk kepada keupayaan elektrod dalam sel untuk dikurangkan atau teroksida manakala potensi sel adalah perbezaan antara potensi elektrod elektrod yang terdapat dalam sel elektrokimia. Oleh itu, potensi elektrod memberikan potensi voltan elektrod tunggal manakala potensi sel menganggap kedua -dua elektrod.
Selain itu, satu lagi perbezaan yang signifikan antara potensi elektrod dan potensi sel adalah mustahil untuk mengukur potensi elektrod kerana ia adalah nilai relatif, tetapi potensi sel dapat diukur dengan mudah kerana kita perlu mencari perbezaan potensi elektrod, yang merupakan nilai relatif.
Ringkasan -potensi elektrod vs potensi sel
Potensi elektrod dan potensi sel dibincangkan di bawah elektrokimia, mengenai sel elektrokimia. Perbezaan utama antara potensi elektrod dan potensi sel ialah potensi elektrod merujuk kepada keupayaan elektrod dalam sel untuk dikurangkan atau teroksida manakala potensi sel adalah perbezaan antara potensi elektrod elektrod yang terdapat dalam sel elektrokimia.
Rujukan:
1. "Potensi elektrod standard." Hyperphysics, Terdapat di sini.
Ihsan gambar:
1. "Galvanic Cell" oleh Gringer - Fail: Galvanische Zelle.PNG, oleh Tinux (CC BY-SA 3.0) melalui Commons Wikimedia