Perbezaan antara stoikiometri komposisi dan tindak balas
The Perbezaan utama Antara komposisi dan stoikiometri reaksi ialah Stoikiometri komposisi merujuk kepada pembuatan atom dari sebatian kimia, sedangkan stoikiometri reaksi merujuk kepada jumlah sebatian yang digunakan atau dihasilkan semasa reaksi kimia.
Stoikiometri adalah istilah kimia yang menggambarkan data kuantitatif mengenai sebatian kimia atau tindak balas kimia. Jika data ini adalah mengenai sebatian kimia, maka kami menyebutnya stoikiometri komposisi; Sekiranya ia mengenai tindak balas kimia, kita boleh menyebutnya reaksi stoikiometri.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah stoikiometri komposisi
3. Apakah stoikiometri reaksi
4. Perbandingan sampingan - Komposisi vs stoikiometri reaksi dalam bentuk jadual
5. Ringkasan
Apakah stoikiometri komposisi?
Stoikiometri komposisi adalah analisis kuantitatif sebatian kimia mengenai komposisi atomnya. Istilah ini merujuk kepada jenis atom dan bilangannya yang terdapat dalam sebatian kimia tertentu. Kita dapat menentukan ini menggunakan formula kimia kompaun. Atomicity of a molekul memberikan jumlah atom yang terdapat dalam sebatian kimia. Tetapi ia tidak memberi sebarang perincian mengenai unsur -unsur kimia yang mana atom -atom kompaun itu milik dan nombor mereka. Walau bagaimanapun, kita boleh menggunakan stoikiometri komposisi sebatian tertentu untuk meramalkan formula kimia. Oleh itu, stoikiometri komposisi hanyalah pembuatan kimia spesies kimia.
Sebagai contoh, stoikiometri komposisi molekul glukosa diberikan sebagai enam atom karbon, dua belas atom hidrogen dan enam atom oksigen. Oleh itu, kita dapat menentukan bahawa satu molekul glukosa mengandungi atom karbon, hidrogen dan oksigen dalam nisbah 6: 12: 6. Ini adalah stoikiometri komposisi glukosa.
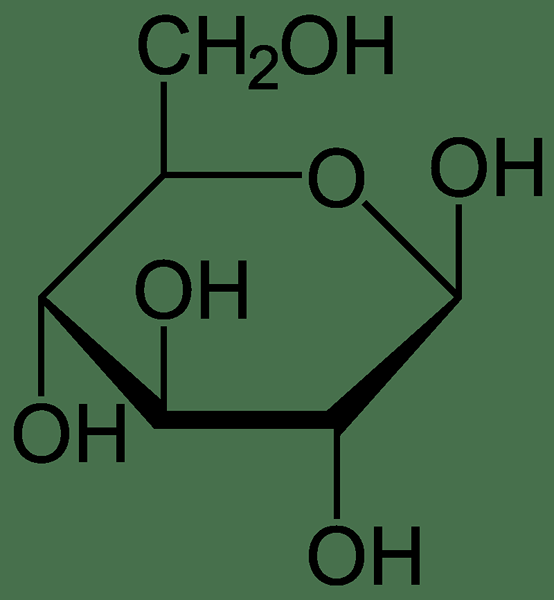
Rajah 01: Komposisi kimia molekul glukosa
Terdapat cara yang berbeza untuk menentukan stoikiometri komposisi sebatian yang tidak diketahui. Sampel sebatian yang tidak diketahui boleh digunakan untuk menentukan jenis elemen kimia dalam sampel itu bersama -sama dengan jisim setiap elemen. Kemudian bilangan tahi lalat setiap elemen setiap sampel dapat dikira menggunakan massa ini. Nilai molar boleh dibundarkan untuk mendapatkan nisbah yang paling mungkin antara pelbagai jenis atom dalam sampel untuk meramalkan formula molekul.
Apakah stoikiometri reaksi?
Stoikiometri tindak balas adalah nisbah antara reaktan dan produk tindak balas kimia tertentu. Fenomena ini sangat penting dalam mengimbangi tindak balas kimia untuk mendapatkan hubungan antara reaktan dan berapa banyak produk yang kita dapat dari bertindak balas dari spesies tersebut.

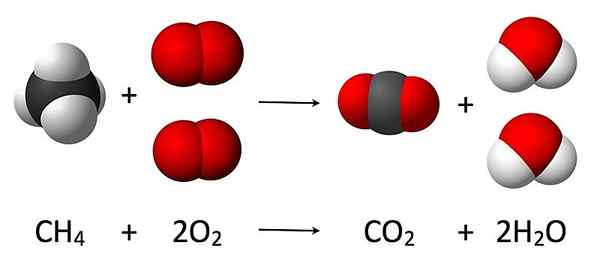
Rajah 02: Contoh untuk stoikiometri tindak balas
Konsep reaksi stoikiometri adalah berdasarkan kepada undang -undang pemuliharaan massa, yang menunjukkan bahawa jumlah jisim reaktan harus sama dengan jumlah jisim produk kerana jisim tidak dapat dicipta atau dimusnahkan, hanya dapat ditukar menjadi bentuk lain, seperti tenaga.
Marilah kita mempertimbangkan contoh untuk memahami teori di sebalik reaksi stoikiometri. Reaksi antara logam dan air alkali menghasilkan tenaga haba, hidroksida logam, dan gas hidrogen. Di sini, butiran yang kita tahu adalah jisim logam alkali yang digunakan dan jumlah air yang digunakan untuk reaksi. Setelah selesai reaksi, jumlah gas hidrogen dapat dikumpulkan dan menggunakan jumlahnya, tahi lalat gas hidrogen berkembang dapat dikira. Oleh itu, dengan mengandaikan bahawa semua logam alkali bertindak balas dengan air, kita boleh mendapatkan nisbah antara reaktan dan produk yang terlibat dalam reaksi ini. Ini adalah reaksi stoikiometri logam alkali dalam reaksi air.
Apakah perbezaan antara komposisi dan stoikiometri tindak balas?
Perbezaan utama antara komposisi dan reaksi stoikiometri ialah stoikiometri komposisi merujuk kepada make-up atom sebatian kimia, sedangkan stoikiometri reaksi merujuk kepada jumlah sebatian yang digunakan atau dihasilkan semasa tindak balas kimia. Walaupun stoikiometri komposisi memberikan nisbah antara atom setiap elemen kimia yang terdapat dalam sebatian, stoikiometri reaksi memberikan nisbah antara reaktan dan produk yang terlibat dalam tindak balas tertentu.
Di bawah infographic meringkaskan perbezaan antara komposisi dan reaksi stoikiometri.

Ringkasan -Komposisi vs stoikiometri reaksi
Stoikiometri adalah kaedah analisis kuantitatif sebatian kimia atau tindak balas kimia. Perbezaan utama antara komposisi dan reaksi stoikiometri ialah stoikiometri komposisi merujuk kepada make-up atom sebatian kimia, sedangkan stoikiometri reaksi merujuk kepada jumlah sebatian yang digunakan atau dihasilkan semasa tindak balas kimia.
Rujukan:
1. "Reaksi stoikiometri dan mengimbangi." Kimia Libreetexts, Libretexts, 25 Sept. 2019, boleh didapati di sini.
Ihsan gambar:
1. "Beta-D-Glucopyranose" oleh Neurotiker-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia
2. "Reaksi Pembakaran Metana" oleh Jyntorobert a. Rohdejacek Fhjynto - (Domain Awam) melalui Commons Wikimedia


