Perbezaan antara bromin dan klorin

The Perbezaan utama antara bromin dan klorin adalah Bromin kurang reaktif daripada klorin.
Halogen adalah elemen kumpulan VII dalam jadual berkala. Semua elemen ini adalah elemen elektronegatif dan mempunyai keupayaan untuk menghasilkan -1 anion. Ahli -ahli kumpulan ini termasuk fluorin, klorin, bromin, iodin dan astatin.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu Bromine
3. Apa itu klorin
4. Perbandingan sampingan - Bromine vs klorin dalam bentuk jadual
5. Ringkasan
Apa itu Bromine?
Bromin dilambangkan oleh simbol Br. Ini ada di 4th Tempoh jadual berkala antara halogen klorin dan iodin. Konfigurasi elektronnya ialah [AR] 4S2 3d10 4p5. Tambahan pula, bilangan atom bromin adalah 35. Jisim atomnya adalah 79.904. Bromin kekal sebagai cecair warna merah coklat pada suhu bilik. Ia wujud sebagai molekul diatom, BR2. Selain itu, ia adalah toksik, mengakis dan mempunyai bau yang kuat.
Kereaktifan kimia bromin terletak di antara klorin dan iodin. Bromin kurang reaktif daripada klorin tetapi lebih reaktif daripada yodium. Ia menghasilkan ion bromida dengan mengambil satu elektron. Oleh itu, ia mengambil bahagian dalam pembentukan kompaun ionik dengan mudah. Sebenarnya, dalam alam semula jadi, bromin wujud sebagai garam bromida dan bukannya Br2. Terdapat dua isotop bromin yang stabil. 79BR (50.69%) dan 81BR (49.31%) Adakah isotop itu.

Rajah 01: Sampel bromin
Bromin sedikit larut dalam air tetapi larut dalam pelarut organik seperti kloroform. Ia boleh dihasilkan dengan merawat brin kaya bromida dengan gas klorin, atau gas bromin lain boleh dihasilkan dengan merawat HBR dengan asid sulfurik. Selanjutnya, ia sangat penting dalam industri dan makmal kimia. Sebatian bromida berguna sebagai bahan tambahan petrol dan untuk racun perosak.
Apa itu klorin?
Klorin adalah elemen dalam jadual berkala yang kami nyatakan oleh Cl. Ia adalah halogen (17th kumpulan) dalam 3Rd Tempoh jadual berkala. Bilangan atom klorin ialah 17; Oleh itu, ia mempunyai tujuh belas proton dan tujuh belas elektron. Konfigurasi elektronnya ialah 1s2 2s2 2p6 3s2 3p5. Sejak p Sublevel sepatutnya mempunyai 6 elektron untuk mendapatkan konfigurasi elektron gas argon mulia, klorin mempunyai keupayaan untuk menarik elektron.

Rajah 02: Contoh klorin
Klorin mempunyai elektronegativiti yang sangat tinggi, iaitu kira -kira 3, menurut skala Pauling. Selain itu, berat atom klorin adalah 35.453 amu. Di bawah suhu bilik, ia wujud sebagai molekul diatomik (CL2). Cl2 adalah gas warna kuning-hijau.
Klorin mempunyai titik lebur sebanyak -101.5 ° C dan titik mendidih -34.04 ° C. Di antara semua isotop klorin, CL-35 dan CL-37 adalah isotop yang paling stabil. Apabila gas klorin larut di dalam air, ia membentuk asid hidroklorik dan asid hypochlorous, yang sangat berasid.
Klorin mempunyai semua nombor pengoksidaan yang berbeza -beza dari -1 hingga +7. Selanjutnya, ia adalah gas yang sangat reaktif. Ia boleh melepaskan bromin dan iodin dari garam bromida dan iodida. Oleh itu, ia mempunyai keupayaan untuk mengoksida anion unsur -unsur yang terletak di bawah klorin dalam jadual berkala. Walau bagaimanapun, ia tidak dapat mengoksidakan fluorida untuk memberikan fluorin. Klorin terutamanya dihasilkan oleh elektrolisis penyelesaian natrium klorida. Kemudian di anod, kita boleh mengumpul gas klorin. Klorin terutamanya penting sebagai pembasmi kuman dalam pembersihan air. Selanjutnya, berguna dalam menghasilkan pelbagai produk pengguna seperti makanan, racun serangga, cat, produk petroleum, plastik, ubat, tekstil, pelarut.
Apakah perbezaan antara bromin dan klorin?
Bromin adalah elemen kimia yang mempunyai nombor atom 35 dan simbol BR manakala klorin adalah elemen kimia yang mempunyai nombor atom 17 dan simbol cl. Perbezaan utama antara bromin dan klorin ialah bromin kurang reaktif daripada klorin.
Selain itu, jisim atom bromin dan klorin adalah 79.904 amu dan 35.453 amu, masing -masing. Juga, perbezaan selanjutnya antara bromin dan klorin adalah bahawa bromin berlaku sebagai cecair warna merah coklat pada suhu bilik, manakala klorin berlaku sebagai gas warna kuning-hijau.
Berikut adalah ringkasan perbezaan antara bromin dan klorin dalam bentuk jadual.
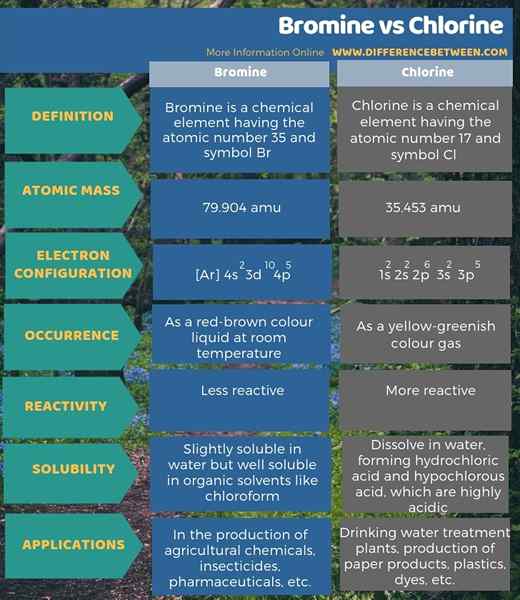
Ringkasan -Bromine vs klorin
Bromin adalah elemen kimia yang mempunyai nombor atom 35 dan simbol br. Klorin adalah elemen kimia yang mempunyai nombor atom 17 dan simbol cl. Ringkasnya, perbezaan utama antara bromin dan klorin ialah bromin kurang reaktif daripada klorin.
Rujukan:
1. "Bromine - Maklumat Unsur, Hartanah dan Kegunaan | Jadual berkala."Royal Society of Chemistry - Memajukan Kecemerlangan dalam Sains Kimia, yang terdapat di sini.
Ihsan gambar:
1. "Bromine -Ampoule" oleh Jurii - (CC oleh 3.0) melalui Commons Wikimedia
2. "Sampel Klorin" oleh Benjah-Bmm27-Kerja Sendiri (Domain Awam) melalui Commons Wikimedia


