Perbezaan antara asid binari dan ternary
Perbezaan Utama -Asid Ternary Binary Vs
Asid adalah sebatian yang mampu menderma ion hidrogen (h+) atau membentuk ikatan kovalen dengan pasangan elektron (asid Lewis). Asid mempunyai banyak ciri ciri seperti keupayaan untuk menjadikan litmus biru menjadi warna merah, meneutralkan penyelesaian alkali, dll. Sebilangan besar asid menghakis pada kepekatan yang rendah. Oleh itu, penjagaan harus diambil ketika bekerja dengan asid. Asid binari dan ternary adalah dua bentuk asid. The Perbezaan utama Antara asid binari dan ternary ialah Asid binari adalah sebatian kimia yang terdiri daripada hidrogen sebagai komponen penting yang terikat kepada nonmetal manakala asid ternary adalah sebatian asid yang mengandungi atom hidrogen dan oksigen yang terikat kepada elemen lain, kebanyakan masa, bukan logam.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah asid binari
3. Apakah asid ternary
4. Persamaan antara asid binari dan ternary
5. Perbandingan sampingan - binari vs asid ternary dalam bentuk jadual
6. Ringkasan
Apakah asid binari
Asid binari adalah sebatian berasid yang selalu mempunyai hidrogen yang dibebankan kepada unsur -unsur kimia lain, kebanyakan masa bukan metal. Ia dipanggil "binari" kerana ia mempunyai dua elemen yang berbeza digabungkan antara satu sama lain. Oleh kerana hidrogen hadir sebagai komponen penting, asid binari juga dipanggil hidracid. Asid binari adalah sebatian kovalen yang bertindak sebagai asid dalam medium berair.
Logam lain yang digabungkan dengan atom hidrogen di sini adalah elemen blok p. Walaupun asid ini hanya terdiri daripada dua elemen yang berbeza, mereka tidak pada dasarnya diatom. Sebatian diatomik adalah molekul yang terdiri daripada dua atom. Asid binari boleh diatomik atau boleh ada lebih daripada dua atom per molekul.
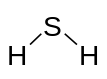
Rajah 01: H2S adalah asid binari
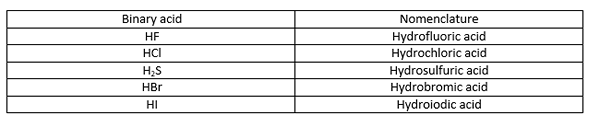
Asid binari mengandungi ion hidrogen (h+) sebagai satu -satunya kation. Oleh itu, ketika menamakan asid binari, komponen berikut harus berada di sana.
- Awalan 'hidro-'
- Nama akar anion
- Akhiran '-ic' diikuti oleh asid perkataan
Mari kita pertimbangkan beberapa contoh asid binari.
Apakah asid ternary?
Asid ternary adalah sebatian berasid yang mengandungi hidrogen dan oksigen digabungkan dengan elemen lain. Elemen kimia yang lain adalah kebanyakan masa, bukan logam. Ia adalah sebatian yang terdiri daripada ion hidrogen (h+) terikat pada anion polyatomik. Walau bagaimanapun, ion hidrogen adalah satu -satunya kation yang terdapat dalam asid ternary.
Asid ternary sering dikenali sebagai "Oxyacids". Itu kerana ini adalah oksigen mengandungi sebatian yang mempunyai keupayaan untuk melepaskan ion hidrogen (h+) ke medium berair yang dibubarkan. Oleh itu, formula umum untuk asid ternary ialah "H-O-X".
Untuk menjadi asid, sebatian ini harus mendermakan ion hidrogen dengan memecahkan ikatan antara atom hidrogen dan atom oksigen (-O-H). Untuk ini berlaku, yang tidak terikat kepada oksigen (x) harus sangat elektronegatif. Kemudian, elektron sangat tertarik dengan non -logam ini, dan akibatnya, ikatan antara oksigen dan hidrogen melemahkan.

Rajah 02: Asid sulfurik adalah asid ternary
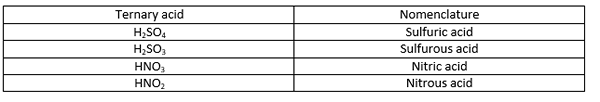
Apabila menamakan asid ternary, akhiran nama anion diubah (berdasarkan keadaan pengoksidaan nonmetal) diikuti dengan perkataan "asid". Berikut adalah beberapa contoh.
Apakah persamaan antara asid binari dan ternary?
- Kedua -dua asid binari dan ternary adalah bentuk asid.
- Kedua -dua asid binari dan ternary mampu menderma ion hidrogen.
- Kedua -dua asid binari dan ternary terdiri daripada atom hidrogen.
Apakah perbezaan antara asid binari dan ternary?
Binari vs asid ternary | |
| Asid binari adalah sebatian berasid yang selalu mempunyai hidrogen yang dibebankan kepada unsur -unsur kimia lain, kebanyakan masa bukan metal. | Asid ternary adalah sebatian berasid yang mengandungi hidrogen dan oksigen digabungkan dengan elemen lain. |
| Komponen | |
| Asid binari mempunyai satu dua jenis elemen kimia (hidrogen terikat dengan nonmetal). | Asid ternary mempunyai lebih daripada dua jenis elemen kimia (hidrogen, oksigen dan bukan logam). |
| Oksigen | |
| Asid binari tidak mempunyai atom oksigen. | Asid ternary pada dasarnya mengandungi atom oksigen. |
| Formula Umum | |
| Asid binari mempunyai formula umum H-X. | Asid ternary mempunyai formula umum h-o-x. |
Ringkasan -Binari vs asid ternary
Asid binari adalah sebatian yang mempunyai formula umum h-x. Asid ternary adalah sebatian berasid yang mempunyai formula umum h-o-x. Perbezaan antara asid binari dan ternary ialah asid binari adalah sebatian kimia yang terdiri daripada hidrogen sebagai komponen penting yang terikat kepada nonmetal manakala asid ternary adalah sebatian asid yang mengandungi atom hidrogen dan oksigen yang terikat kepada elemen lain, kebanyakan masa, bukan metal.
Rujukan:
1."Asid binari."Wikipedia, Yayasan Wikimedia, 22 Jan. 2018. Terdapat di sini
2.Stanley Smith, et al. Asas Kimia,Seksyen 6.2: Penamaan sebatian. 2000.Terdapat di sini
3."Asid binari dan ternary."Kimia Umum untuk Profesion Penjagaan Kesihatan. Terdapat di sini
Ihsan gambar:
1.'Hydrogen sulfide'by Bangin - Kerja sendiri, (CC oleh 2.5) Melalui Wikimedia Commons
2.'Sulfurik-asid-2d' (domain awam) melalui Wikimedia Commons


