Perbezaan antara campuran azeotropik dan zeotropik
The Perbezaan utama antara campuran azeotropik dan zeotropik ialah titik embun dan titik gelembung campuran azeotropik bersilang manakala titik embun dan titik gelembung campuran zeotropik dibezakan.
Istilah campuran azeotropik dan zeotropik sangat berkaitan antara satu sama lain kerana mereka mempunyai sifat bertentangan antara satu sama lain. Oleh itu, mereka mempunyai ciri -ciri lengkung embun dan gelembung yang berbeza juga. Lengkung embun dan gelembung ini ditarik dalam graf komposisi suhu.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah campuran azeotropik
3. Apakah campuran zeotropik
4. Perbandingan sampingan - campuran azeotropik vs zeotropik dalam bentuk jadual
5. Ringkasan
Apakah campuran azeotropik?
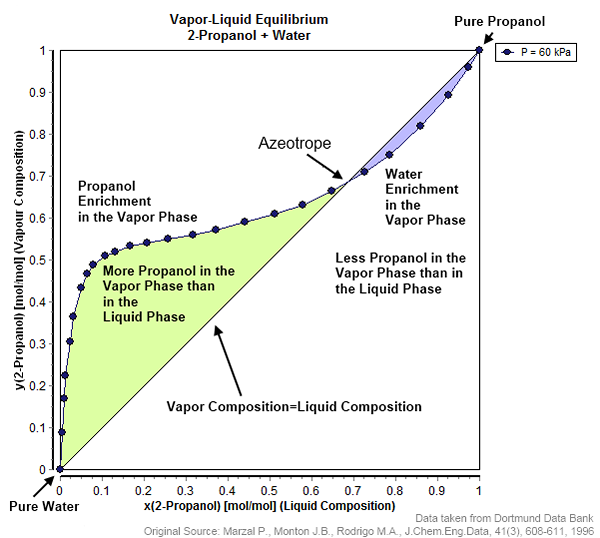
Campuran azeotropik adalah campuran kimia di mana terdapat cecair yang mempunyai titik mendidih yang tetap. Ini kerana wap campuran cecair mempunyai komposisi yang sama dengan campuran cecair. Titik mendidih campuran ini boleh lebih tinggi atau lebih rendah daripada mana -mana komponen individu campuran.

Rajah 01: Keseimbangan vapour-cecair 2-propanol dan air yang menunjukkan tingkah laku azeotropik
Oleh kerana titik mendidih campuran azeotropik tetap, kita tidak boleh menggunakan penyulingan mudah untuk pemisahan komponen dalam campuran ini. Oleh itu, kita perlu menggunakan beberapa teknik lain seperti menggunakan dua lajur penyulingan dengan tahap pemisahan yang berbeza atau penambahan sebatian ketiga ke campuran azeotropik untuk mengubah turun naik dan mendidih titik komponen.
Apakah campuran zeotropik?
Campuran zeotropik adalah campuran komponen cecair yang mempunyai titik mendidih yang berbeza. Oleh kerana ia bertentangan dengan campuran azeotropik, kita boleh menyebutnya campuran bukan gabungan. Oleh kerana perbezaan dalam titik mendidih mereka, komponen individu tidak menjalani penyejatan atau pemeluwapan pada suhu yang sama. Oleh itu, campuran dalam suhu meluncur. Perubahan fasa komponen cecair berlaku dalam satu siri suhu dan bukan pada suhu yang sama.
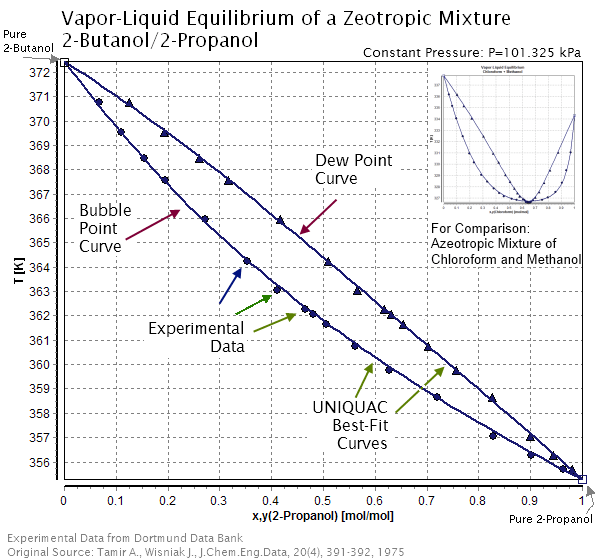
Rajah 02: Graf komposisi suhu untuk campuran zeotropik
Sekiranya kita melukis suhu vs. Grafik komposisi untuk campuran zeotropik, kita dapat melihat suhu mendidih komponen antara titik gelembung dan titik embun. Titik gelembung adalah suhu di mana gelembung pertama bentuk wap. Titik embun adalah suhu di mana pemeluwapan berlaku. Suhu vs. Grafik komposisi menunjukkan bagaimana komposisi cecair dan wap berubah apabila mendidih, pemeluwapan dan suhu di antara mereka. Contoh campuran zeotropik adalah campuran etana, metana, nitrogen, propana dan isobutene.
Apakah perbezaan antara campuran azeotropik dan zeotropik?
Azeotropic dan zeotropik adalah istilah yang bertentangan. Perbezaan utama antara campuran azeotropik dan zeotropik ialah titik embun dan titik gelembung campuran azeotropic bersilang, sedangkan titik embun dan titik gelembung campuran zeotropik dibezakan. Maksudnya, kita dapat melihat dua mata dengan jelas sebagai titik gelembung dan titik embun dalam graf suhu vs. Komposisi dalam campuran zeotropik, tetapi untuk campuran azeotropik, titik -titik ini terletak di antara satu sama lain.
Berikut adalah ringkasan perbezaan antara campuran azeotropik dan zeotropik.

Ringkasan -campuran zeotropik azeotropik vs
Istilah azeotropik dan zeotropik bertentangan antara satu sama lain. Perbezaan utama antara campuran azeotropik dan zeotropik ialah titik embun dan titik gelembung campuran azeotropic bersilang, sedangkan titik embun dan titik gelembung campuran zeotropik dibezakan.
Rujukan:
1. "Azeotrope."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 19 Feb. 2020, boleh didapati di sini.
2. "Campuran Zeotropik."Wikipedia, Yayasan Wikimedia, 15 Okt. 2019, boleh didapati di sini.
3. "Apa itu azeotrope?"Kitar semula pelarut dan azeotropes, tersedia di sini.
Ihsan gambar:
1. "Vleisoropanolwaterazeotrope" oleh Wilfriedc - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia
2. "VLE of A Zeotropic Campuran" oleh Wilfriedc - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia


