Perbezaan antara ampholyte dan amphoterik
The Perbezaan utama Antara ampholyte dan amphoterik adalah bahawa Istilah amphoterik bermaksud keupayaan molekul untuk bertindak sebagai asid atau asas manakala ampholyte adalah molekul, iaitu amphoterik.
Kami menjumpai molekul, yang kami mengkategorikan sebagai asas, berasid atau neutral. Penyelesaian asas menunjukkan nilai pH lebih tinggi daripada 7 dan penyelesaian berasid menunjukkan nilai pH, yang lebih rendah daripada 7. Penyelesaian yang mempunyai nilai pH 7 adalah penyelesaian neutral. Terdapat beberapa molekul, yang berbeza dari pengkategorian biasa ini. Ampholytes adalah salah satu molekul. Mereka mempunyai sifat kimia berasid dan asas.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu ampholyte
3. Apa itu amphoterik
4. Perbandingan sampingan - Ampholyte vs amphoterik dalam bentuk jadual
5. Ringkasan
Apa itu ampholyte?
Ampholyte adalah molekul yang mempunyai kumpulan asas dan berasid. Contoh umum yang terbaik dan paling meluas untuk ampholyte adalah asid amino. Kami tahu bahawa semua asid amino mempunyai -cooh, -nh2 kumpulan dan a -h terikat kepada karbon. Kumpulan karboksilik (-COOH) bertindak sebagai kumpulan berasid dalam asid amino, dan amina (-NH2) kumpulan bertindak sebagai kumpulan asas. Selain daripada ini, terdapat kumpulan -r dalam setiap asid amino. Kumpulan R berbeza dari satu asid amino ke yang lain. Asid amino yang paling mudah dengan kumpulan r ialah h adalah glisin.
Walau bagaimanapun, kumpulan R dalam beberapa asid amino mengandungi kumpulan karboksilik tambahan atau kumpulan amina. Contohnya, lisin, histidin, dan arginin adalah asid amino yang mempunyai kumpulan amina tambahan. Dan asid aspartik, asid glutamat mengandungi kumpulan karboksilik tambahan. Selanjutnya, sesetengahnya mengandungi kumpulan -OH, yang boleh bertindak sebagai asas atau asid dalam keadaan tertentu (Tyrosine). Oleh kerana kedua -dua kumpulan berasid dan asas, mereka biasanya mempunyai sekurang -kurangnya dua nilai PKA (jika terdapat lebih daripada satu -NH2 Kumpulan atau kumpulan -COOH, maka akan ada lebih daripada dua nilai PKA). Oleh itu, lengkung titrasi amfolit adalah kompleks daripada lengkung titrasi biasa.
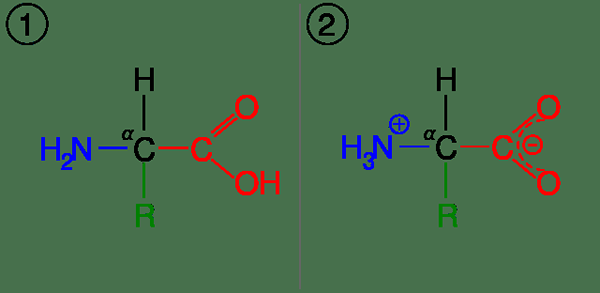
Rajah 01: Asid amino dalam bentuk zwitterionic (1) un-ionisasi dan (2)
Kejadian
Dalam pelbagai sistem, ampholytes berlaku dalam pelbagai bentuk yang dikenakan bergantung pada pH. Sebagai contoh, dalam larutan berasid, kumpulan amina asid amino akan berlaku dalam keadaan positif, dan kumpulan karboksil akan wujud sebagai -cooh. Dalam penyelesaian pH asas, kumpulan karboksil akan wujud dalam bentuk anion karboksilat (-coo-), dan kumpulan amino akan hadir sebagai -nh2.
Di badan manusia, pH hampir 7.4. Oleh itu, dalam pH ini, asid amino hadir sebagai zwitterions. Di sini, kumpulan amino menjalani protonasi dan mempunyai caj positif, sedangkan kumpulan karboksil mempunyai caj negatif. Oleh itu, caj bersih molekul adalah sifar. Pada ketika ini, molekul mencapai titik isoelektriknya.
Apa itu amphoterik?
Istilah amphoterik bermaksud keupayaan molekul, ion atau sebatian kompleks lain untuk bertindak sebagai asas dan asid. Terdapat beberapa molekul, yang mempunyai kedua -dua sifat ini dalam keadaan tertentu. Selain itu, terdapat beberapa oksida logam dan hidroksida, yang amphoterik.
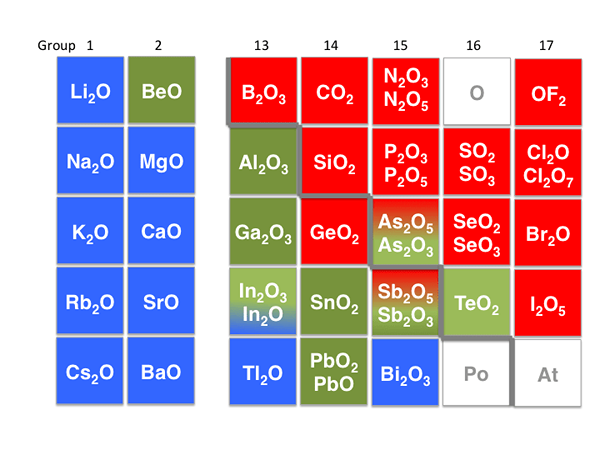
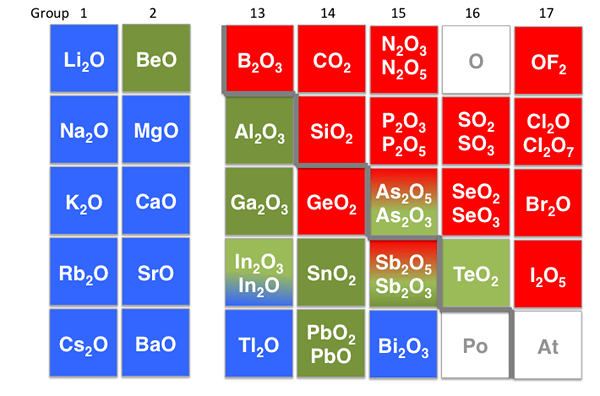
Rajah 02: Sebatian amphoterik
Contohnya, zink oksida (ZnO), aluminium oksida (AL2O3), aluminium hidroksida (AL (OH)3), dan oksida plumbum adalah amphoterik. Dalam medium berasid, mereka bertindak sebagai pangkalan, dan dalam medium asas, mereka bertindak sebagai asid. Molekul amphoterik yang paling biasa dan terkenal adalah asid amino, yang dapat kita perhatikan dalam semua sistem biologi.
Apakah perbezaan antara ampholyte dan amphoteric?
Ampholyte adalah molekul yang mempunyai kumpulan asas dan berasid dan istilah amphoterik bermaksud keupayaan molekul, ion atau sebatian kompleks lain untuk bertindak sebagai asas dan asid. Perbezaan utama antara ampholyte dan amphoterik ialah istilah amphoterik bermaksud keupayaan molekul untuk bertindak sebagai asid atau asas manakala ampholyte adalah molekul yang amphoterik.
Tambahan pula, zink oksida, aluminium oksida, aluminium hidroksida, dan oksida plumbum adalah amphoterik, yang mempunyai tingkah laku yang berbeza dalam penyelesaian berasid dan asas. Walau bagaimanapun, ini bukan ampholytes kerana mereka tidak mempunyai kumpulan berasid dan asas dalam molekul tersebut. Bagaimanapun, asid amino adalah ampholyte, yang mempunyai kumpulan berasid dan asas yang terdapat dalam satu molekul. Oleh itu, ia juga amphoterik.

Ringkasan -Ampholyte vs Amphoteric
Amphoterik bermaksud keupayaan molekul untuk bertindak sebagai asid atau asas. Ampholytes adalah molekul yang amphoterik. Oleh itu, ampholytes mempunyai kumpulan berasid dan asas. Oleh itu, perbezaan utama antara ampholyte dan amphoterik ialah istilah amphoterik bermaksud keupayaan molekul untuk bertindak sebagai asid atau asas manakala ampholyte adalah molekul yang amphoterik.
Rujukan:
1. Helmenstine, Anne Marie, PH.D. "Definisi dan contoh amphoterik."Pemikiran, Jun. 22, 2018. Terdapat di sini
2. Libretexts. "Amphoteric."Kimia Libretexts, Yayasan Sains Kebangsaan, 20 Feb. 2017. Terdapat di sini
Ihsan gambar:
1."Zwitterions Asid Amino" oleh Timvickersvector (CC oleh 3.0) melalui Commons Wikimedia
2."Amphoteric" oleh TEM5Psu - Kerja Sendiri, (CC BY -SA 3.0) melalui Commons Wikimedia


