Perbezaan antara logam alkali dan logam bumi alkali
The Perbezaan utama Antara logam alkali dan logam bumi alkali ialah Semua logam alkali mempunyai elektron di dalam shell terluar mereka manakala semua logam bumi alkali mempunyai dua elektron luar.
Oleh kerana kedua -dua logam alkali dan logam bumi alkali adalah dua kumpulan pertama dalam jadual berkala, perbezaan antara logam alkali dan logam bumi alkali adalah subjek kepentingan bagi mana -mana pelajar kimia. Logam Alkali dan Logam Bumi Alkali adalah unsur-unsur "S-blok" kerana unsur-unsur dalam kedua-dua kumpulan ini mempunyai elektron paling luar mereka di S-Subshell.
Kedua -dua logam alkali dan logam bumi alkali adalah konduktor elektrik dan haba yang baik. Unsur -unsur dalam kedua -dua kumpulan ini adalah logam paling reaktif dalam jadual berkala. Titik lebur mereka agak lebih rendah daripada logam lain. Logam Alkali dan Logam Bumi Alkali mempunyai banyak sifat yang serupa, tetapi artikel ini membincangkan perbezaannya.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah logam alkali
3. Apakah logam bumi alkali
4. Perbandingan sampingan - Logam Alkali vs Logam Bumi Alkali dalam bentuk jadual
5. Ringkasan
Apakah logam alkali?
Logam Alkali adalah unsur -unsur yang terdapat dalam kumpulan pertama jadual berkala. Mereka adalah litium (li), natrium (na), kalium (k), rubidium (rb), cesium (cs) dan francium (fr). Mereka semua adalah logam dan sangat reaktif oleh itu tidak ada logam ini tidak berlaku sebagai logam percuma. Kita harus menyimpan logam ini selalu dalam cecair lengai seperti minyak tanah kerana mereka cepat bertindak balas dengan udara, wap air dan oksigen di udara. Kadang -kadang mereka bertindak balas dengan bahan lain dengan bahan lain. Mereka boleh mencapai keadaan gas mulia dengan mudah, dengan mengeluarkan elektron paling luar dalam shell valence.
Ketumpatan litium dan natrium kurang daripada ketumpatan air. Walau bagaimanapun, elemen lain lebih padat daripada air. Banyak sebatian logam alkali (NaCl, KCl, NA2Co3, NaOH) secara komersil sangat penting.
Apakah logam bumi alkali?
Logam Bumi Alkali berada dalam kumpulan kedua jadual berkala. Unsur -unsur kumpulan II termasuk; Beryllium (BE), Magnesium (Mg), Kalsium (Ca), Strontium (Sr), Barium (BA) dan Radium (RA). Sama dengan logam alkali, unsur -unsur ini juga tidak berlaku secara bebas dan mereka juga sangat reaktif.

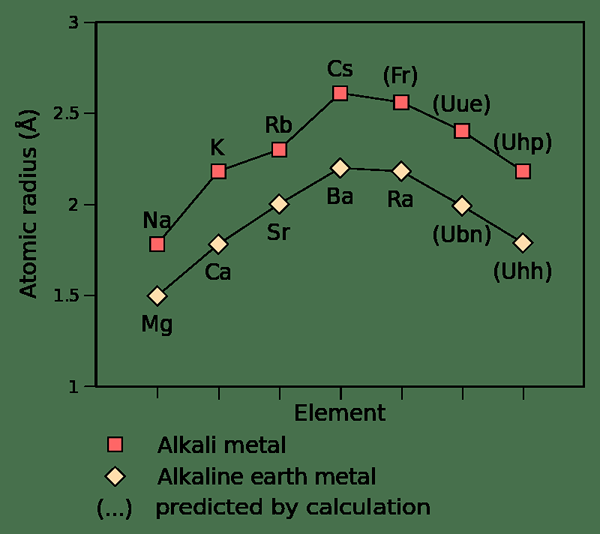
Rajah 01: Radius atom Logam Alkali dan Alkali Bumi
Semua unsur dalam kumpulan ini lebih padat daripada air. Logam tulen mempunyai warna perak kelabu, tetapi mereka cenderung untuk menghilangkannya dengan cepat apabila terdedah kepada udara kerana mereka membentuk lapisan oksida di permukaan. Sama seperti logam alkali, logam ini juga konduktor yang baik dalam haba dan elektrik. Semua logam ini berharga secara komersial.
Apakah perbezaan antara logam alkali dan logam bumi alkali?
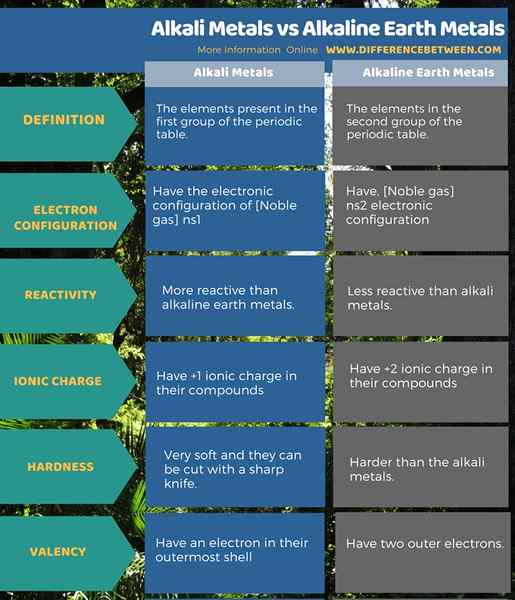
Logam Alkali adalah unsur -unsur yang terdapat dalam kumpulan pertama jadual berkala. Logam Bumi Alkali berada dalam kumpulan kedua jadual berkala. Logam alkali mempunyai konfigurasi elektronik [gas mulia] ns1 Walaupun logam bumi alkali mempunyai, [gas mulia] ns2 Konfigurasi Elektronik. Berkenaan dengan valensi logam ini, semua logam alkali mempunyai elektron di cangkang paling luar mereka. Dan semua logam bumi alkali mempunyai dua elektron luar.
Logam Alkali hanya mempunyai caj +1 ionik dalam sebatian mereka apabila logam bumi alkali mempunyai caj +2 ionik dalam sebatian mereka. Secara perbandingan, logam alkali lebih reaktif daripada logam bumi alkali. Selain itu, logam alkali sangat lembut dan mereka boleh dipotong dengan pisau tajam. Walau bagaimanapun, logam bumi alkali lebih sukar daripada logam alkali.
Ringkasan -Logam Alkali vs Logam Bumi Alkali
Logam Alkali dan Logam Bumi Alkali adalah unsur Kumpulan I dan Kumpulan II dalam jadual berkala masing -masing. Perbezaan yang paling ketara antara kedua -dua kumpulan ini ialah konfigurasi elektronik. Ia menentukan valensi unsur -unsur. Oleh itu, perbezaan antara logam alkali dan logam bumi alkali adalah bahawa semua logam alkali mempunyai elektron di dalam shell terluar mereka sedangkan semua logam bumi alkali mempunyai dua elektron luar.
Rujukan:
1. Tepper, Frederick, dan James L. Pewarna. "Logam Alkali."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 21 Jun 2017. Terdapat di sini
2. "Logam Bumi Alkali."Wikipedia, Yayasan Wikimedia, 20 Mei 2018. Terdapat di sini
Ihsan gambar:
1.'Radius atom Logam Alkali dan Alkali Bumi Logam' By Depiep - Kerja Sendiri, (CC BY -SA 3.0) melalui Commons Wikimedia


