Perbezaan antara tindak balas tambahan dan penggantian

The Perbezaan utama antara tindak balas tambahan dan pengganti adalah bahawa Reaksi tambahan adalah tindak balas kimia yang membentuk molekul besar dari dua atau lebih molekul kecil manakala tindak balas penggantian adalah tindak balas kimia di mana atom atau kumpulan berfungsi menggantikan atom atau kumpulan fungsi molekul.
Reaksi kimia adalah perubahan dalam perkara dengan cara kimia. Reaksi tambahan adalah tindak balas kombinasi di mana molekul besar terbentuk dari gabungan molekul kecil. Reaksi penggantian adalah tindak balas penggantian di mana molekul molekul menggantikan molekul molekul lain. Ini menghasilkan sebatian yang berbeza.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah reaksi tambahan
3. Apakah reaksi penggantian
4. Perbandingan sampingan - Penambahan vs tindak balas penggantian dalam bentuk jadual
5. Ringkasan
Apakah reaksi tambahan?
Reaksi tambahan adalah tindak balas kimia di mana molekul besar membentuk dari dua atau lebih molekul kecil. Di sini, produk sampingan tidak terbentuk. Oleh itu, ia adalah satu bentuk tindak balas kimia organik yang sangat mudah. Kami memanggil produk "adduct". Reaksi ini terhad kepada alkena dan alkynes.

Rajah 01: Ethene dapat menjalani tindak balas tambahan
Selain itu, kumpulan karbonil dan kumpulan imine juga boleh menjalani tindak balas jenis ini kerana kehadiran ikatan berganda. Reaksi tambahan adalah bertentangan dengan reaksi penghapusan. Dua jenis utama adalah tindak balas tambahan elektrofilik dan tindak balas tambahan nukleofilik. Apabila tindak balas ini menyebabkan pempolimeran, kami menyebutnya pempolimeran tambahan.
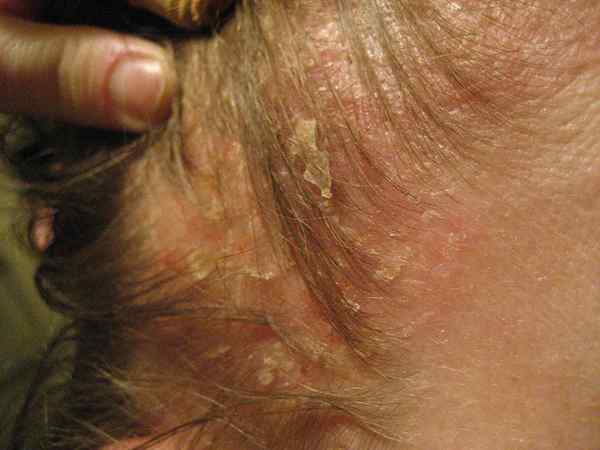
Apakah reaksi penggantian?
Reaksi penggantian adalah tindak balas kimia di mana molekul molekul menggantikan molekul molekul lain. Moieties ini boleh menjadi atom, ion, atau kumpulan berfungsi. Kebanyakan masa, tindak balas ini berlaku dengan menggantikan kumpulan fungsi molekul dengan kumpulan fungsi lain. Oleh itu, ini adalah tindak balas yang sangat penting dalam kimia organik.
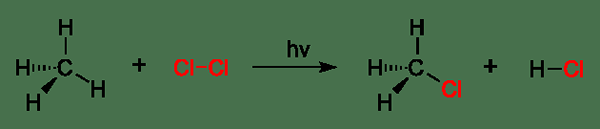
Rajah 02: Klorinasi metana adalah tindak balas penggantian
Terdapat dua jenis tindak balas penggantian; iaitu, tindak balas penggantian elektrofilik dan tindak balas penggantian nukleofilik. Selain itu, kategori lain juga ada; itu adalah tindak balas penggantian radikal.
Apakah perbezaan antara tindak balas tambahan dan penggantian?
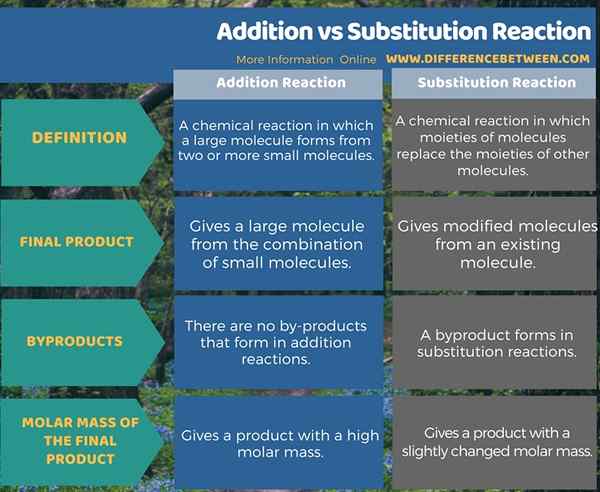
Reaksi tambahan adalah tindak balas kimia di mana molekul besar membentuk dari dua atau lebih molekul kecil. Reaksi penggantian adalah tindak balas kimia di mana molekul molekul menggantikan molekul molekul lain. Ini adalah perbezaan utama antara tindak balas tambahan dan penggantian. Seperti yang diberikan di bawah, terdapat lebih banyak perbezaan yang berkaitan antara tindak balas tambahan dan penggantian.
Ringkasan -Tambahan vs Reaksi Penggantian
Dua reaksi kimia penting utama dalam kimia organik adalah tindak balas tambahan dan tindak balas penggantian. Perbezaan utama antara penambahan dan tindak balas penggantian ialah tindak balas tambahan adalah tindak balas gabungan di mana molekul besar membentuk dari dua atau lebih molekul kecil manakala tindak balas penggantian adalah tindak balas kimia di mana atom atau kumpulan fungsi menggantikan atom atau kumpulan fungsi molekul suatu molekul.
Rujukan:
1. "Tambahan reaksi."Wikipedia, Yayasan Wikimedia, 27 Jun 2018.Terdapat di sini
2. Helmenstine, Anne Marie. "Definisi tindak balas penggantian."Thoughtco, Thoughtco. Terdapat di sini
Ihsan gambar:
1.'Tambahan Reaksi terhadap Ethene'by Calvero - Kerja Sendiri, (Domain Awam) melalui Commons Wikimedia
2.'SubstitationReaction'by v8rik di Wikipedia Bahasa Inggeris, (CC BY-SA 3.0) melalui Commons Wikimedia