Perbezaan antara pemalar pengionan asid dan asas pengionan asas
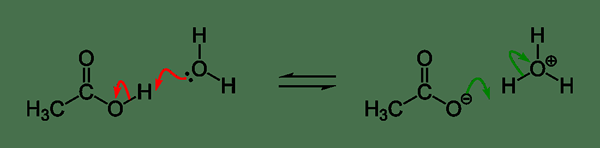
Perbezaan utama - Pengionan Asid Malar vs asas pengionan asas
Pemalar pengionan asid (ka, juga dikenali sebagai pemisahan pemisahan asid) memberikan pengukuran kuantitatif keseimbangan yang wujud antara molekul asid dan bentuk terionisasinya. Begitu juga, pemalar pengionan asas (kb, atau pemisahan pemisahan asas) memberikan pengukuran kuantitatif keseimbangan yang wujud antara molekul asas dan bentuk terionisasi mereka. The Perbezaan utama antara pemalar pengionan asid dan pemalar pengionan asas ialah Pemalar pengionan asid memberikan ukuran kuantitatif kekuatan asid dalam larutan manakala pemalar pengionan asas memberikan ukuran kuantitatif kekuatan asas dalam larutan.
Pengionan adalah pemisahan molekul ke dalam spesies ionik (kation dan anion). Pemalar keseimbangan adalah hubungan antara jumlah reaktan dan produk yang berada dalam keseimbangan antara satu sama lain.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu pemalar pengionan asid
3. Apakah asas pengionan asas
4. Perbandingan sampingan - Pengionan asid tetap vs asas pengionan asas dalam bentuk tabular
5. Ringkasan
Apa itu pemalar pengionan asid?
Pemalar pengionan asid adalah bilangan yang menyatakan hubungan antara molekul asid dan spesies ionik yang wujud dalam penyelesaian yang sama. Pemalar pemisahan asid dilambangkan oleh KA. Ia adalah ukuran kuantitatif kekuatan asid dalam larutan. Kekuatan asid bergantung kepada pengionan (atau pemisahan) asid dalam larutan berair.
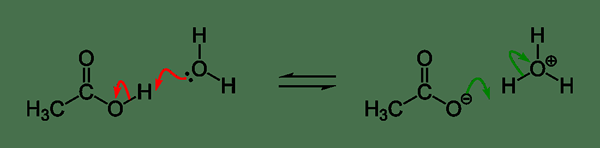
Rajah 01: Contoh untuk pengionan asid
Pengionan asid boleh diberikan seperti di bawah,
Ha + h2O ↔ a- + H3O+
Dalam hal ini, HA adalah asid lemah yang memisahkan sebahagiannya ke dalam ion; Anion dikenali sebagai asas konjugasi asid tertentu. Pemisahan asid mengeluarkan proton (ion hidrogen; h+). Proton ini menggabungkan dengan molekul air yang membentuk ion hidronium (h3O+). Pemalar pengionan asid asid HA ini boleh diberikan seperti di bawah,
Ka = [a-] [H3O+] / [Ha] [h2O]
Bentuk biasa ka adalah PKA, yang merupakan nilai log minus ka. Itu kerana nilai ka adalah nilai yang sangat kecil dan sukar dikendalikan. PKA memberikan nombor mudah yang mudah ditangani. Ia boleh diberikan seperti di bawah,
pka = -log (ka)
Nilai KA atau PKA boleh digunakan untuk menyatakan kekuatan asid.
- Asid lemah mempunyai nilai KA yang lebih rendah dan nilai PKA yang lebih tinggi
- Asid kuat mempunyai nilai KA yang lebih tinggi dan nilai PKA yang lebih rendah.
Apakah asas pengionan asas?
Pemalar pengionan asas adalah bilangan yang menyatakan hubungan antara molekul asas dan spesies ionik wujud dalam penyelesaian yang sama. Ini dilambangkan oleh KB. Ia mengukur kekuatan asas dalam penyelesaian. Lebih tinggi kb, lebih tinggi pengionan asas. Untuk asas tertentu dalam penyelesaian, pemalar pemisahan asas boleh diberikan seperti di bawah,
B+ h2O ↔ bh+ + Oh-
Kb = [bh+] [OH-] / [B] [h2O]
Oleh kerana nilai kb asas adalah nilai yang sangat kecil, nilai log minus kb digunakan sebaliknya kb. Nilai log minus kb dilambangkan oleh pkb. PKB memberikan nombor yang mudah dikendalikan.
pkb = -log (kb)
Kekuatan asas boleh dinyatakan oleh nilai kb atau nilai pkb seperti berikut.
- Lebih tinggi nilai pemalar pengionan asas, lebih kuat asas (menurunkan PKB)
- Menurunkan nilai pemalar pengionan asas, lemah asas (lebih tinggi PKB)
Apakah perbezaan antara pemalar pengionan asid dan pemalar pengionan asas?
Pengionan asid tetap vs asas pengionan asas | |
| Pemalar pengionan asid adalah bilangan yang menyatakan hubungan antara molekul asid dan spesies ionik yang ada dalam larutan yang sama. | Pemalar pengionan asas adalah bilangan yang menyatakan hubungan antara molekul asas dan spesies ionik yang ada dalam penyelesaian yang sama. |
| Konsep | |
| Pemalar pengionan asid memberikan kekuatan asid. | Pemalar pengionan asas memberikan kekuatan asas. |
| Nilai log | |
| Nilai log minus ka adalah pka. | Nilai log minus kb ialah pkb. |
| Nilai pemalar | |
| Asid lemah mempunyai nilai KA yang lebih rendah dan nilai PKA yang lebih tinggi manakala asid kuat mempunyai nilai KA yang lebih tinggi dan nilai PKA yang lebih rendah. | Pangkalan lemah mempunyai nilai kb yang lebih rendah, dan nilai pkb yang lebih tinggi manakala pangkalan yang kuat mempunyai nilai kb yang lebih tinggi dan nilai pkb yang lebih rendah. |
Ringkasan - Pengionan asid Malar vs asas pengionan asas
Pemalar pengionan asid dan pemalar pengionan asas adalah ukuran asid dan kekuatan asas masing -masing. Perbezaan antara pemalar pengionan asid dan pemalar pengionan asas ialah pemalar pengionan asid memberikan ukuran kuantitatif kekuatan asid dalam larutan manakala pemalar pengionan asas memberikan ukuran kuantitatif kekuatan asas dalam larutan.
Rujukan:
1."16.4: Kekuatan asid dan pemisahan asid (ka)."Kimia Libretexts, Libretexts, 26 Feb. 2017. Terdapat di sini
2."Pangkalan yang kuat dan lemah dan pemalar pengionan asas (KB)."Yayasan CK-12, Yayasan CK-12, 11 Sept. 2016. Terdapat di sini
3."Asid dan Pangkalan: Pemalar Pengionan."Pengionan asid dan pangkalan. Terdapat di sini
Ihsan gambar:
1.'Acetic-asid-disociation-2d-curly-arrows'by Ben Mills-kerja sendiri, (domain awam) melalui Commons Wikimedia


