Apakah perbezaan antara titik triple dan titik eutektik
The Perbezaan utama antara titik tiga dan titik eutektik adalah pada titik tiga, tiga fasa bahan wujud dalam keseimbangan, sedangkan pada titik eutektik, campuran eutektik tertentu membeku atau cair.
Mengubah suhu dan tekanan sistem kimia dapat mengubah keadaan fizikal atau fasa sistem itu kerana komponen dalam sistem itu mempunyai titik lebur dan mendidih tertentu di mana perubahan fasa berlaku antara fasa pepejal, cecair, dan gas.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu Titik Triple
3. Apakah titik eutektik
4. Titik Triple Vs Rajah Titik Eutektik
5. Ringkasan -titik triple vs titik eutektik
Apa itu Titik Triple?
Titik triple adalah suhu dan tekanan di mana fasa pepejal, cecair, dan wap bahan tertentu wujud dalam keseimbangan. Ia menggambarkan keadaan termodinamik tertentu. Kadang -kadang, titik tiga mungkin melibatkan lebih daripada satu fasa pepejal apabila terdapat polimorf bahan yang wujud. Dalam rajah fasa, titik tiga adalah titik di mana ketiga -tiga garis sempadan bertemu antara satu sama lain.
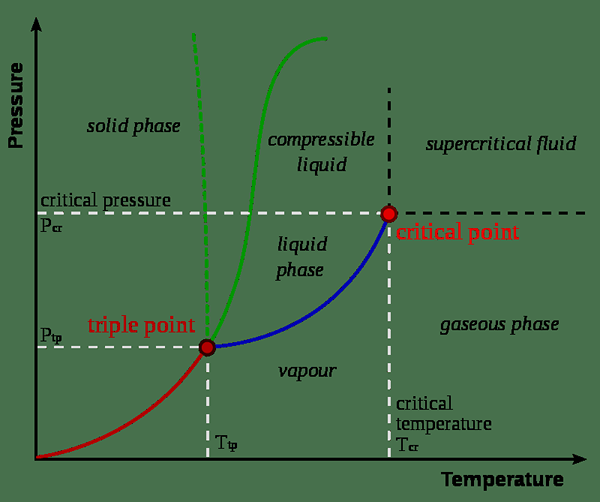
Rajah 01: Titik Triple
Apakah titik eutektik?
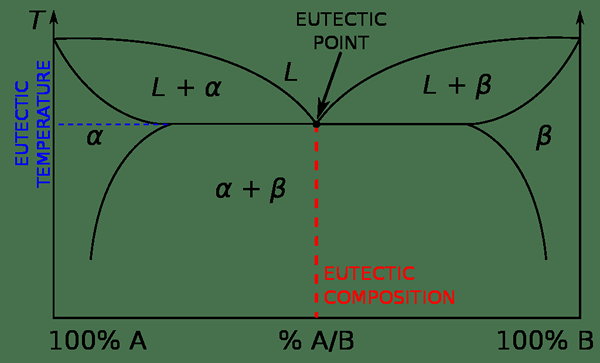
Titik eutektik adalah suhu dan tekanan di mana campuran cecair tertentu berubah menjadi dua fasa pepejal pada masa yang sama apabila menyejukkan cecair. Sistem eutektik adalah campuran bahan homogen yang dapat mencairkan atau menguatkan pada suhu yang lebih rendah daripada titik lebur dari konstituen dalam campuran itu. Selain itu, istilah suhu eutektik menerangkan suhu lebur yang paling rendah untuk semua nisbah pencampuran yang mungkin terlibat dalam pembentukan campuran.

Rajah 02: Titik eutektik
Apabila memanaskan campuran eutektik, kekisi satu komponen dalam campuran akan mencairkan terlebih dahulu pada suhu eutektik. Walau bagaimanapun, apabila menyejukkan sistem eutektik, setiap komponen dalam campuran cenderung menguatkan, membentuk kekisi komponen tersebut pada suhu yang berbeza. Pemejalan berlaku sehingga semua bahan menjadi pepejal. Secara umum, sistem eutektik mengandungi dua komponen: oleh itu, pada suhu eutektik, cecair berubah menjadi dua fasa pepejal pada masa yang sama dan pada suhu yang sama. Oleh itu, kita boleh menamakan tindak balas jenis ini sebagai tindak balas tiga fasa. Ini adalah jenis reaksi fasa tertentu; Contohnya, cecair menguatkan, membentuk kisi pepejal alfa dan beta. Di sini, fasa cecair dan fasa pepejal berada dalam keseimbangan antara satu sama lain, keseimbangan terma.
Apakah perbezaan antara titik triple dan titik eutektik?
Titik triple adalah suhu dan tekanan di mana fasa pepejal, cecair, dan wap bahan tertentu wujud dalam keseimbangan. Titik eutektik istilah adalah suhu dan tekanan di mana campuran cecair tertentu berubah menjadi dua fasa pepejal pada masa yang sama apabila menyejukkan cecair. Perbezaan utama antara titik tiga dan titik eutektik ialah pada titik tiga, tiga fasa bahan wujud dalam keseimbangan, sedangkan pada titik eutektik, campuran eutektik tertentu membeku atau cair. Dalam erti kata lain, pada titik tiga, tiga fasa wujud pada suhu dan keadaan tekanan yang sama, sedangkan pada titik eutektik, cecair berubah menjadi dua fasa pepejal pada suhu dan keadaan tekanan yang sama.
Infographic di bawah menyenaraikan perbezaan antara titik tiga dan titik eutektik dalam bentuk tabular untuk perbandingan sampingan
Ringkasan -titik triple vs titik eutektik
Ringkasnya, titik tiga adalah suhu dan tekanan di mana fasa pepejal, cecair, dan wap bahan tertentu wujud dalam keseimbangan, manakala titik eutektik adalah suhu dan tekanan di mana campuran cecair tertentu berubah menjadi dua fasa pepejal pada masa yang sama apabila menyejukkan cecair. Perbezaan utama antara titik tiga dan titik eutektik ialah pada titik tiga, tiga fasa bahan wujud dalam keseimbangan, sedangkan pada titik eutektik, campuran eutektik tertentu membeku atau cair.
Rujukan:
1. Connor, Nick. "Apakah titik tiga air - definisi." Kejuruteraan Thermal, 3 Jun 2019.
Ihsan gambar:
1. "Fasa-Diag2" oleh Matthieumarechal (CC BY-SA 3.0) melalui Commons Wikimedia
2. "Rajah fasa sistem eutektik" oleh Eutektikum_new.SVG: *Eutektikum.GIF: Dr. Báder Imrederivative Work: Michbich (Talk) Derivative Work: Wizard191 (Talk) - Eutektikum_new.SVG (CC BY-SA 3.0) melalui Commons Wikimedia


