Perbezaan antara isotop dan radioisotop yang stabil
Perbezaan utama - Isotop stabil vs radioisotop
Isotop adalah bentuk yang berbeza dari elemen kimia yang sama yang mempunyai jisim atom yang berbeza. Ini bermakna isotop elemen kimia tertentu mempunyai nombor atom yang sama tetapi jisim atom yang berbeza. Ini kerana isotop ini mempunyai bilangan neutron yang berlainan dalam nukleus atom mereka. Beberapa isotop stabil sedangkan ada yang tidak stabil. Isotop yang stabil adalah bentuk unsur kimia secara semula jadi. Isotop stabil ini boleh berlaku secara semula jadi dalam bentuk atom atau digabungkan dengan atom lain. Isotop yang tidak stabil menjalani kerosakan radioaktif sehingga mereka mendapat keadaan yang stabil. Isotop ini dikenali sebagai radioisotop. Perbezaan utama antara isotop stabil dan radioisotop ialah Isotop stabil tidak mengalami kerosakan radioaktif manakala radioisotop mengalami kerosakan radioaktif.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah isotop stabil
3. Apa itu radioisotop
4. Perbandingan sampingan - isotop stabil vs radioisotop dalam bentuk jadual
5. Ringkasan
Apakah isotop stabil?
Isotop stabil adalah bentuk yang berbeza dari elemen kimia yang sama, yang mempunyai nukleus yang stabil. Atom ini mempunyai bilangan atom yang sama (bilangan proton dalam nukleus atom) kerana ia tergolong dalam elemen kimia yang sama, tetapi massa atom berbeza antara satu sama lain kerana mereka mempunyai bilangan neutron yang berlainan dalam nukleus atom.
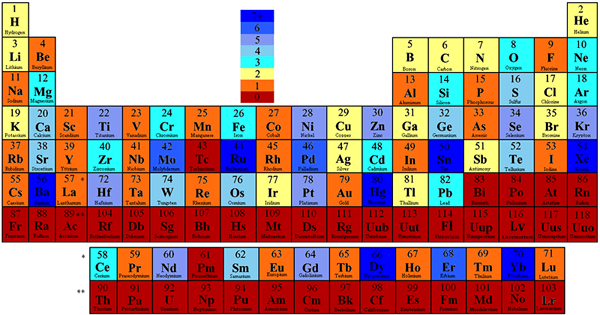
Isotop stabil tidak radioaktif kerana kestabilan nukleus atom. Oleh itu, atom -atom ini tidak memancarkan radiasi. Unsur kimia tertentu boleh mempunyai lebih dari satu isotop yang stabil. Tetapi dalam beberapa elemen kimia, semua isotop tidak stabil; Oleh itu, mereka radioaktif.

Rajah 1: Jadual berkala berwarna berdasarkan bilangan isotop stabil
Kestabilan nukleus atom bergantung kepada dua faktor asas:
- Nisbah antara proton dan neutron
- Jumlah proton dan neutron
"Nombor Magic" adalah konsep kimia yang digunakan untuk menentukan kestabilan nukleus atom tertentu. Ia memberikan bilangan elektron yang hadir di isotop stabil. Nombor sihir boleh sama ada bilangan proton atau bahkan bilangan neutron yang terdapat di dalam nukleus.
Nombor Magic: 2, 8, 20, 28, 50, 82 dan 126
Sekiranya bilangan atom isotop sama dengan salah satu nombor di atas, maka itu adalah isotop yang stabil. Di samping itu, jika isotop mempunyai 114 proton, ia adalah isotop stabil. Selain itu, jika terdapat 126 atau 184 neutron hadir, mereka juga stabil isotop. Di samping.
Apa itu radioisotop?
Radioisotop adalah isotop unsur -unsur kimia yang tidak stabil yang mengalami kerosakan radioaktif. Isotop ini mengalami kerosakan radioaktif kerana mereka mempunyai nukleus atom yang tidak stabil. Sebilangan besar elemen kimia mempunyai satu atau lebih isotop radioaktif manakala beberapa elemen kimia hanya mempunyai isotop radioaktif (contohnya: uranium).
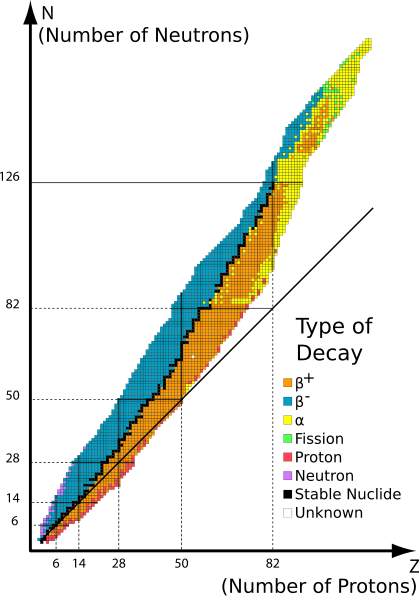
Rajah 2: Radioisotop yang berbeza dan kerosakan radioaktif mereka
Isotop radioaktif tidak stabil kerana beberapa sebab:
- Kehadiran bilangan neutron yang tinggi dalam nukleus atom berbanding bilangan proton
- Di radioisotop ini, neutron diubah menjadi proton dan elektron semasa kerosakan radioaktif.
- Kehadiran bilangan proton yang tinggi dalam nukleus atom
- Di radioisotop ini, proton diubah menjadi neutron dan positron.
- Kehadiran bilangan proton dan elektron yang tinggi
- Radioisotop ini menjalani kerosakan alfa di mana dua proton dan dua neutron dipancarkan sebagai zarah alfa
Apakah perbezaan antara isotop stabil dan radioisotop?
Isotop stabil vs radioisotop | |
| Isotop stabil adalah bentuk yang berbeza dari elemen kimia yang sama, yang mempunyai nukleus yang stabil. | Radioisotop adalah isotop unsur -unsur kimia yang tidak stabil yang mengalami kerosakan radioaktif. |
| Kestabilan | |
| Isotop stabil sangat stabil dan tidak mengalami kerosakan radioaktif. | Radioisotop sangat tidak stabil dan mengalami kerosakan radioaktif untuk mendapatkan keadaan yang stabil. |
| Proton | |
| Kehadiran 114 proton menjadikan isotop isotop yang stabil. | Kehadiran bilangan proton yang tinggi menjadikan isotop radioisotop. |
| Neutron | |
| Kehadiran 126 atau 184 neutron menjadikan isotop isotop yang stabil. | Bilangan neutron dalam jejari atom lebih tinggi daripada bilangan proton. |
Ringkasan -Isotop stabil vs radioisotop
Isotop adalah atom elemen kimia yang sama yang mempunyai nombor atom yang sama tetapi jisim atom yang berbeza. Sesetengah isotop stabil sedangkan yang lain tidak stabil. Isotop stabil adalah bentuk semula jadi unsur -unsur kimia. Isotop yang tidak stabil juga dipanggil radioisotop kerana isotop ini mengalami kerosakan radioaktif untuk mendapatkan keadaan yang stabil. Perbezaan utama antara isotop stabil dan radioisotop adalah berdasarkan keupayaan mereka untuk menjalani kerosakan radioaktif.
Rujukan:
1. "Nisbah isotop stabil."Wikipedia, Yayasan Wikimedia, 27 Feb. 2018, boleh didapati di sini.
2. "Apa itu radioisotop?"Foro Nuklear, boleh didapati di sini.
3. Britannica, editor Encyclopaedia. "Nombor sihir."Encyclopædia Britannica, Encyclopædia Britannica, Inc., 12 Julai 2017, boleh didapati di sini.
Ihsan gambar:
1. "Jadual berkala dengan bilangan isotop stabil" oleh Nergaal di Wikipedia Inggeris (CC BY-SA 3.0) melalui Commons Wikimedia
2. "Jadual Isotop en" oleh Table_Isotopes.SVG: Napy1kenobiderivative Work: Sjlegg (Talk) - Table_isotopes.SVG (CC BY-SA 3.0) melalui Commons Wikimedia


