Perbezaan antara KSP dan QSP
Perbezaan utama - KSP vs QSP
KSP adalah pemalar produk kelarutan dan QSP adalah kelarutan produk Kuasa. The Perbezaan utama antara KSP dan QSP ialah KSP menunjukkan kelarutan bahan manakala QSP menunjukkan keadaan semasa penyelesaian. Produk kelarutan adalah hasil kepekatan spesies ionik yang terdapat dalam larutan apabila bahan dibubarkan dalam pelarut seperti air.
Produk kelarutan ditentukan apabila penyelesaiannya tepu dengan bahan tersebut. Kuasa produk kelarutan adalah hasil kepekatan spesies ionik dalam penyelesaian pada bila -bila masa; Sebelum ketepuan atau selepas penyelesaiannya tepu. Kadang -kadang dikenali sebagai produk ionik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu KSP
3. Apa itu QSP
4. Hubungan antara KSP dan QSP
5. Perbandingan sampingan - KSP vs QSP dalam bentuk jadual
6. Ringkasan
Apa itu KSP?
KSP adalah pemalar produk kelarutan bahan tertentu. Ia menunjukkan kelarutan bahan (berapa banyak pepejal dibubarkan dalam larutan). Pemalar produk kelarutan diberikan untuk penyelesaian yang tepu dengan bahan. Lebih tinggi KSP, lebih tinggi kelarutan bahan tersebut. Produk kelarutan diberikan sebagai hasil kepekatan spesies ionik dalam penyelesaian.
Penyelesaian tepu muncul dengan kelembutan yang menunjukkan permulaan pembentukan pendahuluan. Ia adalah bentuk larut yang tidak larut. Bahagian cecair sistem itu mempunyai larutan larut. KSP penyelesaian itu mewakili keseimbangan antara bentuk larut dan tidak larut ini.
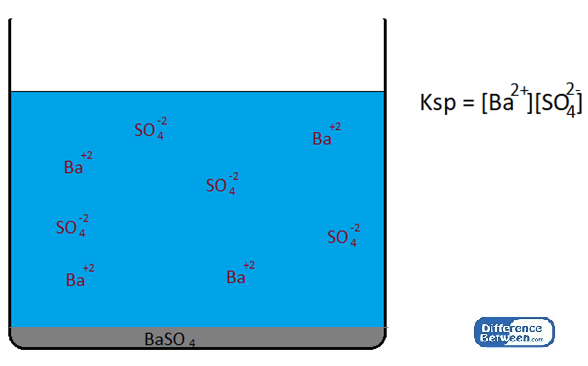
Faktor -faktor yang mempengaruhi nilai pemalar produk kelarutan adalah suhu, kehadiran ion biasa, pH atau keasidan, dll. Apabila suhu meningkat, kelarutan mendakan pepejal juga meningkat. Kemudian produk kepekatan spesies ionik meningkat, mengakibatkan nilai tinggi kelarutan produk pemalar. Kehadiran ion biasa digambarkan oleh kesan ion biasa. Apabila ion biasa hadir, KSP berkurangan. Ion biasa bermaksud salah satu spesies ionik yang sudah ada dalam penyelesaiannya. Sebagai contoh, untuk sistem keseimbangan yang mengandungi baso4 (barium sulfat) mendakan bersama dengan, BA+2 ion dan sebagainya42- ion, penambahan sama ada BA+2 atau lebih42- ion boleh menjejaskan keseimbangan.
Baso4 (s)↔ ba+2(aq) + Jadi42-(aq)

Rajah 01: KSP penyelesaian tepu BASO4
Apabila salah satu daripada ion-ion ini ditambah dari sumber luaran, maka keseimbangan di atas beralih ke arah kiri (bentuk bahan yang lebih tidak larut terbentuk menurun jumlah ion yang ada dalam larutan), mengurangkan kelarutan bahan tersebut.
Apa itu QSP?
QSP adalah kelarutan produk penyelesaian penyelesaian. Ia menerangkan keadaan penyelesaian semasa. Ini bermaksud QSP diberikan untuk penyelesaian yang tidak tepu (sebelum tepu), tepu atau penyelesaian supersaturated. QSP juga dipanggil produk ion kerana ia adalah hasil kepekatan spesies ionik pada bila -bila masa (tidak pada saat tertentu seperti ketepuan). Oleh itu, KSP (pemalar produk kelarutan) adalah bentuk khas QSP.
Apakah hubungan antara KSP dan QSP?
- Sekiranya nilai QSP kurang daripada KSP untuk bahan dalam penyelesaian, lebih banyak pepejal dapat dibubarkan dalam penyelesaian tersebut.
- Apabila QSP dan KSP mempunyai nilai yang sama, maka penyelesaiannya telah menjadi tepu.
- Sekiranya QSP lebih tinggi daripada nilai KSP, endapan terbentuk.
Apakah perbezaan antara KSP dan QSP?
KSP vs QSP | |
| KSP adalah pemalar produk kelarutan bahan tertentu. | QSP adalah kelarutan produk penyelesaian penyelesaian. |
| Alam | |
| KSP adalah nilai keseimbangan. | QSP bukan nilai keseimbangan. |
| Keadaan penyelesaian | |
| KSP adalah hasil kepekatan spesies ionik dalam larutan tepu. | QSP adalah hasil kepekatan spesies ionik dalam larutan tak tepu, tepu atau supersaturated. |
Ringkasan - KSP vs QSP
KSP dan QSP adalah istilah yang sangat berkaitan dalam kimia. KSP ditakrifkan sebagai penyelesaian tepu yang mempunyai keseimbangan antara spesies ionik dan mendakan pepejal (momen di mana pembentukan endapan telah bermula). QSP diberikan untuk bila -bila masa (tidak ditentukan); sebelum ketepuan atau selepas ketepuan. Perbezaan antara KSP dan QSP adalah bahawa KSP adalah pemalar produk kelarutan sedangkan QSP adalah kota produk kelarutan.


