Perbezaan antara atom hidrogen dan ion hidrogen
The Perbezaan utama antara atom hidrogen dan ion hidrogen ialah Atom hidrogen adalah neutral sedangkan ion hidrogen membawa caj.
Hidrogen adalah elemen pertama dan terkecil dalam jadual berkala dan dilambangkan sebagai h. Ia dikategorikan di bawah Kumpulan 1 dan Tempoh 1 dalam jadual berkala kerana konfigurasi elektronnya: 1s1. Hidrogen boleh mengambil elektron untuk membentuk ion yang dikenakan negatif, atau dengan mudah boleh mendermakan elektron untuk menghasilkan proton yang dikenakan positif. Jika tidak, ia boleh berkongsi elektron untuk membuat bon kovalen.
Unsur -unsur dalam jadual berkala tidak stabil kecuali gas mulia. Oleh itu, unsur -unsur cuba bertindak balas dengan unsur -unsur lain untuk mendapatkan konfigurasi elektron gas mulia dan mencapai kestabilan. Begitu juga, hidrogen juga perlu mendapatkan elektron untuk mencapai konfigurasi elektron gas mulia, helium. Apabila mencapai konfigurasi elektron ini, ia membentuk ion hidrogen.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu atom hidrogen
3. Apa itu ion hidrogen
4. Perbandingan sampingan - Atom hidrogen vs ion hidrogen dalam bentuk tabular
5. Ringkasan
Apa itu atom hidrogen?
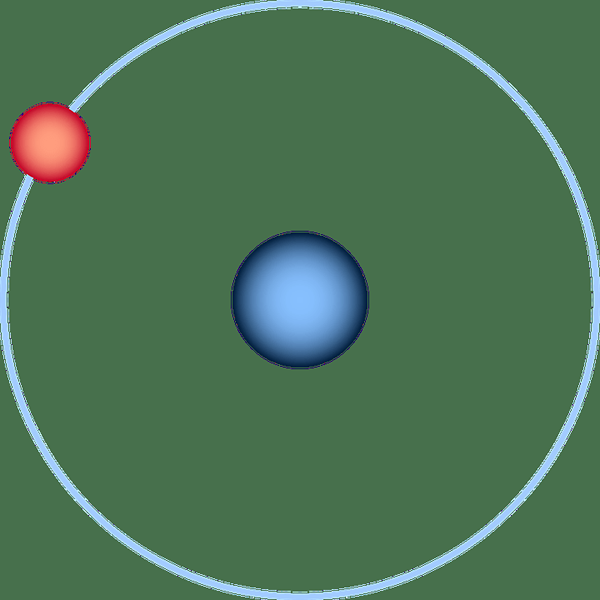
Atom hidrogen adalah elemen pertama dalam jadual berkala. Atom hidrogen mempunyai satu elektron dan satu proton. Oleh itu, konfigurasi elektronnya ialah 1s1. Selain itu, ia hanya mempunyai satu elektron di S-suborbital walaupun orbital ini dapat menampung dua elektron. Oleh itu, atom hidrogen tidak stabil dan sangat reaktif untuk mendapatkan konfigurasi elektron yang stabil.

Rajah 1: Struktur atom hidrogen
Oleh kerana bilangan proton dan elektron dalam atom hidrogen adalah serupa, atom ini tidak membawa caj bersih. Oleh itu, kita mengatakan bahawa ia adalah netral. Walau bagaimanapun, terdapat tiga isotop hidrogen: protium-1H (tiada neutron), deuterium-2H (satu neutron), dan tritium- 3H (dua neutron). Isotop ini mempunyai bilangan neutron yang berbeza -beza dalam nukleus atom.
Apa itu ion hidrogen?
Ion hidrogen adalah bentuk elemen hidrogen yang dikenakan caj. Tuduhan ion ini boleh sama ada positif atau negatif, bergantung pada cara ia membentuk. Ia boleh terbentuk dari sama ada penyingkiran satu elektron dari hidrogen atom atau dari elektron memperoleh. Oleh itu, ion hidrogen mempunyai caj +1 atau -1 (monovalen). Kita boleh menandakan ion hidrogen yang dikenakan positif sebagai H+ (kation) dan ion negatif sebagai H- (anion).
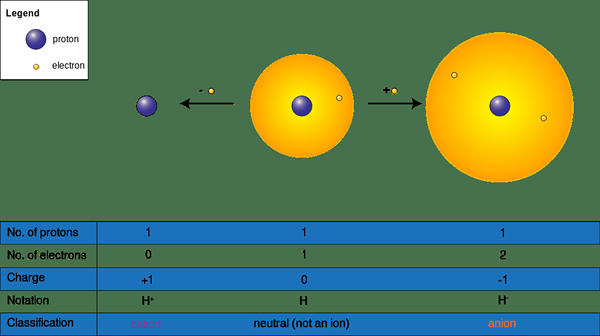
Rajah 2: Pembentukan ion dari atom hidrogen
Kation protium secara khusus dikenali sebagai proton, dan mereka adalah jenis atom hidrogen yang kita pertimbangkan terutamanya dalam tindak balas kimia kerana kelimpahan semulajadi protium sangat tinggi berbanding dengan isotop lain. Selanjutnya, ini wujud dalam larutan akueus sebagai ion hidronium (H3O+).
Ion hidrogen bertanggungjawab untuk keasidan, dan kepekatan ion hidrogen diambil untuk mengira nilai pH. Apabila atom hidrogen bertindak balas dengan nonmetal lain, ion hidrogen dibentuk, dan ini dilepaskan ke medium berair sepenuhnya atau sebahagiannya apabila molekul dibubarkan. Walaupun pembentukan anion hidrogen jarang berlaku, ia terbentuk apabila hidrogen bertindak balas dengan logam seperti logam kumpulan 1.
Apakah perbezaan antara atom hidrogen dan ion hidrogen?
Hidrogen adalah elemen kimia terkecil. Ia mempunyai satu proton dan satu elektron, menjadikannya neutral. Walau bagaimanapun, ion atom hidrogen dikenakan spesies. Oleh itu, perbezaan utama antara atom hidrogen dan ion hidrogen ialah atom hidrogen adalah neutral sedangkan ion hidrogen membawa caj. Satu lagi perbezaan yang signifikan antara atom hidrogen dan ion hidrogen ialah atom hidrogen mempunyai satu elektron manakala kation hidrogen tidak mempunyai elektron dan anion hidrogen mempunyai dua elektron.
Selain itu, atom hidrogen sangat reaktif untuk mendapatkan konfigurasi elektron yang stabil. Tetapi, ion hidrogen kurang/tidak reaktif kerana mereka telah memperoleh keadaan yang stabil. Tuduhan kation adalah +1, dan pertuduhan anion adalah -1. Jadi, kita boleh menganggap ini juga sebagai perbezaan antara atom hidrogen dan ion hidrogen.

Ringkasan -Atom hidrogen vs ion hidrogen
Hidrogen adalah elemen pertama dalam jadual unsur berkala. Oleh itu, ia adalah atom terkecil. Ia boleh membentuk sama ada ion yang dicas secara positif atau negatif. Perbezaan utama antara atom hidrogen dan ion hidrogen ialah atom hidrogen adalah neutral manakala ion hidrogen membawa caj.
Rujukan:
1. John c. Morrison, dalam Fizik Moden, 2010
2. "8.1: Atom hidrogen."Libetexts Fizik, Libretexts, 2 Mei 2019, boleh didapati di sini.
Ihsan gambar:
1. "2750576" (CC0) melalui Pixabay
2. "Ion" oleh JKWCHUI - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia