Perbezaan antara asid hidrofluorik dan asid hidroklorik

The Perbezaan utama antara asid hidrofluorik dan asid hidroklorik ialah Asid hidrofluorik adalah asid lemah manakala asid hidroklorik adalah asid yang kuat. Juga, asid hidrofluorik mampu membentuk ikatan hidrogen manakala asid hidroklorik tidak dapat membentuk ikatan hidrogen.
Selain itu, satu lagi perbezaan penting antara asid hidrofluorik dan asid hidroklorik berada dalam struktur molekul mereka. The Molekul asid hidrofluorik mempunyai ion fluorida manakala molekul asid hidroklorik mempunyai ion klorida. Selanjutnya, kedua -dua asid hidrofluorik dan hidroklorik adalah penderma proton. Oleh itu, molekul asid ini dapat mengionkan dalam medium berair yang melepaskan proton (h+). Proton ini menyebabkan keasidan dalam medium berair.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah asid hidrofluorik
3. Apakah asid hidroklorik
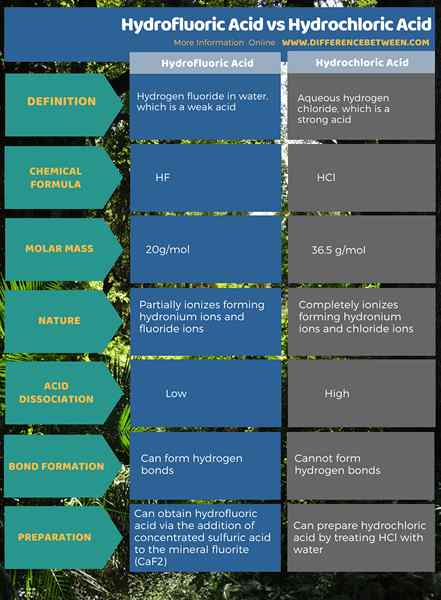
4. Perbandingan sampingan - asid hidrofluorik vs asid hidroklorik dalam bentuk tabular
5. Ringkasan
Apakah asid hidrofluorik?
Asid hidrofluorik adalah hidrogen fluorida di dalam air. Fluorida hidrogen adalah sebatian berasid yang mempunyai formula kimia HF dan jisim molar 20 g/mol. Selain itu, asid ini adalah sebatian permulaan untuk hampir semua sebatian yang mengandungi fluorin. Ex: Teflon. Asid ini sangat reaktif dengan kaca dan sederhana reaktif dengan logam. Oleh itu, ia disimpan dalam bekas plastik. Walau bagaimanapun, bekas yang diperbuat daripada Teflon sedikit telap kepada asid ini.

Rajah 01: sebotol asid hidrofluorik
Asid hidrofluorik adalah asid lemah. Itu kerana ia mempunyai pemalar pemisahan yang lebih rendah. Pemisahan asid ini memberikan ion hidronium (gabungan proton dan molekul air membentuk ion hidronium) dan ion fluorida. Antara asid hidrrohalic, ini adalah satu -satunya asid lemah. Kita boleh mendapatkan asid ini melalui penambahan asid sulfurik pekat ke fluorit mineral (CAF2).
Apakah asid hidroklorik?
Asid hidroklorik adalah klorida hidrogen berair. Hidrogen klorida mempunyai formula kimia HCl, dan jisim molarnya adalah 36.5 g/mol. Asid ini mempunyai bau pedas. Selain itu, penting sebagai sebatian permulaan untuk banyak bahan kimia bukan organik seperti vinil klorida.

Rajah 02: sebotol asid hidroklorik
Tidak seperti HF, HCL adalah asid kuat yang dapat mengionkan sepenuhnya dalam medium berair, membentuk ion hidronium dan ion klorida. Oleh itu, asid ini mempunyai nilai ka yang tinggi. Kita boleh menyediakan asid ini dengan merawat HCL dengan air.
Apakah perbezaan antara asid hidrofluorik dan asid hidroklorik?
Asid hidrofluorik adalah hidrogen fluorida di dalam air. Ia adalah asid yang lemah, dan ia boleh membentuk ikatan hidrogen. Asid hidroklorik adalah hidrogen klorida berair. Ia adalah asid yang kuat, dan ia tidak dapat membentuk ikatan hidrogen. Ini adalah perbezaan utama antara asid hidrofluorik dan asid hidroklorik.
Selanjutnya, molekul asid hidrofluorik mempunyai ion fluorida manakala molekul asid hidroklorik mempunyai ion klorida. Walau bagaimanapun, kedua -duanya adalah asid hidrogali yang mempunyai atom hidrogen yang terikat kepada halogen. Selain itu, asid hidrofluorik adalah satu -satunya asid lemah di kalangan asid hidrogali lain.
Ringkasan -Asid Hydrofluoric Vs Asid Hydrochloric
Asid hidrofluorik dan hidroklorik adalah asid hidrogali kerana kedua -dua sebatian asid ini mempunyai halida yang terikat pada atom hidrogen. Selain itu, terdapat banyak perbezaan antara kedua -dua asid ini. Perbezaan antara asid hidrofluorik dan asid hidroklorik ialah asid hidrofluorik adalah asid yang lemah dan ia boleh membentuk ikatan hidrogen manakala asid hidroklorik adalah asid kuat dan ia tidak dapat membentuk ikatan hidrogen.
Rujukan:
1. "Asid Hydrofluoric."Pusat Kebangsaan Maklumat Bioteknologi. Pangkalan data kompaun pubchem, u.S. Perpustakaan Perubatan Negara. Terdapat di sini
2. "Asid hidroklorik."Pusat Kebangsaan Maklumat Bioteknologi. Pangkalan data kompaun pubchem, u.S. Perpustakaan Perubatan Negara. Terdapat di sini
Ihsan gambar:
1.'Hydrogen Fluoride'by Pengguna: Dorgan-Diri Diri, (CC BY-SA 3.0) melalui Commons Wikimedia
2.'Asid hidroklorik 05' (domain awam) melalui wikimedia Commons


