Perbezaan antara asid nitrik dan asid nitrik pekat

The Perbezaan utama antara asid nitrik dan asid nitrik pekat ialah Asid nitrik fuming membentuk asap yang tidak berwarna, kekuningan atau kecoklatan sedangkan asid nitrik pekat biasanya tidak membentuk asap; Tetapi kepekatan asid ini yang sangat tinggi boleh memberikan asap berwarna putih.
Asid nitrik adalah asid yang sangat menghakis dan berbahaya yang mempunyai formula kimia hno3. Lebih -lebih lagi, ia boleh mempunyai sifat kimia cair atau pekat. Sama ada cara, ia mempunyai molekul asid nitrik yang dibubarkan di dalam air. Reaksi antara nitrogen dioksida dan air membentuk asid nitrik. Tetapi dalam penyediaan asid nitrik fuming, kita dapat menyediakannya dengan menambahkan nitrogen dioksida yang berlebihan kepada asid nitrik.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apa itu asid nitrik fuming
3. Apa itu asid nitrik pekat
4. Perbandingan sampingan - asid nitrik vs asid nitrik pekat dalam bentuk tabular
5. Ringkasan
Apa itu asid nitrik fuming?
Asid nitrik fuming adalah gred komersil asid nitrik yang mempunyai kepekatan yang sangat tinggi dan ketumpatan tinggi. Ia mengandungi 90-99% HNO3. Kita boleh menyediakan cecair ini melalui menambah nitrogen dioksida yang berlebihan kepada asid nitrik. Ia membentuk cecair fuming yang tidak berwarna, kekuningan atau kecoklatan yang sangat menghakis. Oleh itu, larutan asid ini mempunyai molekul gas dalam kombinasi dengan air; tidak ada air di dalamnya. Asap asid ini naik dari permukaan asid; Ini membawa namanya, "Fuming". Formula kimia sebatian ini adalah hno3-xTidak2.
Tambahan pula, terdapat dua bentuk utama asid ini sebagai asid nitrik putih dan merah. Oleh itu, kita menganggap asid fuming putih sebagai bentuk asid nitrik yang paling murni yang mempunyai kurang daripada 2%; kadang -kadang, tidak ada air sama sekali. Oleh itu, ia sangat dekat dengan asid nitrik anhydrous, dan ia boleh didapati sebagai penyelesaian 99%. Ia mengandungi maksimum 0.5% nitrogen dioksida. Ia berguna sebagai pengoksida yang boleh disimpan dan propelan roket.

Rajah 01: Asid nitrik putih fuming
Asid nitrik fuming merah terdiri daripada 90% HNO3. Ia mempunyai kandungan nitrogen dioksida yang tinggi, yang menjadikan penyelesaiannya muncul dalam coklat kemerahan. Ia mempunyai ketumpatan kurang dari 1.49 g/cm3. Jadi, ia juga berguna sebagai pengoksida yang boleh disimpan dan propelan roket. Untuk menyediakan asid ini, kita boleh menggunakan 84% asid nitrik dan 13% dinitrogen tetroksida dengan air 2%.
Kegunaan:
- Asid nitrik fuming merah adalah komponen monopropel.
- Berguna sebagai bahan bakar tunggal dalam roket.
- Sebagai pengoksidaan yang boleh disimpan.
- Asid nitrik putih fuming digunakan dalam pengeluaran bahan letupan. Ex: Nitrogliserin.
Apa itu asid nitrik pekat?
Asid nitrik pekat hanyalah penyelesaian yang mengandungi lebih banyak asid nitrik dalam air yang kurang. Ini bermakna bentuk asid ini tertumpu mengandungi jumlah air yang kurang berbanding dengan jumlah larutan di dalamnya. Dalam skala komersial, 68% atau ke atas dianggap sebagai asid nitrik pekat.

Rajah 02: 70% asid nitrik
Selain itu, ketumpatan penyelesaian ini ialah 1.35 g/cm3. Kepekatan ini tidak menghasilkan asap, tetapi kepekatan asid ini yang sangat tinggi boleh memberikan asap berwarna putih. Kita boleh menghasilkan cecair ini melalui reaksi nitrogen dioksida dengan air.
Apakah perbezaan antara asid nitrik dan asid nitrik pekat?
Asid nitrik fuming adalah gred komersil asid nitrik yang mempunyai kepekatan yang sangat tinggi dan ketumpatan tinggi. Selain itu, ia membentuk asap yang tidak berwarna, kekuningan atau kecoklatan. Kepekatan terendah asid ini ialah 90%. Asid nitrik pekat hanyalah penyelesaian yang mengandungi lebih banyak asid nitrik dalam air yang kurang. Kepekatan terendah asid ini ialah 68%. Di samping itu, asid ini biasanya tidak membentuk asap; Tetapi kepekatan asid ini yang sangat tinggi boleh memberikan asap berwarna putih. Infographic berikut memberikan lebih banyak butiran mengenai perbezaan antara asid nitrik dan asid nitrik pekat.
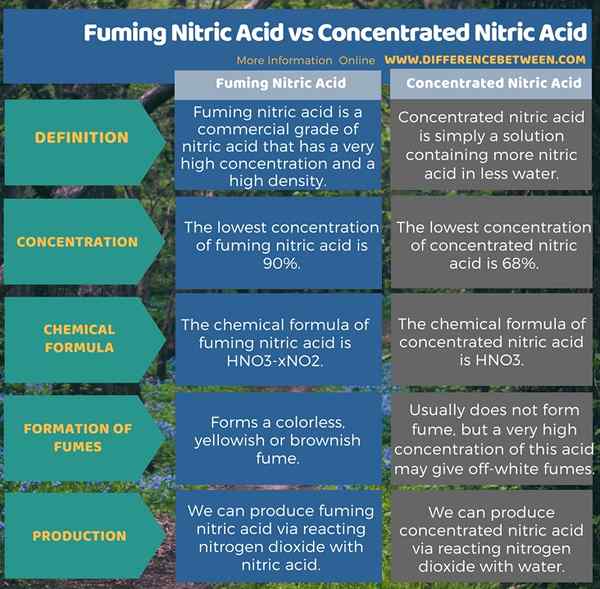
Ringkasan -Asid nitrik yang memusnahkan vs asid nitrik pekat
Terdapat dua bentuk asid nitrik dengan kepekatan tinggi HNO3; mereka memusnahkan asid nitrik dan asid nitrik pekat. Perbezaan utama antara asid nitrik dan asid nitrik pekat adalah bahawa asid nitrik fuming membentuk fuming yang tidak berwarna, kekuningan atau kecoklatan sedangkan asid nitrik pekat biasanya tidak membentuk asap; Tetapi kepekatan asid ini yang sangat tinggi boleh memberikan asap berwarna putih.
Rujukan:
1. "Asid nitrik."Wikipedia, Yayasan Wikimedia, 31 Julai 2018. Terdapat di sini
2. "Asid nitrik."Pusat Kebangsaan Maklumat Bioteknologi. Pangkalan data kompaun pubchem, u.S. Perpustakaan Perubatan Negara. Terdapat di sini
Ihsan gambar:
1.'Asid nitrik fuming'by w. OELEN (CC BY-SA 3.0) melalui Commons Wikimedia
2.'Asid nitrik 70'by Aleksander Sobolewski melalui Wikimedia Commons, (CC by-SA 4.0) melalui Commons Wikimedia


