Perbezaan antara esterifikasi dan penetapan
The Perbezaan utama antara esterifikasi dan peneutralan ialah Estification menghasilkan ester dari asid dan alkohol, sedangkan peneutralan menghasilkan garam dari asid dan asas.
Estification and Neutralization adalah dua reaksi penting kimia. Estification, seperti namanya, adalah tindak balas kimia yang menghasilkan ester pada akhir reaksi. Neutralisasi merujuk kepada pengimbangan keasidan dari kealkalian.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah esterifikasi
3. Apa itu peneutralan
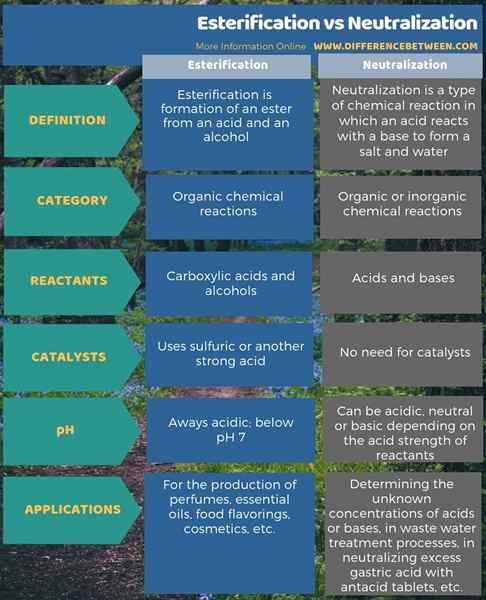
4. Perbandingan sampingan - esterifikasi vs peneutralan dalam bentuk jadual
5. Ringkasan
Apakah esterifikasi?
Estification adalah proses membentuk ester dari asid dan alkohol. Asid biasanya asid karboksilik, dan alkohol harus menjadi alkohol primer atau sekunder. Dan, tindak balas berlaku dalam persekitaran berasid. Oleh itu, kita menggunakan asid sulfurik sebagai asid kuat untuk reaksi. Ia bertindak sebagai pemangkin untuk tindak balas kerana campuran asid karboksilik dan alkohol tidak memberikan apa -apa jika medium tidak berasid. Sebagai hasil sampingan, molekul air terbentuk. Oleh itu, ini adalah reaksi pemeluwapan.
Ikatan Pi dalam kumpulan karbonil asid karboksilik boleh bertindak sebagai asas kerana herotan elektron disebabkan oleh perbezaan elektronegativiti antara oksigen dan atom karbon. Elektron dalam ikatan Pi diberikan kepada satu atom hidrogen dalam molekul asid sulfurik. Oleh itu, ini menukarkan ikatan -c = o ke -c -oh.
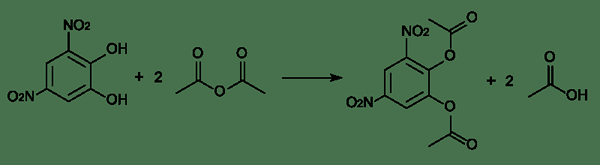
Rajah 01: Contoh tindak balas esterifikasi
Di sini, atom karbon mempunyai caj positif kerana hanya mempunyai tiga ikatan kimia di sekelilingnya. Kami menyebutnya sebagai karbohidrat. Di hadapan alkohol, pasangan elektron tunggal dalam atom oksigen alkohol dapat memberikan elektron ke atom karbon karbokati. Oleh itu, alkohol bertindak sebagai nukleofil. Selepas itu, penyusunan semula berlaku dan membentuk ester dan molekul air.
Apa itu peneutralan?
Neutralisasi adalah jenis tindak balas kimia di mana asid bertindak balas dengan asas untuk membentuk garam dan air. Oleh itu, tindak balas ini melibatkan gabungan h+ ion dan oh- ion, dan ia menjana air. Oleh itu, tidak ada ion hidrogen atau ion hidroksida yang berlebihan dalam campuran tindak balas selepas selesai reaksi.

Jika asid kuat bertindak balas dengan asas yang kuat, maka pH campuran tindak balas akhir adalah 7. Selain daripada itu, pH campuran tindak balas bergantung kepada kekuatan asid reaktan. Apabila mempertimbangkan aplikasi peneutralan, adalah penting dalam menentukan kepekatan asid atau asas yang tidak diketahui, dalam proses rawatan air sisa, dalam meneutralkan asid gastrik yang berlebihan dengan tablet antacid, dll.
Apakah persamaan antara esterifikasi dan peneutralan?
- Kedua -dua tindak balas menghasilkan air sebagai hasil sampingan
- Kedua -dua reaksi melibatkan gabungan h+ ion dan oh-
Apakah perbezaan antara esterifikasi dan peneutralan?
Estification dan Neutralisasi adalah tindak balas penting dalam kimia. Perbezaan utama antara esterifikasi dan peneutralan adalah bahawa esterifikasi menghasilkan ester dari asid dan alkohol, sedangkan peneutralan menghasilkan garam dari asid dan asas. Tambahan pula, reaktan untuk esterifikasi adalah asid karboksilik dan alkohol sementara untuk peneutralan, reaktan adalah asid dan pangkalan.
Selain itu, perbezaan lain antara esterifikasi dan peneutralan adalah bahawa esterifikasi memerlukan pemangkin seperti asid sulfurik sementara peneutralan tidak memerlukan pemangkin.
Ringkasan -Estification vs Neutralisasi
Estification dan Neutralisasi adalah tindak balas penting dalam kimia. Ringkas.
Rujukan:
1. "Mekanisme Estification (Kimia Organik) - KimiaSkor."Belajar kimia di sini, 19 Sept. 2018, boleh didapati di sini.
2. Admin. "Ester - proses esterifikasi dengan struktur, sifat & kegunaan."Byjus, Byju, 25 Julai 2018, boleh didapati di sini.
Ihsan gambar:
1. "Estification 3,5-Dinitrocatechol" oleh Megabyte07-Kerja Sendiri (CC BY-SA 3.0) melalui Commons Wikimedia
2. "Titolazione" oleh Luigi Chiesa - Ditarik oleh Luigi Chiesa (Domain Awam) melalui Commons Wikimedia


