Perbezaan antara pemalar keseimbangan dan kadar pemalar
The Perbezaan utama antara pemalar keseimbangan dan pemalar kadar adalah bahawa Pemalar keseimbangan dinyatakan menggunakan kedua -dua kepekatan reaktan dan produk, sedangkan pemalar kadar dinyatakan menggunakan kepekatan reaktan atau produk.
Kedua -duanya, pemalar keseimbangan dan pemalar kadar, adalah nilai malar untuk tindak balas tertentu. Maksudnya, pada tindak balas yang tetap, keadaan seperti suhu, nilai pemalar keseimbangan, dan pemalar kadar tidak berubah dengan masa. Tambahan pula, dalam menyatakan keseimbangan keseimbangan, kita harus mempertimbangkan pekali stoikiometrik juga. Tetapi, untuk pemalar kadar, kita perlu menentukan nilai hanya menggunakan kaedah eksperimen.
Kandungan
1. Gambaran Keseluruhan dan Perbezaan Utama
2. Apakah keseimbangan keseimbangan
3. Apakah kadar pemalar
4. Perbandingan sampingan - keseimbangan vs. Nilai pemalar dalam bentuk jadual
5. Ringkasan
Apakah keseimbangan keseimbangan?
Pemalar keseimbangan adalah nisbah antara kepekatan produk dan kepekatan reaktan pada keseimbangan. Kita boleh menggunakan istilah ini hanya dengan reaksi yang ada dalam keseimbangan. Reaksi reaksi dan pemalar keseimbangan adalah sama untuk reaksi yang ada dalam keseimbangan.
Lebih -lebih lagi, kita harus memberikan pemalar ini dengan menggunakan kepekatan yang dibangkitkan kepada kuasa pekali stoikiometrik. Pemalar keseimbangan bergantung pada suhu sistem kerana suhu mempengaruhi kelarutan komponen dan pengembangan isipadu. Walau bagaimanapun, persamaan untuk pemalar keseimbangan tidak termasuk butiran mengenai pepejal yang antara reaktan atau produk. Hanya bahan dalam fasa cecair dan fasa gas yang dipertimbangkan.
Sebagai contoh, keseimbangan antara asid asetik dan ion asetat adalah seperti berikut:
Ch3COOH ⇌ CH3COO- + H+
Pemalar keseimbangan, KC untuk tindak balas ini adalah seperti berikut:
Kc = [ch3COO-] [H+]/[Ch3Cooh]

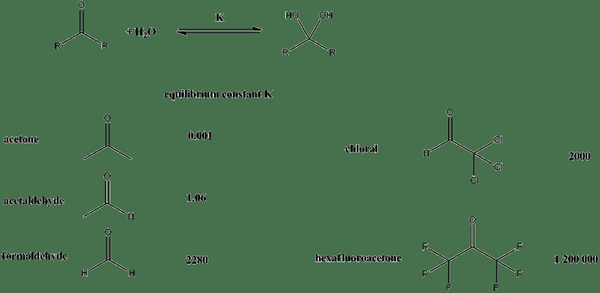
Rajah 01: Pemalar keseimbangan untuk sebatian yang berbeza
Apakah kadar pemalar?
Pemalar kadar adalah pekali perkadaran yang berkaitan dengan kadar tindak balas kimia pada suhu yang diberikan kepada kepekatan reaktan atau produk reaksi. Sekiranya kita menulis persamaan kadar berhubung dengan reaktan A untuk tindak balas yang diberikan di bawah, ia adalah seperti berikut.
AA + BB ⟶ CC + DD
R = -k [a] a [b] b
Dalam tindak balas ini, k adalah kadar pemalar. Ia adalah pemalar perkadaran yang bergantung pada suhu. Kita dapat menentukan kadar dan pemalar kadar tindak balas oleh eksperimen.
Apakah perbezaan antara pemalar keseimbangan dan kadar pemalar?
Perbezaan utama antara pemalar keseimbangan dan pemalar kadar adalah bahawa pemalar keseimbangan dinyatakan menggunakan kedua -dua kepekatan reaktan dan produk, sedangkan pemalar kadar dinyatakan menggunakan sama ada kepekatan reaktan atau produk. Tambahan pula, pemalar keseimbangan diberikan untuk tindak balas keseimbangan, sementara pemalar kadar dapat diberikan untuk sebarang reaksi.
Selain itu, dalam menyatakan pemalar keseimbangan, kita boleh menggunakan kepekatan reaktan dan produk bersama -sama dengan pekali stoikiometrik sementara, dalam menyatakan kadar pemalar, kita tidak boleh menggunakan pekali stoikiometrik kerana kita perlu menentukan nilai eksperimen yang berterusan. Selain itu, pemalar keseimbangan menerangkan campuran tindak balas yang tidak berubah, sementara pemalar kadar menerangkan campuran tindak balas yang berubah dengan masa.
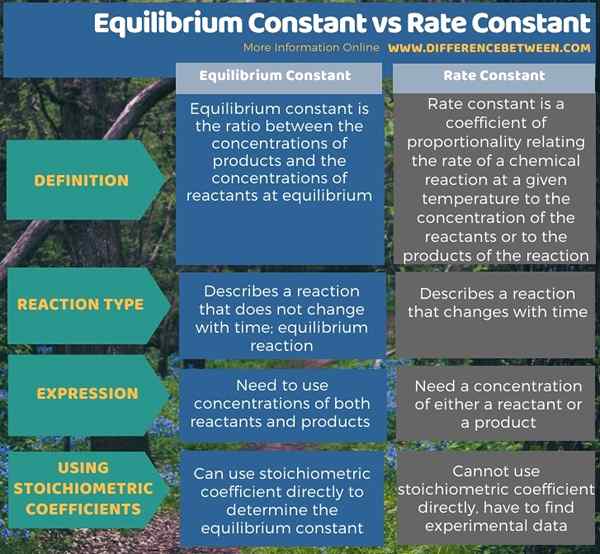
Ringkasan -keseimbangan keseimbangan vs. Kadar pemalar
Ringkasnya, kedua -duanya, pemalar keseimbangan dan kadar pemalar, jangan berubah dengan masa jika keadaan tindak balas seperti suhu tidak berubah. Walau bagaimanapun, perbezaan utama antara pemalar keseimbangan dan pemalar kadar adalah bahawa pemalar keseimbangan dinyatakan menggunakan kedua -dua kepekatan reaktan dan produk, sedangkan pemalar kadar dinyatakan menggunakan kepekatan reaktan atau produk.
Rujukan:
1. Helmenstine, Anne Marie. "Berapakah kadar pemalar dalam kimia?"Pemikiran, Sep. 27, 2018, boleh didapati di sini.
2. "Pemalar keseimbangan, k."Kimia Libreetexts, Libretexts, 5 Jun 2019, boleh didapati di sini.
Ihsan gambar:
1. "Hidrasi."Oleh Nikolaivica - Kerja Sendiri (CC BY -SA 3.0) melalui Commons Wikimedia


